
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Работа 9. Химическая природа гемпротеидов
|
|
|
|
Состав и свойства сложных белков
Сложные белки являются представителями смешанных макромолекул, которые содержат как минимум два разных химических компонента, соединенных ковалентными или слабыми (ионными, водородными, вандерваальсовыми) связями. К сложным белкам относят кофакторпротеиды (гемпротеиды, хлорофиллпротеиды, флавопротеиды и др.), гликопротеиды и протеогликаны, липопротеиды и протеолипиды, металлопротеиды, фосфопротеиды и нуклеопротеиды.
Особенность строения этих макромолекул позволяет использовать при обнаружении и количественном определении их в биологическом материале методы анализа как на белковый фрагмент молекулы, так и на простетическую группу. Поскольку последняя специфична для каждого класса сложных белков, реакции на нее применяются чаще.
К гемпротеидам относят гемоглобин, миоглобин, цитохромы и ферменты – каталазу и пероксидазу. Они состоят из белковой части и гема, представляющего собой тетрапиррольное соединение, связанное с атомом железа (II).
При действии на гемоглобин концентрированной уксусной кислоты в присутствии NaCl гем переходит в гемин, в котором железо трехвалентно и его третья валентность связана с хлором. При действии на гемоглобин щелочей гем переходит в гематин, в котором атом железа также трехвалентен, и третья его валентность связана с гидроксильной группой.
Гем, входящий в гемоглобин, ускоряет реакцию окисления субстратов (S·H2) пероксидом водорода, т.е. действует подобно ферменту пероксидазе: S·H2 + H2O2 – S + 2H2O. Это объясняется сходством строения простетических групп гемоглобина и пероксидазы. Однако в отличие от фермента гемоглобин сохраняет каталитические свойства при кипячении и действии сильных кислот, которые вызывают денатурацию белка.
Если в исследуемом материале содержится кровь, то ее присутствие можно обнаружить по способности геминовой группы катализировать окисление подходящих субстратов (бензидин, гвояковая смола) пероксидом водорода.
Реактивы. Пероксид водорода, 3%-ный свежеприготовленный раствор; бензидин, 5%-ный свежеприготовленный раствор в ледяной уксусной кислоте; гваяковая смоляная кислота, 1%-ный раствор на 95%-ном этиловом спирте, свежеприготовленный; азотная кислота, конц.; соляная кислота, не содержащая железа, 10%-ный раствор; гексацианоферрат (II) калия, 2,5%-ный раствор; роданид аммония, 1%-ный раствор; гидроксид натрия, 3%-ный раствор; биуретовый реактив*; ацетон, подкисленный соляной кислотой (3 мл 2 М раствора HCl на 1 л ацетона, рН≈2), охлажденный в холодильнике.
Оборудование. Полоски фильтровальной бумаги шириной 1 см; глазные пипетки; пипетки вместимостью 1 и 10 мл; штатив; простые и центрифужные пробирки; водяная и песчаная бани; центрифуга с центрифужными весами; тигель фарфоровый и тигельные щипцы.
Материал.
1. Цельная кровь, разведенная в 5000 раз дистиллированной водой.
2. Кровь дефибринированная.
3. Гемоглобин кристаллический, 1%-ный водный раствор.
а. Бензидиновая проба на геминовую группу гемоглобина. Метод основан на способности геминовой группы гемоглобина катализировать реакцию окисления бензидина в дифенохинондиимин пероксидом водорода
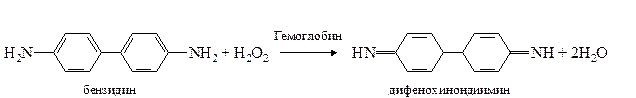
Дифенохинондиимин конденсируется с молекулой неокисленного бензидина с образованием окрашенного комплекса сине-зеленого цвета.
В пробирку наливают 1 мл цельной крови, разведенной в 5000 раз, кипятят несколько минут на водяной бане, охлаждают и добавляют по 2 капли раствора бензидина и пероксида водорода. Отмечают появление окрашивания.
б. Гваяковая проба на геминовую группу гемоглобина. Метод основан на способности геминовой группы гемоглобина катализировать реакцию окисления гваяковой смоляной кислоты пероксидом водорода до ее озонида, окрашенного в синий цвет.
Ход определения. В пробирку вносят несколько капель цельной крови (разведенной в 5000 раз) и кипятят ее в течение 1 мин на водяной бане. После охлаждения приливают к пробе 1-2 капли спиртового раствора гваяковой смоляной кислоты и 3 капли раствора пероксида водорода. Отмечают развитие окрашивания.
в. Проба с гексацианоферратом (II) калия и роданидом аммония на железо гемоглобина. Метод основан на способности железа, входящего в гемоглобин, образовывать с гексацианоферратом (II) калия в присутствии соляной кислоты сине-зеленое комплексное соединение – берлинскую лазурь:
4FeCl3 + 3K4[Fe(CN)6] → Fe4[Fe(CN)6]3 + 12KCl,
гексацианоферрат (II) берлинская
калия лазурь
а с роданидами – роданид железа розового или красного цвета:
FeCl3 + 3NH4CNS → Fe(CNS)3 + 3KCl
роданид роданид
аммония железа
Ход определения. Несколько капель дефибринированной крови помещают в фарфоровую чашечку (тигель) и выпаривают досуха на песчаной бане. Сухой остаток озоляют, добавляют 2-3 капли концентрированной азотной кислоты и продолжают нагревание (под тягой). При этом железо гемоглобина переходит в состав золы.
Сухой остаток переносят в пробирку, добавляют 10 капель раствора соляной кислоты до растворения золы. Разливают содержимое примерно поровну в две пробирки. В одну из них добавляют 2 капли раствора гексацианоферрата (II) калия. Наблюдают за появлением характерного окрашивания. Во вторую пробирку приливают 2 капли раствора роданида аммония и отмечают развитие специфического окрашивания.
г. Разделение гемоглобина на гем и глобин. Метод основан на способности ацетона, подкисленного соляной кислотой, разрывать связи между гемом и глобином, причем отщепившийся гем растворяется в ацетоне, а глобин выпадает в осадок.
Ход определения. В пробирку наливают 10 мл подкисленного ацетона и медленно добавляют 10 капель раствора гемоглобина. Наблюдают появление беловатой взвеси (глобин), которая постепенно оседает. Содержимое пробирки перемешивают стеклянной палочкой, переливают в центрифужные пробирки и центрифугирую при 1500 об/мин в течение 5 мин.
После центрифугирования в верхний слой (ацетоновый) осторожно опускают две полоски фильтровальной бумаги и проделывают реакции на наличие геминовой группировки. Для этого на одну полоску наносят по капле бензидина и раствора пероксида водорода (бензидиновая проба), на вторую –по две капли спиртового раствора гваяковой смоляной кислоты и раствора пероксида водорода (гваяковая проба). Отмечают постепенное появление характерного окрашивания на обеих полосках бумаги.
Верхний слой жидкости осторожно сливают, а к оставшемуся осадку добавляют 1 мл 3%-ного раствора гидроксида натрия. Перемешивают содержимое и добавляют 10 капель биуретового реактива. Наблюдают появление характерного окрашивания.
Оформление работы. Результаты оформить в виде таблицы.
| Компонент гемоглобина | Вид реакции | Характер окрашивания |
В выводах указать на возможность обнаружения гемоглобина в исследуемом материале с помощью проделанных качественных реакций и разделения его компонентов действием кислых растворов ацетона; отметить значение реакций для практики.
Практическое значение работы. Основная часть гемпротеидов крови находится в виде гемоглобина эритроцитов. В сыворотке или плазме крови содержится лишь незначительное количество гемпротеидов, появляющихся при значительном распаде эритроцитов (гемолизе). В сыворотке крови железо находится в виде ферротрансферина, являющегося сложным белком (металлопротеидом), который переносит железо между тканями и органами.
Качественные реакции на простетические группы протеидов позволяют выявить структурные компоненты: геминовую группировку и входящее в состав гема железо. Для обнаружения следов крови очень чувствительные бензидиновая и гваяковые пробы используются в клинике и судебно-медицинских исследованиях.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 1306; Нарушение авторских прав?; Мы поможем в написании вашей работы!