
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение универсальной газовой постоянной
|
|
|
|
Оборудование: 1) шар для взвешивания воздуха с резиновым патрубком и винтовым зажимом; 2) манометр с пределами измерения от –1,0 до 1,5 атм; 3) термометр от 0 до 30˚С, 4) насос воздушный ручной; 5) весы технические (нагрузка до 1кг) с разновесами; 6) тройник стеклянный; 7) три резиновые трубки длиной по 20–30 см.
В предлагаемой работе определение универсальной газовой постоянной производится из сравнения двух различных состояний газа. Если масса m1 занимает в баллоне объем V1 при давлении р1 и температуре T1, то это состояние может быть описано уравнением Менделеева–Клапейрона:
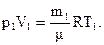 (1)
(1)
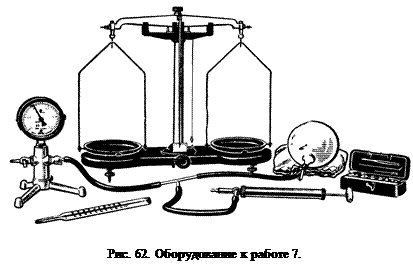
При изменении массы газа путем откачки или нагнетания его в баллон без изменения температуры образуется второе состояние газа, определяемое следующими параметрами: m2, p2, V1, T1. Уравнение Менделеева–Клапейрона для этого состояния можно записать так:
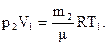 (2)
(2)
Вычитая из равенства (2) равенство (1), получим:
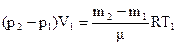
отсюда 
Здесь объем газа V1 и температура T1 для обоих состояний остаются постоянными. Давления p1 и p2 легко измеряются с помощью манометра. Для определения же разности m2–m1 достаточно произвести два взвешивания: определить массу баллона с газом для одного и другого состояний и найти разность между результатами взвешивания. Пусть, например, mб – масса баллона, тогда
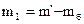 и
и 
отсюда 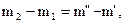
где m' и m"– массы баллона с газом для соответствующих состояний, μ = 2,9·10-2 кг/моль.
Выполнение работы
Измеряют температуру воздуха в помещении. Записывают объем шара (объем обозначен на стенке шара, например, 1,23 дм3). Собирают установку. С помощью стеклянного тройника и резиновых трубок соединяют шар с манометром и откачивающим патрубком насоса. Медленно откачивая воздух, понижают давление в шире до 0,5 атм и надежно сжимают резиновый патрубок винтовым зажимом. Отсоединяют шар от установки и взвешивают его.
Для того чтобы получить второе состояние воздуха, отпускают зажим у шара и подключают его вновь к установке, а резиновую трубку с разрежающего патрубка насоса переставляют на нагнетающий. С помощью насоса доводят давление воздуха в системе до 1 атм. Снова сжимают патрубок у шара, отсоединяют шар от системы и взвешивают его. Опыт повторяют ещё 2–3 раза, увеличивая каждый раз давление на 0,5 атм и определяя массу шара с воздухом. Все результаты измерений заносят в таблицу:
| № опыта | |||||
| ρ, 104 Н/м2 | |||||
| m, 10-3 кг |
Пользуясь данными таблицы, вычисляют значение универсальной газовой постоянной R для каждого состояния, а затем ее среднее значение.
| № состояний | 1-2 | 1-3 | 1-4 | 1-5 | 2-3 | 2-4 | 2-5 | 3-4 | 3-5 |
R, 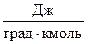
|
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 1247; Нарушение авторских прав?; Мы поможем в написании вашей работы!