
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные законы и формулы
|
|
|
|
1. Количество теплоты, сообщенное телу при теплообмене:
 ,
,
где С – теплоемкость тела; Т – термодинамическая температура.
2. Виды теплоемкостей тел и связь между ними:
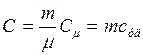 ,
,
где 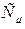 - молярная теплоемкость тела;
- молярная теплоемкость тела;  - удельная теплоемкость тела.
- удельная теплоемкость тела.
3. Молярные теплоемкости при разны процессах:
 ;
; 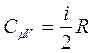 ,
,
где 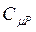 - молярная теплоемкость при изобарическом процессе;
- молярная теплоемкость при изобарическом процессе;
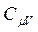 - молярная теплоемкость при изохорическом процессе.
- молярная теплоемкость при изохорическом процессе.
4. Уравнение Роберта-Майера:
 .
.
5. Внутренняя энергия идеального газа:
 ,
,
где m - масса газа;  - молярная масса газа;
- молярная масса газа;
 - число степеней свободы молекулы;
- число степеней свободы молекулы;
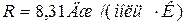 - молярная газовая постоянная;
- молярная газовая постоянная;
Т – термодинамическая температура.
или
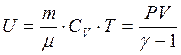
6. Элементарная работа, связанная с изменением объема газа:
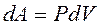 или
или  ,
,
где  и
и 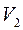 - начальный и конечный объемы газа.
- начальный и конечный объемы газа.
7. Первое начало (закон) термодинамики
a) в дифференциальной форме:
 ,
,
где 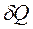 - количество тепла, сообщенное системе;
- количество тепла, сообщенное системе;
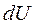 - изменение внутренней энергии системы;
- изменение внутренней энергии системы;
 - работа, совершенная системой.
- работа, совершенная системой.
б) в интегральной форме:
 .
.
8. Работа газа при изотермическом процессе
 ,
,
где 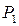 и
и  - начальное и конечное давления.
- начальное и конечное давления.
9. Уравнение адиабатического процесса (уравнение Пуассона):
 или
или  ,
,
где  - показатель адиабаты.
- показатель адиабаты.
10. Термический коэффициент полезного действия тепловой машины:
 ,
,
где  - количество тепла, полученное системой от нагревателя;
- количество тепла, полученное системой от нагревателя;
A – работа цикла.
11. Термический коэффициент цикла Карно:
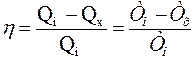 ,
,
где  - тепло, полученное от нагревателя;
- тепло, полученное от нагревателя;
 - тепло, переданное холодильнику;
- тепло, переданное холодильнику;
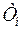 - температура нагревателя;
- температура нагревателя; 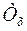 - температура холодильника
- температура холодильника
12. Изменение энтропии двух состояний системы:
 ,
,
где  и
и  - начальное и конечное состояние системы. Знак равенства соответствует обратимом процессу, а знак неравенства – необратимому.
- начальное и конечное состояние системы. Знак равенства соответствует обратимом процессу, а знак неравенства – необратимому.
 - элементарное количество теплоты, полученное телом при температуре Т.
- элементарное количество теплоты, полученное телом при температуре Т.
 ,
,
т.е изменение энтропии идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида процесса перехода.
При адиабатическом процессе:
 ;
;  .
.
При изотермическом процессе:
 .
.
При изохорном процессе:
 .
.
13. Энтропия для квазистационарных процессов:
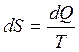 .
.
14. Формула Больцмана:
 ,
,
где  - энтропия системы;
- энтропия системы;
 - термодинамическая вероятность состояния системы;
- термодинамическая вероятность состояния системы;
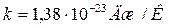 - постоянная Больцмана.
- постоянная Больцмана.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 545; Нарушение авторских прав?; Мы поможем в написании вашей работы!