
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Галогенированиеароматических соединений
|
|
|
|
Схема и механизм галогенирования аренов
Общая схема реакции может быть представлена следующим образом:

Иногда вместо галогена используются гипогалогенные кислоты:

При иодировании используются окислители или хлориод.
В качестве катализаторов процесса галогенированиячаще всего используют кислоты Льюиса (FeCl3 и др.), концентрированную серную кислоту, иод.
Галогенирование аренов протекает как реакция электрофильного замещения атома водорода.

Электрофильными частицами (Е+) обычно являются галоген-катион, поляризованный комплекс галогена с кислотой Льюиса и поляризованная молекула галогена, а в случае гипогалогенных кислот — катион HlgOH2+ или галоген-катион. Их образованию способствуют катализаторы или растворитель.
Механизм образования электрофильных частиц зависит от взятого катализатора и других условий проведения реакции.
1. Катализ кислотами Льюиса. В промышленности чаще всего реакцию проводят в присутствии галогенида железа (III ), который, как правило, получают прямо в реакционной массе при добавлении в нее железа.

При хлорировании аренов в этих условиях электрофильной частицей является хлорид-катион. При бромировании (а также и иодировании) в присутствии FeBr3 и других малоактивных кислот Льюиса, образование катиона галогена идет в незначительной степени, а основной атакующей частицей является поляризованный комплекс, например:
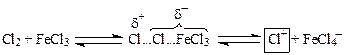

Аналогично протекает катализ другими кислотами Льюиса.
2. Катализ серной кислотой:


3. Катализ иодом:

При использовании каталитических количеств иода арены хлорируются, так как образуется катион Сl+, а при соотношениях близких к эквимолекулярным образуется I+ и идет иодирование.
4. Каталитическое влияние растворителя. Роль электрофильной частицы может выполнять и поляризованная молекула галогена.

Степень ее поляризации зависит от полярности растворителя. В связи с этим галогенирование активных субстратов (ароматических аминов, фенолов, полиалкилбензолов типа мезитилена, нафталина, и т. п.) молекулярным хлором и бромом возможно и без катализатора. В воде при комнатной температуре амины и фенолы образуют тригалогенпроизводные.
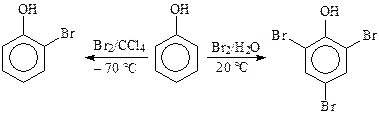
Однако в неполярном растворителе при низкой температуре (–70 °С) даже при избытке галогена получаются лишь монозамещенные фенолы. Бромирование фенолов в этом случае идет исключительно в о -положение. Для получения монозамещенных первичных аминов их предварительно ацилируют по аминогруппе.

|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 432; Нарушение авторских прав?; Мы поможем в написании вашей работы!