
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гидрофобные взаимодействия
|
|
|
|
Термин «гидрофобные взаимодействия» был предложен Ленгмюром еще в 1916 г. при выводе уравнения изотермы мономолекулярной адсорбции. Они возникают только в водных растворах в результате взаимодействия полярных молекул воды с неполярными гидрофобными частицами, молекулами (углеводородами) или неполярными радикалами молекул, в частности неполярными радикалами молекул ПАВ.
Гидрофобные взаимодействия вызваны особенностями структуры воды. Между молекулами воды образуются водородные связи (показаны пунктиром):
 Энергия водородной связи между молекулами воды больше энергии взаимодействия молекул воды с неполярными частицами и радикалами.
Энергия водородной связи между молекулами воды больше энергии взаимодействия молекул воды с неполярными частицами и радикалами.
Кроме того, вода является сильноассоциированной структурированной жидкостью. Наряду с упорядоченной, но рыхлой структурой (плотность структурированной твердой фазы — льда — меньше плотности воды) существует более плотная, лишенная упорядоченности структура. Растворение углеводородов в воде приводит к тому, что структура становится более упорядоченной. Следствием этого является увеличение числа водородных связей в воде.
Значительная энергия взаимодействия между молекулами воды за счет водородных связей и увеличение числа этих связей предопределяет притяжение гидрофобных частиц, т.е. гидрофобное взаимодействие. На рис. 5.6 схематически показано возникновение гидрофобных взаимодействий между двумя гидрофобными неполярными частицами 1 и 2. Эти частицы окружены молекулами воды, которые самопроизвольно ориентируются на границе с неполярной средой, образуя сначала максимально уплотненный мономолекулярный слой 3. Этот монослой является своеобразной «матрицей» для построения за счет водородных
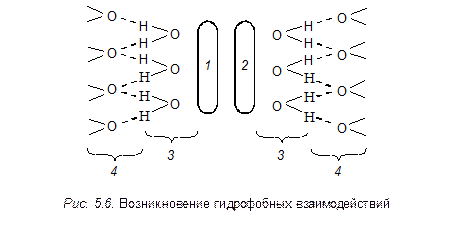 |
связей следующих слоев 4 и образования структуры в объеме системы. Образовавшаяся вокруг частиц структура способствует сближению частиц. Таким
 |
образом, неполярные частицы прижимаются друг к другу окружающими их молекулами воды.
Гидрофобные взаимодействия выполняют лишь ориентирующую функцию — они обеспечивают наиболее предпочтительный контакт между родственными гидрофобными частицами. Сам же контакт реализуется за счет межмолекулярных (ван-дер-ваальсовых), электростатических, донорно-акцепторных и других сил.
Возникновение гидрофобных взаимодействий получило термодинамическое обоснование. Процесс растворения в воде неполярных гидрофобных веществ, а также ПАВ, приводит к снижению энтропии (ΔS < 0). Оно происходит за счет изменения свойств воды в результате вкрапления в нее неполярных частиц и формирования более упорядоченной по сравнению с чистой водой структуры.
Гидрофобные взаимодействия определяют адсорбцию молекул ПАВ на границе раздела фаз. В результате растворения ПАВ, молекулы которых имеют неполярный гидрофобный радикал, происходит увеличение числа водородных связей в структуре воды и понижение энтропии системы (т.е. водного раствора ПАВ). Реакцией системы на понижение энтропии будет такая перестройка, которая приведет к максимально возможному повышению энтропии. В свою очередь повышение энтропии обусловливает уменьшение числа контактов между неполярными радикалами молекул ПАВ и молекулами воды, что достигается путем самопроизвольного выталкивания молекул ПАВ из объема на поверхность и адсорбции. Подчеркнем, что самопроизвольный процесс адсорбции обусловлен присутствием неполярного гидрофобного радикала в молекулах ПАВ.
Свободная энергия переноса молекул ПАВ из объема раствора на поверхность в расчете на одну СН2 группу примерно равна 3 кДж/моль; относительное постоянство ее значения служит своеобразным подтверждением правила Траубе-Дюкло.
Гидрофобные взаимодействия имеют место и при нахождении молекул ПАВ в адсорбционном слое. На границе раздела фаз неполярные радикалы молекул ПАВ сохраняют контакт с водой. При малых концентрациях молекулы ПАВ располагаются на определенном расстоянии друг от друга и как бы плавают на поверхности. При увеличении концентрации ПАВ и по мере насыщения адсорбционного слоя происходит сближение молекул в поверхностном слое, и между неполярными углеводородными радикалами молекул ПАВ возникают двухмерные гидрофобные взаимодействия. В отличие от трехмерных гидрофобных взаимодействий в объеме системы двухмерные взаимодействия распространяются в двух взаимно перпендикулярных направлениях по отношению к границе раздела фаз.
Двухмерные гидрофобные взаимодействия слабее трехмерных, так как углеводородный радикал лишь частично погружен в воду. Они растут с увеличением размеров углеводородных радикалов молекул ПАВ, поскольку последнее способствует их горизонтальной ориентации в адсорбционном слое, что благоприятствует двухмерным гидрофобным взаимодействиям.
Гидрофобные взаимодействия оказывают влияние на устойчивость дисперсных систем, мицеллообразование коллоидных ПАВ, конформацию белковых молекул, а также на ряд других явлений, которые будут рассмотрены в последующих главах.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 3846; Нарушение авторских прав?; Мы поможем в написании вашей работы!