
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гидролиз солей. Химическое обменное взаимодействие ионов растворенной соли с водой, приводящее к образованию слабодиссоциирующих продуктов (молекул слабых кислот или
|
|
|
|
Химическое обменное взаимодействие ионов растворенной соли с водой, приводящее к образованию слабодиссоциирующих продуктов (молекул слабых кислот или оснований, анионов кислых или катионов основных солей) и сопровождающееся изменением рН среды, называется гидролизом.
Пример 1. Составьте молекулярные и ионно-молекулярные уравнения гидролиза солей: а) KCN б) Na2CO3 в) ZnSO4. Определите реакцию среды растворов этих солей.
Решение. а) Цианид калия KCN - соль слабой одноосновной кислоты (см. табл. 9) HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К+ и анионы CN-.Катионы K+ не могут связывать ионы ОН- воды, так как КОН - сильный электролит. Анионы же CN- связывают ионы Н+ воды, образуя молекулы слабого электролита HCN. Соль гидролизуется, как говорят, по аниону. Ионно-молекулярное уравнение гидролиза
CN- + Н20 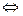 HCN + ОН-
HCN + ОН-
или в молекулярной форме
KCN + Н20 
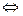 HCN + КОН
HCN + КОН
В результате гидролиза в растворе появляется некоторый избыток ионов ОН-, поэтому раствор KCN имеет щелочную реакцию (рН > 7).
б) Карбонат натрия Na2C03 - соль слабой многоосновной кислоты и сильного
основания. В этом случае анионы соли CО32-, связывая водородные ионы воды, об
разуют анионы кислой соли НС03-, а не молекулы Н2С03, так как ионы НС03 Дис
социируют гораздо труднее, чем молекулы Н2СОз- В обычных условиях гидролиз
идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение
гидролиза
СО32- + Н20 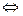 HCO3- + OH-
HCO3- + OH-
или в молекулярной форме
Na2C03 + H20 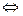 NaHC03 + NaOH
NaHC03 + NaOH
В растворе появляется избыток ионов ОН-, поэтому раствор Na2C03 имеет щелочную реакцию (рН > 7).
в) Сульфат цинка ZnS04 — соль слабого многокислотного основания Zn(OH)2
и сильной кислоты Н2S04. В этом случае катионы Zn2+связывают гидроксильные
ионы воды, образуя катионы основной соли ZnOH+. Образование молекул Zn(OH)2
не происходит, так как ионы ZnOH+ диссоциируют гораздо труднее, чем молекулы
Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется
по катиону. Ионно-молекулярное уравнение гидролиза
Zn2+ + Н20 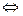 ZnOH+ + Н+
ZnOH+ + Н+
или в молекулярной форме
2ZnS04 + 2Н20 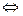 (ZnOH)2S04 + H2S04
(ZnOH)2S04 + H2S04
В растворе появляется избыток ионов водорода, поэтому раствор ZnS04 имеет кислую реакцию (рН < 7).
Пример 2. Какие продукты образуются при смешивании растворов А1(NO3)3 и К2С03? Составьте ионно-молекулярное и молекулярное уравнения реакции.
Решение. Соль AI(N03)3 гидролизуется по катиону, а К2СО3 - по аниону:
AI3+ + Н20 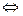 АlOН2+ + Н+
АlOН2+ + Н+
CO32- + H2O 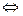 HCO3- + OH-
HCO3- + OH-
Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление
гидролиза каждой из них, ибо ионы Н+ и ОН- образуют молекулу слабого электролита
Н20. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых
солей идет до конца с образованием А1(ОН)3 и С02 (Н2С03). Ионно-молекулярное уравнение
2AI3+ + ЗС032- + ЗН20 = 2Аl(ОН)3 + ЗС02
молекулярное уравнение:
2AI(N03)3 + ЗК2С03 + ЗН20 =2А1(ОН)3 + 3C02 + 6KN03
Контрольные вопросы
201. Составьте ионно-молекулярное и молекулярное уравнения совместного
гидролиза, происходящего при смешивании растворов K2S и СгС13. Каждая из взятых солей
гидролизуется необратимо да конца с образованием соответствующих основания и кислоты.
202. К раствору FeCl3 добавили следующие вещества: в) НCl; б) КОН; в) ZnCl2; г) Na2C03. В каких случаях гидролиз хлорида железа (III) усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
203. Какие из солей Al2(S04)3. K2S, Pb(N03)2, KCl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7<) имеют растворы этих солей?
204. При смешивании растворов FeCl3 и Na2CO3 каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
205. К раствору Na2C03 добавили следующие вещества: а) НCl; б) NaOH; в) Cu(N03)2. г) K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
206. Какое значение рН (> 7 <) имеют растворы солей Na2S, AlCl3, NiS04? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
207. Составьте ионно-молекулярные и молекулярные уравнения гидролиза
солей Pb(N03)2,Na2C03. Fe2(S04)3. Какое значение рН (> 7 <) имеют растворы этих солей?
208. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей СН3СООК. ZnS04, Al(N03)3. Какое значение рН (> 7 <) имеют растворы этих солей?
209. Какое значение рН (> 7 <) имеют растворы солей Na3P04, K2S, CuS04? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
210. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей СuCl2, СsСО3, Сr(NO3)3. Какое значение рН (> 7 <) имеют растворы этих солей?
211. Какие из солей RbCl, Cr2(S04)3, Ni(N03)2, Na2S03 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7<) имеют растворы этих солей?
212. К раствору Al2(S04)3 добавили следующие вещества: a) H2S04; б) КОН в) Na2S03; г) ZnS04. В каких случаях гидролиз сульфата алюминия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
213. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: Nа2СО3 или Na2S03; FeCl3 или FeCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей
214. При смешивании растворов AI2(S04)3 и Na2C03 каждая из взятых солей
гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Составьте ионно-молекулярное и молекулярное уравнение происходящего совместного гидролиза.
215. Какие из солей NaBr, Na2S, K2C03, CoCl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующихсолей. Какое значение рН (> 7 <) имеют растворы этих солей?
216. Какая из двух солей при равных условиях в большей степени подвергается
гидролизу: NaCN или NaClO; MgCl2 или ZnCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
217. Составьте ионно-молекулярное и молекулярное уравнения гидролиза соли, раствор которой имеет: а) щелочную реакцию; б) кислую реакцию.
218. Какое значение рН (> 7 <)имеют растворы следующих солей: К3РО4, Pb(N03)2, Na2S? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
219. Какие из солей К2СО3, FeCl3, K2S04, ZnCl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7 <) имеют растворы этих солей?
220. При смешивании растворов AI2(S04)3 и Na2S каждая из взятых солей
гидролизуется необратимо до конца с образованием соответствующих основания икислоты. Выразите этот совместный гидролиз ионно-молекулярным и молекулярными уравнениями.
КОНТРОЛЬНОЕ ЗАДАНИЕ 2
Окислительно-восстановительные реакции
Окислительно-восстановительными называются реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ.
Под степенью окисления (п) понимают тот условный заряд атома, который вычисляется
исходя из предположения, что молекула состоит только из ионов. Иными словами: степень окисления — это тот условный заряд, который приобрел бы атом элемента, если предположить, что он принял или отдал то или иное число электронов. Окисление - восстановление — это единый, взаимосвязанный процесс. Окисление приводит к повышению степени окисления восстановителя, а восстановление — к ее понижению у окислителя.
Повышение или понижение степени окисления атомов отражается в электронных уравнениях; окислитель принимает электроны, а восстановитель их отдает. При этом не имеет значения, переходят ли электроны от одного атома к другому полностью и образуются ионные связи или электроны только оттягиваются к более электроотрицательному атому и возникает полярная связь. О способности того или иного вещества проявлять окислительные, восстановительные или двойственные (как окислительные, так и восстановительные) свойства можно судить по степени окисления атомов окислителя и восстановителя.
Атом того или иного элемента в своей высшей степени "окисления не может ее повысить (отдать электроны) и проявляет только окислительные свойстве, а в своей низшей степени окисления не может ее понизить (принять электроны) и проявляет только восстановительные свойстве. Атом же элемента, имеющий промежуточную степень окисления, может проявлять как окислительные, так и восстановительные свойства.
Например:
N 5+ (HNO3) S 6+ (H2SO4) 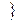 проявляют только окислительные свойства
проявляют только окислительные свойства
N 4+ (NO2) S4+ (SO2)
N 3+ (HNO2)
N 2+ (NO) S 2+ (SO) Проявляют окислительные и восстановительные свойства
N 1+ (N2O)
N 0 (N2) S 0 (S2; S3)
N –1 (NH2OH) S –1 (H2S2)
N 2 - (N2H4)
N 3 - (NH3) S 2 - (H2S) 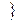 проявляют только восстановительные свойства
проявляют только восстановительные свойства
При окислительно-восстановительных реакциях валентность атомов может и не меняться. Например, в окислительно-восстановительной реакции Н20 + Cl02 = 2H+Cl- валентность атомов водорода и хлора до и после реакции равна единице. Изменилась их степень окисления. Валентность определяет число связей, образованных данным атомом, и поэтому знака не имеет. Степень же окисления имеет знак плюс или минус.
Пример 1. Исходя из степени окисления (n) азота, серы и марганца в соединениях NH3, HN02, HNO3, H2S, H2S03, H2S04, Mn02, KMn04 определить какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
Решение. Степень окисления п (N) в указанных соединениях соответственно равна: —3 (низшая), + 3 (промежуточная), +5 (высшая); n (S) соответственно равна: -2 (низшая), +4 (промежуточная), +6 (высшая); n (Мп) соответственно равна: +4 (промежуточная), +7 (высшая). Отсюда: NH3, H2S — только восстановители; HNO3, H2S04. KMn04 — только окислители; HN02, H2S03, Mn02 — окислители и восстановители.
Пример 2. Могут ли происходить окислительно-восстановительные реакции между следующими веществами: a) H2S и HI; б) H2S и H2S03; в) H2S03 и НClO4?
Решение: а) Степень окисления в H2S n (S) = -2; в HI n (I) = -- 1. Так как и сера, и иод находятся в своей низшей степени окисления, то оба взятые вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут; 6) в H2S n (S) = —2 (низшая); в H2S03 n (S) = +4 (промежуточная). Следовательно, взаимодействия этих веществ возможно, причем H2S03 является окислителем; в) в H2S03 n (S) = +4 (промежуточная); в НClO4 л (Сl) = +7 (высшая). Взятые вещества могут взаимодействовать. H2S03 в этом случае будет проявлять восстановительные свойства.
Пример 3. Составьте уравнения окислительно-восстановительной реакции, идущей по схеме
+7 +3 +2 +5
КМn04 + Н3РО3 + H2SO4  MnS04 + H3P04 + K2S04 + Н20
MnS04 + H3P04 + K2S04 + Н20
Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют свою степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях
Восстановитель 5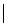 Р3+ -- 2е = Р5+ процесс окисления
Р3+ -- 2е = Р5+ процесс окисления
окислитель 2| Мn7+ + 5е = Мn2+ процесс восстановления
Общее число электронов, отданных, восстановителем, должно быть равно числу электронов, которое присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором. Уравнение реакции будет иметь вид
2КМn04 + 5Н3Р03 + 3H2S04 = 2MnS04 + 5H3P04 + K2S04 + 3H20
Пример 4. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней.
Решение. Цинк, как любой металл, проявляет только восстановительные свойства. В концентрированной серной кислоте окислительную функцию несет сера (+6). Максимальное восстановление серы означает, что она приобретает минимальную степень окисления. Минимальная степень окисления серы как р-элемеита VIA группы равна —2. Цинк как металл IIВ группы имеет постоянную степень окисления +2. Отражаем сказанное в электронных уравнениях:
восстановитель 4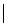 Zn0 — 2e = Zn2+ процесс окисления
Zn0 — 2e = Zn2+ процесс окисления
окислитель 1 S6+ + 8e = S2- процесс восстановления
S6+ + 8e = S2- процесс восстановления
Составляем уравнение реакции:
4Zn + 5H2S04 = 4ZnS04 + H2S + 4H20
Перед'H2S04 стоит коэффициент 5, а не 1, ибо четыре молекулы H2S04 идут на связывание четырех ионов Zn 2+.
Контрольные вопросы
221. Исходя из степени окисления хлора в соединениях НCl, НClO3, НCl4, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании
электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
KBr + KBrO3 + H2SO4  Br2 + K2SO4 + H2O
Br2 + K2SO4 + H2O
222. Реакции выражаются схемами:
Р + НIO3 + Н20  H3РО4 + HI
H3РО4 + HI
H2S + Cl2 + Н20  H2S04 + HCl
H2S04 + HCl
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое — восстановителем; какое вещество окисляется, какое — восстанавливается.
223. Составьте электронные уравнения и укажите, какой процесс — окисление
или восстановление - происходит при следующих превращениях:
As3- As5+; N3+
As5+; N3+ N3-; S-2
N3-; S-2  S°
S°
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
Na2SO3 + KMnO4 + H2O  Na2SO4 + MnO2 + KOH
Na2SO4 + MnO2 + KOH
224. Исходя из степени окисления фосфора в соединениях РН3, Н3РО4, Н3РО3, определите какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
PbS + HNO3  S + Pb(NO3)2 + NO + H2O
S + Pb(NO3)2 + NO + H2O
225. См. условие задачи 222.
P + HNO3 + H2O  H3PO4 + NO
H3PO4 + NO
KMnO4 + Na2SO3 + KOH  K2MnO4 + Na2SO4 + H2O
K2MnO4 + Na2SO4 + H2O
226. Составьте электронные уравнения и укажите, какой процесс – окисление или восстановление – происходит при следующих превращениях:
Mn6+  Mn2+; Cl6+
Mn2+; Cl6+  Cl-; N3-
Cl-; N3-  N5+.
N5+.
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
Cu2O + HNO3  Cu(NO3)2 + NO + H2O
Cu(NO3)2 + NO + H2O
227. См. условие задачи 222.
HNO3 + Ca  NH4NO3 + Ca(NO3)2 + H2O
NH4NO3 + Ca(NO3)2 + H2O
K2S + KMnO4 + H2SO4  S + K2SO4 + MnSO4 + H2O.
S + K2SO4 + MnSO4 + H2O.
228. Исходя из степени окисления хрома, йода и серы в соединениях K2Cr2O7, KI, H2SO3, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
NaCrO2 + PbO2 + NaOH  Na2CrO4 + Na2PbO2 + H2O
Na2CrO4 + Na2PbO2 + H2O
229. См. условие задачи 222.
H2S + Cl2 + H2O  H2SO4 + HCl
H2SO4 + HCl
K2Cr2O7 + H2S + H2SO4  S + Cr2(SO4)3 + K2SO4 + H2O
S + Cr2(SO4)3 + K2SO4 + H2O
230. См. условие задачи 222.
KClO3 + Na2SO3  KCl + Na2SO4
KCl + Na2SO4
KMnO4 + HBr  KBr + MnBr2 + H2O
KBr + MnBr2 + H2O
231. См. условие задачи 222.
Р + HClO3 + H20  H3PO4 + HCl
H3PO4 + HCl
Н3АsО3 + КМn04 + H2S04  Н3Аs04 + MnS04 + K2S04 + Н20
Н3Аs04 + MnS04 + K2S04 + Н20
232. См. условие задачи 222.
NaCrO2 + Br2 + NaOH  Na2Cr04 + NaBr + H20
Na2Cr04 + NaBr + H20
FeS + HN03  Fe(N03)2 + S + NO + H20
Fe(N03)2 + S + NO + H20
233. См. условие задачи 222.
HN03 + Zn  N2O + Zn(N03)2 + H20
N2O + Zn(N03)2 + H20
FeS04 + KCl03 + H2S04  Fe2(S04)3 + KCl + H20
Fe2(S04)3 + KCl + H20
234. См. условие задачи 222.
K2Cr207 + HCl  Cl2+ CrCl3 + KCl + H20
Cl2+ CrCl3 + KCl + H20
Au + HN03 + HCl  AuCl3 + NO + H20
AuCl3 + NO + H20
235. Могут ли происходить окислительно-восстановительные реакции между
веществами: a) NH3 и КМn04; б) HN02 и HI; в) HCl и H2Se? Почему? На основании
электронных уравнений расставьте коэффициенты в уравнении реакции, идущей
по схеме
КМn04 + KN02 + H2S04  MnS04 + KN03 + K2S04 + Н20
MnS04 + KN03 + K2S04 + Н20
236. См. условие задачи 222.
HCl + СrО3  Cl2 + CrCl3 + H20
Cl2 + CrCl3 + H20
Cd + KMn04 + H2SO4  CdS04 + MnS04 + K2S04 + H20
CdS04 + MnS04 + K2S04 + H20
237. См. условие задачи 222.
Cr203 + KClO3 + KOH  K2Cr04 + KC1 + H20
K2Cr04 + KC1 + H20
MnSO4 + PbO2 + HNO3  HMn04 + Pb(N03)2 + PbSO4 + H2O
HMn04 + Pb(N03)2 + PbSO4 + H2O
238. См. условие задачи 222.
H2SO3 + HClO3  H2SO4 + HCl
H2SO4 + HCl
FeS04 + K2Cr207 + H2S04  Fe2(S04) 3 + Cr2(S04)3 + K2S04 + H20
Fe2(S04) 3 + Cr2(S04)3 + K2S04 + H20
239. См. условие задачи 222.
I2 + Cl2 + H20  HI03 + HCl
HI03 + HCl
К2Cr2О7 + Н3РО3 + H2SO4 → Cr2(SO4)3 + Н3РО4 + K2SO4 + H2O
240. Могут ли происходить окислительно-восстановительные реакции между веществами: а) РН3 и НВr; 6) К2Сг2О7 и Н3РО3; в) HNO3 и H2S? Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
АsН3 + HNO3 → H3AsO4 + NO2 + Н2О
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 829; Нарушение авторских прав?; Мы поможем в написании вашей работы!