
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ж: CaCI2, N2O5, AI2O3, Na2S. 1 страница
|
|
|
|
Учебное пособие
Железняк Юрий Дмитриевич, Минбулатов Вагаб Минбулатович
Теория и методика обучения предмету «Физическая культура»
Редактор Л. В. До цен ко
Ответственный редактор С. И. Фрольцова
Технический редактор Е. Ф. Коржуева
Компьютерная верстка: Е. Ю. Матвеева
Корректоры О. Н. Тетерина, Е. В. Кудряшова
Диапозитивы предоставлены издательством.
Изд. № A-920-I. Подписано в печать 26.01.2004. Формат 60x90/16. Гарнитура «Тайме». Печать офсетная. Бумага тип. № 2. Усл. печ. л. 17,0. Тираж 7000 экз. Заказ №12921.
Лицензия ИД № 02025 от 13.06.2000. Издательский центр «Академия». Санитарно-эпидемиологическое заключение № 77.99.02.953.Д.003903.06.03 от 05.06.2003. 117342, Москва, ул. Бутлерова, 17-Б, к. 223. Тел./факс: (095) 334-8337, 330-1092.
Отпечатано на Саратовском полиграфическом комбинате. 410004, г. Саратов, ул. Чернышевского, 59.
- Мыс (II) оксидіндегі элементтердің массалық үлестерін есептеңдер.
Бер: CuO Шешуі: Ar (Cu) = 64
т/к: ω (Cu)% -? Ar (O) = 16
ω (O)% -? Mr (CuO) = 64+16=80
ω (Cu)%= 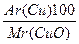 =
= 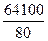 = 80%
= 80%
ω (O)% = 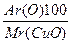 =
= 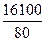 = 20
= 20
2 нұсқа
- Мына қосылыстардағы элементтердің валенттілігін анықтаңдар.
VI II III II I I III I IV I
SO3, P2O3, NaCI, Fe(OH)3, CH4
- 0,8 кг мыс (II) оксидінде неше моль бар?
Бер: m(CuO) = 0,8 г. M(CuO) = 80 г/моль = 0,080 кг/ моль
т/к: υ (CuO) -?
υ= 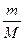 =
= 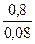 = 10 моль (CuO)
= 10 моль (CuO)
3. Төмендегі химиялық реакция теңдеулерін теңестіріп, типін анықтаңдар.
а) 2Mg + O2 = 2MgO қосылу реакциясы
ә) AI + 2HCI = AICI2 + H2 орынбасу реакциясы
б) 2KMnO4 = K2MnO4 + MnO2 + O2 айырылу реакциясы
4. Төмендегі қосылыстардың формуласын құрыңдар:
а) калий мен хлор;
ә) азот (VI) пен оттек;
б) алюминий мен оттек;
в) күкірт (II) пен оттек;
Ж: КCI, NO3, AIO, SO.
5. Кальций оксидіндегі элементтердің массалық үлесін есептеңдер.
Бер: CaO Шешуі: Ar(Ca) = 40
Ar(O) = 16
т/к: ω (Ca)%-? Mr (CaO) = 56
(Ca)%-? Mr (CaO) = 56
ω (O)% -?
ω (Ca)%=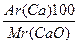 =
= 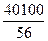 =71,5%
=71,5%
ω (O)% =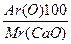 =
= 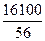 =28,5%
=28,5%
1-нұсқа:
1. Мына қосылыстардағы элементтердің валенттігін анықтаңдар:
NH3, P2O5, CrO3, H2S,,SO3;
2. Мыс (І) және мыс(ІІ)оксидтерінің құрамындағы мыстың массалық үлестерін пайызбен есептеңдер.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) AgCI = Ag +CI2; ә) K + O2 = K2O; б) Fe + HCI = FeCI2 + H2;
4. 7H, 3CaO, 5H2 белгілері нені көрсетеді?
5. Массасы 6г магний жанғанда қанша грамм магний оксиді түзілетінін есептеңдер.
2-нұсқа:
1. Төмендегі қосылыстардың: а) кальций мен хлор; ә) азот(V) пен,оттек; б) алюминий мен,оттек; в) натрий мен күкірт (ІІ) формуласын құрыңдар.
2. Мына әктастың CaCO3 құрамындағы әр химиялық элементтің,массалық үлесін табың дар.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін,анықтаңдар:
а) Fe(OH)3=Fe2O3 + H2O; ә) Na + CI2 = NaCI; б) Na+H2O = NaOH + H2;
4. Бір атом темір мен үш атом хлордан, екі атом алюминий мен үшатом оттектен, бір,атом фосфор мен бес атом хлордан тұратын күрделі заттардың молекулалық формуласын құрыңдар.
5. Массасы 6,2г фосфор жану үшін қанша моль оттек газы О2 қажет болатынын есептеңдер.
3-нұсқа:
1. Валенттіктері 1-ден 7-ге дейін өсу ретімен орналасқан мына: Na,Mg, AI, Si, P, S, CI,,элементтердің оттекпен қосылысының формуласын құрыңдар.
2. Ас содасының құрамы 27,38% Na, 1,19%H, 14,29%C және 57,14% оттектен тұрады. Осы заттың молекулалық формуласын табыңдар.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар: а) Mg + O2 = MgO; б) Ai + HCI = AICI3 + H2;
4. Мына атомдар санын мольмен өрнектеңдер: а) 12,24•1023 атом кальций; ә)3,01•1023 ат,ом оттек; б) 6,02 •1023 атом көміртек;
5. Массасы 4,4г азот (І) оксиді бар. Осы заттың: а) мөлшерін; ә) молекула санын есептеңдер.
Үйге тапсырма беру: Қайталау.
Күні
Сабақтың тақырыбы: « Бастапқы химиялық ұғымдар» тақырыбын қорытындылау.
Сабақтың мақсаты: Білімділік: Осы тарау бойынша алған білімдерін тереңдету. Дамытушылық: Химиялық формула, теңдеу құру дағдыларын, есеп шығару химиялық тәжірибе жасау біліктерін дамыту. Осының бәрін атом – молекулалық ілім тұрғысынан дәлелдеу.
Тәрбиелік мақсаты: ғылымға, пәнге қызығуға тәрбиелеу.
Құрал– жабдықтар: Химиялық және физикалық құбылыстарға тәжірибелер, керекті химиялық ыдыстар және реактивтер.Сабақтың түрі: дәстүрлі емес. Сабақтың әдіс-тәсілдері:топпен жұмыс, деңгейлік тапсырмалар.
Сабақ барысы: Ұйымдастыру кезеңі. Оқушыларға ойын сабағының жоспары хабарланады. Тақтаға жазылады.
Сабақ девизі: «Пысықтау оқу - анасы».1.Бақытты сәт – ойыны.
2. Деңгейлік есептер 3. Қызықты тәжірибелер.
4. Полиглот – ыдысы. 5.Тестілермен жұмыс.
Оқушыларды 2 ұғымдық топқа бөлетін. Топ басшысы осы ұжымның ұпайын есептеп отырады. Оған кесте алдын ала беріледі. 1-кезең. Сұрақтар (Дұрыс жауап берген оқушыға жетон беріледі)
1 ұжымдық топқа қойылатын сұрақтар.
1.Физикалық денелерді құрайтын нәрсе? (Зат) 2. Құрамына кіретін заттардың бөлшектері микрос коп арқылы да көрінбейтін қоспа қалай аталады? (Біртекті) 3. Шынының балқуы қай құбылысқа жата ды? (Физ.) 4. Бөлінбейтін ең кішкентай бөлшектер. (Атомдар) 5. Атомдарының әр түрінен түзілген заттар...(күрделі) 6.Оттектің салыстырмалы атомдық массасы.(16) 7.Мыстың латынша атауы. (купрум) 8. Плюмбум – (қорғасын) 9. О әрпімен белгіленетін элемент.(оттегі) 10.Таңбалар және формулалар арқылы шартты түрде жазылған реакциялар (Химиялық теңдеулер)
2-ұжымдық топқа қойылатын сұрақтар.
1. Заттардың агрегаттық күйлері.(Қатты,сұйық,газ)
2. Құрамына кіретін заттардң бөлшектерін жай көзбен көруге болатын қоспалар қалай аталады?(Әр текті)
3. Темірдің тот басуы қандай құбылысқа жатады?(хим.)
4. Атом-молекулалық ілімді жасаған орыс ғалым.(Ломоносов)
5. «Эн» таңбасы (Азот)
6. Кремнийдің латынша аты?(силициум)
7. Сутегінің таңбасы.(Н)
8. Химиялық теңдеуді теңестіру үшін қойылатын сандар?(Коэфф-р)
9. Феррум...(темір)
10. Азоттың салыстырмалы атомдық массасы.(14)
2-кезең. Деңгейлік есептер шығару. Тапсырма жауаптары тақтаға жазылады. 1-2 ұжымдық топтарға таратылып беріледі.
3-кезең. Демонстрациялық тәжірибелер: Оқушылар өздері орындайды.
а)Тұз бен құмның қоспасы берілген тұз бен құмды бөліп алу керек.Бұл қандай қоспа? Қоспалардың тағы қандай түрлерін білесің. (1 ұжым тобына)
ә)Темір мен күкірт қоспасы берілген. Бұл қандай қоспа? Күрделі зат пен қоспаның айырмашылығы неде?
4-кезең. Үй тапсырманы тексеру үшін «Полиглот» ойыны ойналады. Сұрақтарда кездесетін элементтер дің атын қазақ, орыс, латын тілінде айту керек. Дұрыс жауапқа 10 ұпай, жартылай 5 ұпай. Қай ұжым дық топ жылдам, білімділігін көрстеді.
1.Сұйық металл (Нg, сынап,ртуть-гидраргирум)
2. Ауаның негізгі құрам бөлігі? (О-оттек-кислород-оксигениум)
3.Қай элементтің жетіспеуі тіс ауруына ұшыратады? (Ғ-фтор-фтор-фторум)
4. Ой және өмір элементі. (Р-фосфор-фосфор-фосфорус)
5. Қай элемент бактериялырды өлтіріп, денсаулығымызды қорғайды?(ll, хлор-хлор-хлорум)
6. Ақыл арымас, алтын шірімес. (Аи-алтын-золото-аурум).
7. Темірді қызған кезінде соқ (Ғе-темір- феррум-железо).
5-кезең.Тестілермен жұмыс. Екі ұжымдық топқа тест кітапшасы бойынша деңгейлік тапсырма беріледі.Екі ұжымдық топ бір-бірін тексереді. 9 жұмыс. (тест) 1-2-3 деңгейде орындау Хим. фор-лар бой. есептеулер. Сабақ соңында топ басшыларыұпай санын санап, оқушыларды бағалайды.Қай топтың білімі басым болғанын анықтау. Сабақты қорытындылау.
| Оқушылардың аты жөні | 1 кезең | 2 кезең | 3 кезең | 4 кезең | 5 кезең | Қорытынды ұпай саны |
| 1. 2. |
Үйге тапсырма: Қайталау.
8-сынып Бақылау жұмысы
1-нұсқа:
1. Мына қосылыстардағы элементтердің валенттігін анықтаңдар: NH3, P2O5, CrO3, H2S,,SO3;
2. Мына фосфор қышқылының (H3PO4) құрамындағы әр химиялық элементтің массалық үлесін
есептеп шығар.
3. Төмендегі берілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) AgCI = Ag +CI2; ә) K + O2 = K2O; б) Fe + HCI = FeCI2 + H2;
4. Массасы 6 грамм магний жанғанда түзілген магний оксидінің (MgO) массасын және зат мөлшерін
есептеп шығар.
2-нұсқа:
1. Төмендегі қосылыстардың формуласын құрыңдар: а) кальций мен хлор(І); ә) азот (V) пен,оттек;
б) алюминий мен,оттек;, в) натрий мен,күкірт (ІІ).
2. Мына әктастың (CaCO3) құрамындағы әр химиялық элементтің,массалық үлесін есептеп шығар.
3. Төменде берілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) Fe(OH)3=Fe2O3 + H2O; ә) Na + CI2 = NaCI; б) Na+H2O = NaOH + H2;
4. Массасы 6,2 грамм фосфор жанғанда түзілген фосфор (V) оксидінің (P2O5) массасын және зат
мөлшерін есептеп шығар.
3-нұсқа:
1. Валенттіктері 1-ден 7-ге дейін өсу ретімен орналасқан мына: Na,,Mg, AI, Si, P, S, CI,,элементтердің,,,,,,,,оттекпен,қосылысының формуласын құрыңдар.
2. Ас содасының құрамы 27,38% Na, 1,19%H, 14,29%C және 57,14% оттектен тұрады. Осы заттың,,,,,,,,молекулалық формуласын табыңдар.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) Mg + O2 = MgO; б) Ai + HCI = AICI3 + H2;
4. Мына атомдар санын мольмен өрнектеңдер: а) 12,24•1023 атом,кальций; ә)3,01•1023 атом оттек;
,,,,,,,,б) 6,02 •1023 атом көміртек;
5. Массасы 4,4г азот (І) оксиді бар. Осы заттың: а) мөлшерін; ә) молекула санын есептеңдер.
8-сынып Бақылау жұмысы
1-нұсқа:
1. Мына қосылыстардағы элементтердің валенттігін анықтаңдар: NH3, P2O5, CrO3, H2S,,SO3;
2. Мыс (І) және мыс(ІІ)оксидтерінің құрамындағы мыстың массалық үлестерін пайызбен есептеңдер.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) AgCI = Ag +CI2; ә) K + O2 = K2O; б) Fe + HCI = FeCI2 + H2;
4. 7H, 3CaO, 5H2 белгілері нені көрсетеді?
5. Массасы 6г магний жанғанда қанша грамм магний оксиді түзілетінін есептеңдер.
2-нұсқа:
1. Төмендегі қосылыстардың: а) кальций мен хлор; ә) азот(V) пен,оттек; б) алюминий мен,оттек;
,,,,,,, в) натрий мен,,,,,,,күкірт (ІІ) формуласын құрыңдар.
2. Мына әктастың CaCO3 құрамындағы әр химиялық элементтің,массалық үлесін табыңдар.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) Fe(OH)3=Fe2O3 + H2O; ә) Na + CI2 = NaCI; б) Na+H2O = NaOH + H2;
4. Бір атом темір мен үш атом хлордан, екі атом алюминий мен үш,атом оттектен, бір,атом,,,,,,,,фосфор мен бес,атом хлордан тұратын күрделі заттардың молекулалық формуласын құрыңдар.
5. Массасы 6,2г фосфор жану үшін қанша моль оттек газы О2 қажет болатынын есептеңдер.
3-нұсқа:
1. Валенттіктері 1-ден 7-ге дейін өсу ретімен орналасқан мына: Na,,Mg, AI, Si, P, S, CI,,элементтердің,,,,,,,,оттекпен,қосылысының формуласын құрыңдар.
2. Ас содасының құрамы 27,38% Na, 1,19%H, 14,29%C және 57,14% оттектен тұрады. Осы заттың,,,,,,,,молекулалық формуласын табыңдар.
3. Төмендерілген химиялық реакция теңдеулерін теңестіріп, типтерін анықтаңдар:
а) Mg + O2 = MgO; б) Ai + HCI = AICI3 + H2;
4. Мына атомдар санын мольмен өрнектеңдер: а) 12,24•1023 атом,кальций; ә)3,01•1023 атом оттек;
,,,,,,,,б) 6,02 •1023 атом көміртек;
5. Массасы 4,4г азот (І) оксиді бар. Осы заттың: а) мөлшерін; ә) молекула санын есептеңдер.
Сабақты бекіту мақсатында шығарылатын есептер:
1) 8г мыс(ІІ) оксидін алу үшін қанша грамм мыс реакцияға түседі?
2) Нәтижесінде 4 моль сутек алу үшін қанша грам суды айыруға болады?
3) Массасы 6,5г цинк оттекпен әрекеттессе цинк оксидінің қанша зат мөлшерін алуға болады?
4) 1 моль алюминий күкіртпен реакцияға түсу үшін қанша күкірт қажет және түзілген алюминий сульфидінің массасын есептеңдер?
5) Оттегінде 54г алюминий жанған кезде, алынған алюминий оксидінің массасы қандай?
6) Массасы 360г алюминий сульфидін алу үшін, оған жұмсалған алюминий мен күкірттің массасын есептеп шығар.
7) 8г мыс(ІІ) оксидінен мысты жеке бөліп алу үшін, қанша грамм сутегі жұмсалады?
8) 8г сутегі жанғанда түзілетін судың массасы және зат мөлшері қанша?
9) Реакцияға 16г оттегі түскенде судың қандай зат мөлшері шығады?
10) Реакциядан 9г су түзіледі. Реакцияға түскен оттегінің массасын және зат мөлшерін табыңдар.
Сабақты бекіту мақсатында шығарылатын есептер:
1) 8г мыс(ІІ) оксидін алу үшін қанша грамм мыс реакцияға түседі?
2) Нәтижесінде 4 моль сутек алу үшін қанша грам суды айыруға болады?
3) Массасы 6,5г цинк оттекпен әрекеттессе цинк оксидінің қанша зат мөлшерін алуға болады?
4) 1 моль алюминий күкіртпен реакцияға түсу үшін қанша күкірт қажет және түзілген алюминий сульфидінің массасын есептеңдер?
5) Оттегінде 54г алюминий жанған кезде, алынған алюминий оксидінің массасы қандай?
6) Массасы 360г алюминий сульфидін алу үшін, оған жұмсалған алюминий мен күкірттің массасын есептеп шығар.
7) 8г мыс(ІІ) оксидінен мысты жеке бөліп алу үшін, қанша грамм сутегі жұмсалады?
8) 8г сутегі жанғанда түзілетін судың массасы және зат мөлшері қанша?
9) Реакцияға 16г оттегі түскенде судың қандай зат мөлшері шығады?
10) Реакциядан 9г су түзіледі. Реакцияға түскен оттегінің массасын және зат мөлшерін табыңдар.
Сабақты бекіту мақсатында шығарылатын есептер:
1) 8г мыс(ІІ) оксидін алу үшін қанша грамм мыс реакцияға түседі?
2) Нәтижесінде 4 моль сутек алу үшін қанша грам суды айыруға болады?
3) Массасы 6,5г цинк оттекпен әрекеттессе цинк оксидінің қанша зат мөлшерін алуға болады?
4) 1 моль алюминий күкіртпен реакцияға түсу үшін қанша күкірт қажет және түзілген алюминий сульфидінің массасын есептеңдер?
5) Оттегінде 54г алюминий жанған кезде, алынған алюминий оксидінің массасы қандай?
6) Массасы 360г алюминий сульфидін алу үшін, оған жұмсалған алюминий мен күкірттің массасын есептеп шығар.
7) 8г мыс(ІІ) оксидінен мысты жеке бөліп алу үшін, қанша грамм сутегі жұмсалады?
8) 8г сутегі жанғанда түзілетін судың массасы және зат мөлшері қанша?
9) Реакцияға 16г оттегі түскенде судың қандай зат мөлшері шығады?
10) Реакциядан 9г су түзіледі. Реакцияға түскен оттегінің массасын және зат мөлшерін табыңдар.
Күні
II тарау. ОТТЕК. ОКСИДТЕР. ЖАНУ.
№1 сабақтың тақырыбы:. Оттек. Оттектің табиғатта кездесуі.
Сабақтың мақсаты: Білімділік: Химиялық элементпен және жай затпен таныстыруды жоспарлау.Дамытушылық: Өз еріктерімен ізденіп ойларын дамыту. Тәрбиелік: жеке жұмыс жасауға тәрбиелеу.
Құрал-жабдықтар. “Элементтердің табиғатта таралуы”.
Тірек білім мен біліктер: Элемент, жай зат, химиялық элемент пен жай зат ұғымдары ның айырмашылығы. Физикалық және химиялық құбылыс.
Сабақтың түрі: аралас сабақ, іздену, өз еріктерімен жұмыс.
Сабақтың әдіс-тәсілдері: жаңа сабақты игеру, оқулықпен жұмыс
Сабақтың барысы: Өмірде маңызы бар кейбір заттармен таныстыру оттегімен басталады. Оттегіні оқып үйрену үшін оны әрі элемент, әрі жай зат ретінде қарастыру қажет. Химиялық элемент пен жай ұғымдарының арасында айырмашылық бар екені айтылады. Төмендегі берілген жоспарда бұл айырмашылық айқын көрінеді.
Химиялық элементке сипаттама беру жоспары:
1. Химиялық таңбасы.
2. Салыстырмалы атомдық массасы.
3. Табиғатта кездесуі.
Жай заттарға сипаттама беру жоспары:
1. Химиялық формуласы.
2.Салыстырмалы молекулалық массасы.
3.Физикалық қасиеті.
4.Химиялық қасиеті.
5.Қолданылуы.
6.Зертханада және өндірісте алу жолдары.
Осы келтірілген жоспарға сүйене отырып, оқушы өздігінен оттегіне сипаттама береді. Кейін де элементтерге, жай заттарға сипаттама бергенде осы жоспарды қолдануға болады.
Сабақты пысықтау мақсатында оқулықтан тапсырмалар беріледі.
Үйге тапсырма беру: § 20. 1-7 жаттығулар.
Күні
Ссабақтың тақырыбы: Оттегінің физикалық қасиеттері, зертханада және өндірісте алу.
Сабақтың мақсаты: Білімділік:Оқушыларды оттегінің қасиеттерімен таныстыру. Дамытушылық: зертханада алу әдістерін көрсету.Тәрбиелік: Жек жұмыс жасауға, қорытындылауға тәрбиелеу.
Құрал-жабдықтар: Цилиндрлер, шыны пластинка, заттарды жандыратын қасықша, сіріңке, шыра, кестелер: “Газды жинау”, Калий хлораты (Бертолле тұзы), сутегі асқын оксиді, калий перман- ганаты, күкірт қышқылы, оттегін алуға және жинауға арналған құралдар, шырпы, газометр, сіріңке, газ жанарғысы.Электрондық оқулық
Сабақтың түрі. Аралас сабақ.
Сабақтың әдіс-тәсілдері: жаңа сабақты игеру, сұрақ – жауап.
Тірек білім мен біліктер: Газдарды жинау әдістері, катализатор.
Сабақ барысында оттегінің қолданылуын, табиғатта таралуын қайталау мақсатында бірнеше сұрақтарға жауап алынады.
1.Қандай қасиеттеріне байланысты газ және сұйық күйінде қолданылады?
2Қандай қасиетіне сүйеніп оттегін суды және ауаны ығыстыру арқылы алады?
Жаңа сабақты көрнекі тәжірибелер көрсетуден бастау. Оттегін оңай ыдырайтын заттардан алуға болатыны айтылады. Оттегін алу тәжірибе арқылы көрсетіледі. Тәжірибе мына тәртіппен жүргізіледі:
2KMnO4 → K2MnO4 + MnO2 + O2↑
Оқушыларды тәжірибе жүргізген кезде дұрыс бақылауға, нәтижесін қорытындылауға үйрету керек. Осындай бақылау жүргізуді үйрету үшін газометрге оттегі толтырылады да, оқушыларға “Оттегінің қандай қасиетін бақыладыңдар?”-деген сұрақ қойылады. Одан әрі оттегін ыдыстағы ауаны ығыстыру арқылы жинауды және сынауықтағы суды ығыстыру арқылы жинауды көрсету.
Жиналған оттегінде шала жанған шырпыны апарғанда, оның жарық жалын шығарып жанатынын оқушыларға қөрсету арқылы «оттегі жануды қолдайтын газ» екенін түсіндіремін. Ауадағы оттегіне қарағанда, таза оттегінде заттар өте жақсы және тез жанатыны айтылады.
Оқушылар заттардың физикалық қасиетіне сипаттама беруді біледі.
а)сынауықтағы сутегі асқын оксидін катализатор(өршіткі) салып қыздыру;
ә) марганец (IY) оксидін сынауықта қыздыру;
б)қоспа дайындау H2O2+MnO2, оттегін алу, тәжірибе нәтижесі қорытын- дыланып, катализаторға анықтама беріледі. Катализаторды бөліп алып, массасы өзгермегенін көрсету керек. Бертолле тұзынан да оттегін алғанда өршіткі қолданылады.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 6675; Нарушение авторских прав?; Мы поможем в написании вашей работы!