
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 1. Вычислите изменение энтропии в реакции горения этана:
|
|
|
|
Вычислите изменение энтропии в реакции горения этана:
C2H4(Г) + 3O2(Г) = 2CO2(Г) + 2H2O(Г).
Решение.
Термодинамическая функция энтропия (S) характеризует возможные состояния вещества и их непрерывные изменения. Частицы вещества - атомы, молекулы, ионы и. т. д. совершают непрерывные колебательные и другие виды движения, переходя в каждый момент времени из одного микросостояния в другое. Чем больше таких изменений, тем больше беспорядок в системе, количественной характеристикой которого и служит энтропия.
Так, газообразное состояние более неупорядочено по сравнению с жидким, поэтому переход жидкости в газ (испарениe, кипение) сопровождается увеличением энтропии. Энтропия возрастает также в реакциях, идущих с увеличением объема, усложнением состава молекул, повышением температуры.
Чтобы можно было сравнивать энтропии различных веществ, пользуются стандартной энтропией S0. Величины стандартных энтропий приведены в термодинамических таблицах [1-4].
Энтропия, как и энтальпия, является функцией состояния, т. е. подчиняется закону Гесса и следствию из него:
DS0х.р. = 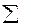 n S0продукт. -
n S0продукт. - 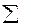 n S0исход. веществ.
n S0исход. веществ.
По условию задачи нужно вычислить DS0 реакции горения этана. Для этого из таблицы [1] выпишем энтропии образования веществ и подставим их в уравнение:
Вещество C2H4 (Г) O2 (Г) CO2 (Г) H2O (Г),
S0, Дж/моль ´ К 219,45 205,03 213,65 188,72,
DS0х.р. = [2S0(H2O) + 2S0(CO2)] - [S0(C2H4) + 3S0(O2)] =
= (2 ´ 188,72 + 2 ´ 213,65) - (219,45 + 3 ´ 205,03) = -29,80 Дж/моль´K.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1494; Нарушение авторских прав?; Мы поможем в написании вашей работы!