
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры составления условий задач и их решения. Разобрать процессы, протекающие у электродов при электролизе водных растворов: Na2SO4, Cd(NO3)2, KBr
|
|
|
|
Задача 472
Разобрать процессы, протекающие у электродов при электролизе водных растворов: Na2SO4, Cd(NO3)2, KBr, CuCl2; для каждого из них составить общее уравнение реакции.
Решение:
Вода может быть как окислителем, так и восстановителем, поэтому при электролизе водных растворов у электродов могут восстанавливаться и окислиться не ионы электролита, а вода. Это зависит от сравнительной величины окислительно-восстановительных потенциалов воды и ионов электролита.
1. Электролиз водного раствора Na2SO4.
Стандартный электродный потенциал системы

 В
В
значительно отрицательнее потенциала водородного электрода в нейтральной водной среде
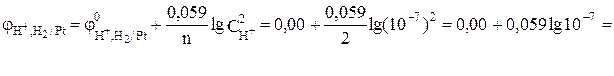
 В.
В.
Поэтому на катоде будет происходить электрохимическое восстановление воды, сопровождающееся выделением водорода:
2H2O +2e ® H2↑ + 2OH–,
а ионы Na+, приходящие к катоду, будут накапливаться в прилегающей к нему части раствора (катодное пространство).
На аноде будет происходить электрохимическое окисление воды, приводящее к выделению кислорода:
2H2O – 4e → O2 + 4H+; 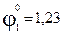 В,
В,
поскольку отвечающий этой системе стандартный электродный потенциал значительно ниже, чем стандартный электродный потенциал, характеризующий систему: 2SO42– – 2e = S2O82–, 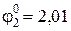 В.
В.
Ионы SO42–, движущиеся при электролизе к аноду, будут накапливаться в анодном пространстве.
Умножая уравнение катодного процесса на два и складывая его с уравнением анодного процесса, получаем суммарное уравнение процесса электролиза:
6H2O ↔ 2H2↑ + 4OH– + O2↑ + 4H+.
у катода у анода
Приняв во внимание, что одновременно происходит накопление ионов Na+ в катодном пространстве и ионов SO42– в анодном пространстве, суммарное уравнение процесса можно записать в следующей форме:
2Na2SO4 + 6H2O ↔ 2H2↑ + 4NaOH + O2↑ + 2H2SO4.
у катода у анода
Таким образом, одновременно с выделением водорода и кислорода образуется гидроксид натрия (в катодном пространстве) и серная кислота (в анодном пространстве).
В случае, когда растворы катодного и анодного пространств перемешиваются, образующиеся в результате электролиза щелочь и кислота нейтрализуются и дают вновь соль (Na2SO4):
4NaOH + 2H2SO4 = 2NaSO4 + 4 H2O.
В итоге электролиз сводится к электрохимическому разложению воды:
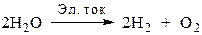 .
.
2. Электролиз водного раствора Cd(NO3)2.
Решение:
При электролизе водных растворов солей цинка, железа, кадмия и некоторых других металлов, стоящих в ряду напряжения, хотя и левее водорода, но близко к нему, на катоде выделяются эти металлы. Объясняется это тем, что процесс разрядки ионов Н+ осложняется адсорбцией атомов и молекул водорода на поверхности электродов. Для того чтобы десорбировать водород и получить его в газообразном состоянии, необходимо приложить избыточную э.д.с. Увеличение э.д.с. приводит к тому, что на катоде происходит выделение металла, стоящего в ряду напряжения левее водорода:
Cd2+ + 2e ↔ Cd,  В.
В.
Нитрат-ионы скапливаются вблизи анода, но окислению легче подвергается вода: 2H2O – 4e → O2 + 4H+, 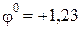 В.
В.
В целом процесс выражается уравнением
2Cd(NO3)2 + 2H2O ↔ 2Cd + O2↑ + 4HNO3.
у катода у анода
При электролезе солей, состоящих из ионов малоактивных металлов (стоящих в ряду напряжения после водорода) и кислородсодержащих анионов, также набдюдается выделение металла на катоде. На аноде выделяется кислород в результате окисления воды с изменением pH среды за счет вторичного процесса – образования кислоты.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 6215; Нарушение авторских прав?; Мы поможем в написании вашей работы!