
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры составления задач и их решения. Вычислить произведение растворимости фосфата серебра, если его растворимость равна 0,0065 г/л
|
|
|
|
Задача 833
Вычислить произведение растворимости фосфата серебра, если его растворимость равна 0,0065 г/л.
Решение:
Находим растворимость Ag3PO4. Молярная масса Ag3PO4 равна 418,6 г/моль. Растворимость:
S = 6,5·10-3 / 418,6 = 1,6·10-5 моль/л.
При диссоциации Ag3PO4 образуется три иона Ag+ и один ион РO43– :
АgзРO4 = 3 Ag+ + PO43–,
поэтому [PO43–] равна растворимости Ag3PO4 , а концентрация иона Ag+ в 3 раза больше, т.е.
[РO43–] = 1,6·10-5 моль/л; [Ag+]=3·1,6·10-5 =4,8 · 10 -5 моль/л.
Произведение растворимости Ag3PО4:
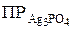 = [Ag+]3 · [ PO43–] = (4,8·10-5)3 · 1,6·10-5=1,77·10 - 18.
= [Ag+]3 · [ PO43–] = (4,8·10-5)3 · 1,6·10-5=1,77·10 - 18.
Задача 859
Произведение растворимости иодида свинца при 20 oC равно 8·10–9. Вычислить растворимость соли (в моль/л и в г/л) при указанной температуре.
Решение:
Обозначим искомую растворимость через S (моль/л). Тогда в насыщенном растворе PbI2 содержится S моль/л ионов Pb2+ и 2S моль/л ионов I–. Отсюда:
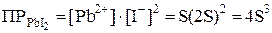 ;
;
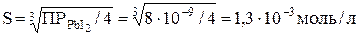 .
.
Поскольку мольная масса PbI2 равна 461 г/моль, то растворимость PbI2, выраженная в г/л, составит 1,3∙10–3∙461 = 0,6 г/л.
В задачах 833–847 вычислить произведение растворимости малорастворимых электролитов
| № задачи | Электролит | Растворимость электролита |
| 833. 834. 835. 836. 837. 838. 839. 840. 841. 842. 843. 844. 845. 846. 847. | Ag3РO4 Мg(ОН)2 АgСl ВаСО3 СаСO3 PbSO4 AgIO3 BaSO4 PbBr2 CaF2 PbCI2 AgBr MgCO3 PbBr2 PbI2 | 0,0065 г/л 0,012 г/л 0,0018 г/л 8,9·10-5 моль/л 1,3·10-4 моль/л 0,132 г в 3 л 0,176 г Ag+ в 3 л 2,3·10-3 г/л 2,7·10-2 моль/л 2·10-4 моль/л 11 г/л 1,1·10-4 г/л 2,67·10-3г/л 0,0427 г/л 1 г в 1470 мл воды |
В задачах 848-859 вычислить растворимость электролита по величине произведения растворимости (прил. табл.10)
| № задачи | Электролит | № задачи | Электролит | № задачи | Электролит |
| 848. 849. 850. 851. | ВаСгО4 Ag2SO3 AgSCN SrCrO4 | 852. 853. 854. 855. | CaC2O4 CaSO4 Ag2CrO4 Ag2CO3 | 856. 857. 858. 859. | Сu(ОН)2 СuS BaF2 PbI2 |
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 2884; Нарушение авторских прав?; Мы поможем в написании вашей работы!