
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительные свойства азотной кислоты
|
|
|
|
Окислительные свойства концентрированной серной кислоты
Концентрированная серная кислота является сильным окислителем. Функцию окислителя в концентрированной серной кислоте выполняют атомы серы со степенью окисления +6 (H2S+6O4). В концентрированной серной кислоте растворяются даже металлы с положительными значениями электродных потенциалов.
При взаимодействии металлов с концентрированной серной кислотой водород не выделяется.
В процессе восстановления сера со степенью окисления +6 может принимать различное число электронов:
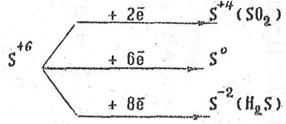
Образующиеся продукты восстановления серы зависят от активности восстановителя. Чем более сильным восстановителем (чем меньше его электродный потенциал) является металл, тем глубже он может восстановить концентрированную серную кислоту. Малоактивные металлы обычно восстанавливают серную кислота до диоксида серы.
Азотная кислота концентрированная и разбавленная относится к кислотам - окислителям. Обладая очень сильными окислительными свойствами, азотная кислота растворяет почти все металлы (за исключением золота, платины, тантала, родия, иридия).
Функцию окислителя в азотной кислоте выполняют атомы азота со степенью окисления +5. Изменение степени окисления азота в зависимости от числа принятых электронов можно представить схемой:
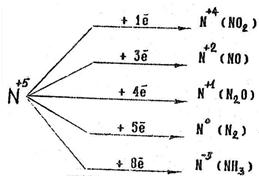
Чей меньше концентрация азотной кислоты и чем активнее восстановитель, тем глубже восстанавливается азот. Малоактивные металлы - металлы с положительными и не очень низкими отрицательными значениями стандартных электродных потенциалов - восстанавливают разбавленная азотную кислоту до NO.
Следует оговориться, что при взаимодействии металлов с азотной и концентрированной серной кислотами образуется, как правило, смесь продуктов восстановления, а в уравнении записывается только один, количество которого является наибольшим.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1763; Нарушение авторских прав?; Мы поможем в написании вашей работы!