
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второй механизм
|
|
|
|
Давление газа зависит от средней кинетической энергии молекул  , где n 0 – концентрация молекул. При увеличении кинетической энергии возрастает и давление, оказываемое газом на стенки сосуда. Но давление, по определению:
, где n 0 – концентрация молекул. При увеличении кинетической энергии возрастает и давление, оказываемое газом на стенки сосуда. Но давление, по определению: 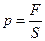 , откуда
, откуда 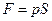 . Таким образом, при увеличении давления возрастает сила, с которой молекулы действуют на стенки сосуда, в котором находится газ. Если на стенки сосуда действует сила, то по второму закону Ньютона
. Таким образом, при увеличении давления возрастает сила, с которой молекулы действуют на стенки сосуда, в котором находится газ. Если на стенки сосуда действует сила, то по второму закону Ньютона 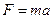 может возникнуть ускорение, т.е. движение стенок сосуда. При этом говорят, что газ совершает работу по расширению.
может возникнуть ускорение, т.е. движение стенок сосуда. При этом говорят, что газ совершает работу по расширению.
Эти два механизма объединяются законом сохранения энергии, который в термодинамике называется первым началом термодинамики:
 (9.7)
(9.7)
- количество теплоты, сообщаемое термодинамической системе, расходуется на увеличение внутренней энергии системы и совершение системой работы против внешних сил.
Если сама система совершает работу, то работа положительна: +А> 0, если над системой совершается работа, то она отрицательна: –А< 0.
Пусть, например, при обратимом процессе сама система возвращается в первоначальное состояние. Это значит, что ее внутренняя энергия не изменяется, т.е. изменение внутренней энергии 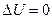 . Подставляя в первое начало термодинамики, получим:
. Подставляя в первое начало термодинамики, получим: 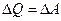 . (9.8)
. (9.8)
Но, т.к. обратимых процессов в природе не существует, то выражение (9.8) трактуется как невозможность создания вечного двигателя первого рода: система может совершить в лучшем случае только такую работу, какое количество тепла ей передано. Это значит, что невозможно, один раз передав системе энергию, получить вечно работающий механизм, совершающий работу больше, чем переданная ему теплота.
Методика определения удельной теплоемкости твердых тел в данной работе основана на использовании закона сохранения энергии при тепловом обмене, который называется уравнением теплового баланса при условии, что тепло не рассеивается в окружающую среду, т. е., что система замкнута.
Нагреем твердое тело и опустим его в воду, налитую в калориметр. Твердое тело будет остывать, отдавая некоторое количества теплоты D Q 1стаканчику калориметра и воде, которые, в свою очередь, получают от нагретого тела количество теплоты D Q 2 и D Q 3, нагреваясь при этом. В результате, в термодинамической системе «калориметр – вода - твердое тело» устанавливается состояние термодинамического равновесия при некоторой равновесной температуре T. Тогда уравнение теплового баланса для системы примет вид:
D Q 1= D Q 2 + D Q 3. (9.9)
Твердое тело массой т 1с удельной теплоемкостью с 1и нагретое до температуры T 1, остывая до температуры равновесия T, отдает количество теплоты D Q 1, которое можно определить по формуле (9.3):
D Q 1 =m 1 c 1 (T 1 -T). (9.10)
Стаканчик калориметра (внутренний стаканчик) массой т 2 с удельной теплоемкостью с 2нагревается от температуры T 2 до температуры равновесия T, принимая количество теплоты D Q 2: D Q 2 =m 2 c 2 (T 2 -T). (9.11)
Вода массой т 3судельной теплоемкостью с 3, налитая в стаканчик калориметра также нагревается от температуры T 2до температуры равновесия T принимая количество теплоты D Q 3: D Q 3 =m 3 c 3 (T 3 -T). (9.12)
Подставим (9.10), (9.11), (9.12) в уравнение теплового баланса (9.9):
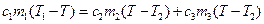 . (9.13)
. (9.13)
Раскрывая скобки, получим: 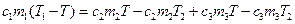 .
.
Скомпонуем слагаемые: 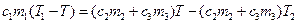 .
.
Вынесем 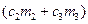 за скобки:
за скобки: 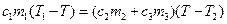 .
.
Откуда, удельная теплоемкость исследуемого твердого тела:
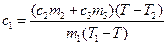 . (9.14)
. (9.14)
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 518; Нарушение авторских прав?; Мы поможем в написании вашей работы!