
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структура ферментов
|
|
|
|
Краткая история ферментологии
СТРУКТУРА, СВОЙСТВА И МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ
Экспериментальное изучение ферментов в 19 веке совпало по времени с изучением процессов дрожжевого брожения, что нашло отражение в терминах «ферменты» и «энзимы». Название ферменты возникло от латинского слова fermentatio – брожение. Термин энзимы произошёл от понятия en zyme - из дрожжей. Вначале этим названиям придавали разный смысл, но в настоящее время они являются синонимами.
Первая ферментативная реакция осахаривания крахмала солодом была исследована отечественным учёным К.С. Кирхгоффом в 1814 году. Впоследствии были предприняты попытки выделения ферментов из дрожжевых клеток (Э. Бюхнер, 1897 год). В начале ХХ века Л. Михаэлис и М. Ментен разработали теорию ферментативного катализа. В 1926 году Д. Самнер впервые выделил очищенный препарат фермента уреазы в кристаллическом состоянии. В 1966 году Б. Меррифилду удалось осуществить искусственный синтез фермента РНК-азы.
Ферменты – это высокоспециализированные белки, способные повышать скорость реакции в живых организмах. Ферменты - биологические катализаторы.
Все ферменты являются белками, как правило, глобулярными. Они могут относиться как к простым, так и к сложным белкам. Белковая часть фермента может состоять из одной полипептидной цепи и относиться к мономерным белкам (например, пепсин). Ряд ферментов являются олигомерными белками, включают в свой состав несколько протомеров или субъединиц. Протомеры, объединяясь в олигомерную структуру, соединяются самопроизвольно непрочными нековалентными связями. В процессе объединения (кооперации) происходят структурные изменения отдельных протомеров, в результате чего активность фермента заметно возрастает. Отделение (диссоциация) протомеров и их объединение в олигомерный белок является механизмом регуляции активности ферментов.
Субъединицы (протомеры) в олигомерах могут быть или одинаковыми, или отличающимися по первичной - третичной структуре (конформации). В случае соединения различных протомеров в олигомерную структуру фермента возникают множественные формы одного и того же фермента – изоферменты.
Изоферменты катализируют одну и ту же реакцию, но отличаются по набору субъединиц, физико-химическим свойствам, электрофоретической подвижности, по сродству к субстратам, активаторам, ингибиторам. Например, лактатдегидрогеназа (ЛДГ) – фермент, окисляющий молочную кислоту в пировиноградную кислоту, является тетрамером. Он состоит из четырёх протомеров двух типов. Один вид протомеров обозначается Н (выделен из сердечной мышцы), второй протомер обозначается М (выделен из скелетной мускулатуры). Возможно 5 сочетаний этих протомеров в составе ЛДГ: Н4, Н3М, Н2М2, Н1М3, М4 соответственно ЛДГ1, ЛДГ2,ЛДГ3,ЛДГ4, ЛДГ5.
Биологическая роль изоферментов.
- Изоферменты обеспечивают протекание химических реакций в соответствии с условиями в разных органах. Так, изофермент ЛДГ1 – обладает высоким сродством к кислороду, поэтому он активен в тканях с высокой скоростью окислительных реакций (эритроциты, миокард). Изофермент ЛДГ5 активен в присутствии высокой концентрации лактата, наиболее характерен для ткани печени.
- Выраженная органоспецифичность изоферментов используется для диагностики заболеваний различных органов.
- Изоферменты изменяют свою активность с возрастом. Так, у плода при недостатке кислорода преобладает ЛДГ3, а с увеличением возраста и увеличением поступления кислорода возрастает доля ЛДГ2.
Если фермент является сложным белком, то он состоит из белковой и небелковой части. Белковая часть является высокомолекулярной, термолябильной частью фермента и называется апоферментом. Он имеет своеобразную структуру и определяет специфичность ферментов.
Небелковая часть фермента называется кофактором (коферментом). Кофактором чаще всего являются ионы металлов, которые могут прочно связываться с апоферментом (например, Zn в ферменте карбоангидразе, Сu в ферменте цитохромоксидазе). Коферменты обычно являются органическими веществами, менее прочно связанными с апоферментом. Коферментами являются, в частности, нуклеотиды НАД, ФАД. Кофермент– низкомолекулярная, термостабильная часть фермента. Его роль заключается в том, что он определяет пространственную укладку (конформацию) апофермента, и определяет его активность. Некоторые кофакторы могут переносить электроны, функциональные группы, участвовать в образовании дополнительных связей между ферментом и субстратом.
В функциональном отношении в ферменте принято выделять два важных участка в молекуле фермента: активный центр и аллостерический участок.
Активный центр – это участок молекулы фермента, который взаимодействует с субстратом и участвует в каталитическом процессе. Активный центр фермента образован радикалами аминокислот, удалённых друг от друга в первичной структуре. Активный центр имеет трёхмерную укладку, чаще всего в его составе выявляются реакционноспособные
- ОН группы серина
- SH – цистеина
- NH2 лизина
- γ-СООН глютаминовой кислоты
Схема активного центра фермента
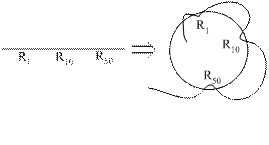
В активном центре различают две зоны – зону связывания с субстратом и каталитическую зону.
Зона связывания обычно имеет жёсткую пространственную структуру, к которой комплементарно присоединяется субстрат реакции. Например, трипсин расщепляет белки в участках, богатых положительно заряженной аминокислотой лизином, так как в его зоне связывания содержатся остатки отрицательно заряженных аспарагиновой и глютаминовой кислот.
Каталитическая зона - это участок активного центра, непосредственно воздействующий на субстрат и осуществляющий каталитическую функцию. Эта зона более подвижна, в ней возможно изменение взаиморасположения функциональных групп.
В ряде ферментов (чаще олигомерных) кроме активного центра присутствует аллостерический участок – участок молекулы фермента, удалённый от активного центра и взаимодействующий не с субстратом, а с дополнительными веществами (регуляторами, эффекторами). В аллостерических ферментах в одной субъединице может находиться активный центр, в другой - аллостерический участок. Аллостерические ферменты изменяют свою активность следующим образом: эффектор (активатор, ингибитор) действует на аллостерическую субъединицу и изменяет её структуру. Затем изменение конформации аллостерической субъединицы по принципу кооперативных изменений опосредованно меняет структуру каталитической субъединицы, что сопровождается изменение активности фермента.
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 581; Нарушение авторских прав?; Мы поможем в написании вашей работы!