
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции гиперчувствительности
|
|
|
|
Реакции гиперчувствительности это местные иммунные (ал-
лергические) реакции, совершающиеся в сенсибилизированном организме.
Механизм развития реакций гиперчувствительности различен. Выделяют
пять механизмов, с которыми связаны реакции гиперчувствительности.
Первый механизм связан с аллергическими антителами, или реагина-
ми (IgE), которые фиксируются на поверхности клеток (лаброциты, базо-
филы). Выброс медиаторов при соединении антител с клеткой (антигеном) ве-
дет к развитию острого воспаления — анафилактических реакций
немедленнного типа.
Второй механизм представлен цитотоксическим и цитолитическим
действием на соответствующие клетки циркулирующих антител и (или) комп-
лемента — цитотоксические реакции. Цитолиз может быть обуслов-
лен либо комплементом (цитотоксичность, опосредованная комплемен-
том), который активируется при соединении антител с антигеном, либо анти-
телами (цитотоксичность, опосредованная антителами), которые связаны
с клетками — К-клетки и NK-клетки (схема IX).


|
Третий механизм связан с токсическим действием на клетки и ткани
циркулирующих иммунных комплексов, что ведет к активации
компонентов комплемента и развитию острого воспаления — реакции
токсических иммунных комплексов (схема X).
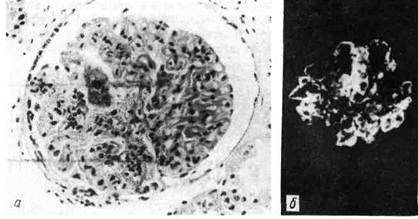
Рис. 95. Реакция гиперчувствительности немедленного типа.
а — фибриноидное набухание и фибриноидный некроз капилляров почечного клубочка при системной
красной волчанке; б—в участках фибриноида фиксация IgG. Иммунолюминесцентное исследование.
Четвертый механизм обусловлен действием на ткани эффекторных
клеток — лимфоцитов-киллеров и макрофагов. Развиваются цито-
лиз, обусловленный л и м ф о ц и т а м и, и воспалительная реакция.
Пятый механизм — гранулематоз (см. с. 132).
Следовательно, одни иммунологические механизмы являются проявлением
гуморального иммунитета (антитела, компоненты комплемента, циркулирую-
щие комплексы антиген — антитело), другие — клеточного иммунитета (лимфо-
циты, макрофаги). Это определяет характер реакций гиперчувствительности
и принципы их классификации. Реакции, связанные с иммунопатологическими
механизмами, являющимися проявлением гуморального иммунитета, назы-
вают реакциями гиперчувствительности немедленного т и -
п а (ГНТ), а связанные с иммунопатологическими механизмами, являющими-
ся проявлением клеточного иммунитета — реакциями гиперчувстви-
тельности замедленного типа (ГЗТ). Кроме того, выделяют
реакции трансплантационного иммунитета (реакции от-
торжения).
Морфологическая характеристика. 1. Реакция гиперчувствитель-
ности немедленного типа (ГНТ). Для этой реакции характерна мор-
фология острого иммунного воспаления (А. И. Струков), которо-
му свойственны быстрота развития, преобладание альтеративных и сосудис-
то-экссудативных изменений, медленное течение репаративных процессов. Аль-
теративные изменения касаются преимущественно стенок сосудов, основного
вещества и волокнистых структур соединительной ткани. Они представлены
плазматическим пропитыванием, мукоидным и фибриноидным набуханием
(рис. 95). Крайним выражением альтерации является характерный для ГНТ
фибриноидный некроз. С ярко выраженными плазморрагическими и сосуди-
сто-экссудативными реакциями связано появление в очаге иммунного воспа-
ления грубодисперсных белков, фибриногена (фибрина), нейтрофилов, «пере-
варивающих» иммунные комплексы, и эритроцитов. В связи с этим наиболее
характерным для ГНТ становится фибринозный или фибринозно-
геморрагический экссудат. Пролиферативно-репаративные реакции
при ГНТ развиваются позже и выражены слабее. Они проявляются пролифе-
рацией клеток эндотелия и перителия (адвентиции) сосудов и во времени со-
впадают с появлением мононуклеарно-гистиоцитарных элементов, что отра-
жает элиминацию иммунных комплексов и начало репаративных процессов.
Оценка морфологических изменений при ГНТ, их принадлежность к иммун-
ной реакции требуют доказательств с помощью иммуногистохимического ме-
тода (см. рис. 95).
Наиболее типично динамика морфологических изменений при ГНТ пред-
ставлена при феномене Артюса, который возникает у сенсибилизиро-
ванных животных при локальном введении разрешающей дозы антигена.
В патологии человека ГНТ составляет сущность многих бактериальных ин-
фекций, аллергических заболеваний и процессов, протекая с преобладанием
альтеративных или сосудисто-экссудативных изменений. Проявления ГНТ
с преобладанием альтерации (казеозный некроз) постоянны при туберкулезе,
сифилисе, они лежат в основе сосудистых изменений (фибриноидный некроз)
при системной красной волчанке, гломерулонефрите, узелковом периартерии-
те и др. Сосудисто-экссудативные проявления ГНТ ярко выражены при
крупозной пневмонии; к ним относятся полисерозиты и артриты при
ревматизме, туберкулезе, бруцеллезе и других болезнях.
Реакциям ГНТ подобны так называемые реагиновые реакции, т. е.
реакции, в которых участвуют аллергические антитела, или реагины (IgE),
фиксированные на клетках. Они отличаются поверхностной альтерацией кле-
ток и тканей, что объясняют отсутствием участия комплемента в реакции
и преобладанием сосудисто-экссудативных изменений, связанных с массивной
дегрануляцией лаброцитов и выбросом гистамина. Примером реагиновой ре-
акции могут служить изменения при атопической бронхиальной астме (см.
«Бронхиальная астма»).
2. Реакция гиперчувствительности замедленного типа
(ГЗТ). В этой реакции участвуют два вида клеток — сенсибилизиро-
ванные лимфоциты и макрофаги. Лимфоцитарная и макрофагаль-
ная инфильтрация в очаге иммунного конфликта является выражением хро-
нического иммунного воспаления; лежащего в основе ГЗТ
(А. И. Струков).
Разрушение клетки-мишени, т. е. иммунологически обуслов-
ленный клеточный цитолиз, связано с активацией лизосомных
ферментов лимфоцитов-киллеров (см. схему IX). Макрофаги вступают
в специфическую реакцию с антигеном при помощи медиаторов
клеточного иммунитета — лимфокинов и цитофильных антител, ад-
сорбированных на поверхности этих клеток. При этом между
лимфоцитами и макрофагами появляются контакты в виде ц и т о-
плазматических мостиков, которые, по-видимому, служат для обме-
на информацией между клетками об антигене.
Доказательством участия Т-лимфоцитов в ГЗТ является тот факт, что
у тимэктомированных в период новорожденности животных ГЗТ не разви-
вается и трансплантат не отторгается. С помощью сенсибилизированных лим-
фоцитов возможна передача ГЗТ.
Воспаление в виде лимфогистиоцитарной и макрофагальной инфильтрации
ткани в сочетании с сосудисто-плазморрагическими и паренхиматозно-дистро-
фическими процессами может считаться иммунным, т. е. отражающим
ГЗТ, лишь при наличии доказательств связи клеток инфильтрата с сенсибили-
зированными лимфоцитами. Эти доказательства могут быть найдены при ги-
стохимическом и электронно-микроскопическом исследовании (повышение ак-
тивности кислой фосфатазы и падение активности дегидрогеназ в лимфоци-
тах, увеличение объема их ядер и ядрышек, увеличение числа полисом,
гипертрофия комплекса Гольджи).
К клинико-морфологическим проявлениям ГЗТ огно-

Рис. 96. Реакция отторжения аллотрансплантата почки от живого донора.
а — гнездная перивасхулярная и перигломерулярная лимфоцитарная инфильтрация через 14 сут после
операции; 6 — диффузная лимфоцитарная инфильтрация через 23 сут после операции.
с я т: реакцию туберкулинового типа в коже в ответ на введение антигена, кон-
тактный дерматит (контактную аллергию), аутоиммунные болезни, иммуни-
тет при многих вирусных и некоторых бактериальных (туберкулез, бруцеллез,
туляремия) инфекциях.
Морфологическим проявлением ГЗТ служит гранулематоз (см. с.
132), который, однако, может быть выражением иммунопатологических про-
цессов различного содержания. О причастности гранулемы к ГЗТ можно гово-
рить в тех случаях, когда она предназначена для резорбции продуктов иммун-
ной реакции и распада в очагах иммунного повреждения. Примером такой
гранулемы может служить характерная для ревматизма макрофагальная
гранулема Ашоффа-Талалаева. К ГЗТ могут быть отнесены и гранулемы, ха-
рактерные для специфического воспаления (при туберкулезе, сифилисе, лепре),
хотя они и являются гранулемами не столько иммунного фагоцитоза
(незавершенный фагоцитоз возбудителя гигантскими клетками), сколько гра-
нулемами отграничения.
Для определения ГЗТ в клинике и эксперименте разработан ряд критериев и тестов. In vivo
ГЗТ определяют при помощи внутрикожной пробы с антигеном, путем пассивного переноса ГЗТ
от одного животного другому клетками лимфоидных органов, а также с помощью реакции ис-
чезновения макрофагов из брюшной полости при подкожном введении антигена сенсибилизиро-
ванным животным.
Для определения ГЗТ in vitro используют: реакцию бласттрансформации лимфоцитов под
действием антигена или неспецифического антигенного раздражителя, феномен цитопатического
действия лимфоцитов на нормальные фибробласты в культуре ткани в присутствии антигена,
реакцию угнетения макрофагов под действием антигена и реакцию адсорбции на лимфоцитах
аутоэритроцитов, нагруженных антигеном. Эти тесты специфичны в отношении используемого
в реакции антигена.
Реакции ГНТ и ГЗТ нередко сочетаются или сменяют друг друга, отражая
динамику иммунопатологического процесса.
3. Проявления трансплантационного иммунитета пред-
ставлены реакцией организма реципиента на генетически чужеродный транс-
плантат донора, т. е. реакцией отторжения трансплантата. Анти-
гены трансплантата индуцируют выработку специфических антител, которые
циркулируют в крови, и продукцию сенсибилизированных лимфоцитов, осу-
ществляющих клеточную инвазию трансплантата. Основную роль в реакции
отторжения играют сенсибилизированные лимфоциты, поэтому проявле-
ния трансплантационного иммунитета подобны ГЗТ.
Морфологические проявления реакции отторжения сводятся к нарастаю-
щей инфильтрации трансплантата в основном лимфоцитами, а также гистио-
цитами в результате инвазии этих клеток и размножения их на месте (рис. 96).
Клеточная инфильтрация сопровождается расстройством кровообращения
и отеком трансплантата. В финале среди клеток инфильтрата появляется
много нейтрофилов и макрофагов. Считают, что иммунные лимфоциты, раз-
рушая клетки трансплантата, способны насыщаться его антигенами, поэтому
гуморальные антитела, направленные против трансплантационных антигенов,
не только связываются с клетками трансплантата, но и лизируют лимфоциты.
Высвобождающиеся из активированных лимфоцитов ферменты разрушают
клетки трансплантата, что ведет к высвобождению новых транспланта-
ционных антигенов. Так осуществляется все нарастающая ферментатив-
ная деструкция трансплантата.
Реакция отторжения может быть подавлена с помощью ряда иммуно-
депрессивных средств. Это позволяет при пересадке органов и тканей
пользоваться не только изотрансплантатом (реципиент и донор — близнецы),
но и аллотрансплантатом (реципиент и донор чужеродны) как от живого че-
ловека, так и от трупа.
Аутоиммунные болезни
Аутоиммунные болезни — группа заболеваний, основным механизмом раз-
вития которых является реакция аутоантител и сенсибилизированных лимфоци-
тов против нормальных антигенов собственных тканей.
Аутоиммунизация тесно связана с понятием иммунологической толерантности
(от лат. tolerare — переносить, терпеть). Оно характеризуется состоянием ареактивности («терпи-
мости») лимфоидной ткани по отношению к тем веществам антигенной природы, которые
в обычных условиях вызывают развитие иммунного ответа. В период созревания лимфоидной
ткани возникает иммунологическая толерантность к антигенам всех органов и тканей, кроме
тканей глаза, щитовидной железы, семенников, надпочечников, головного мозга и нервов. Счи-
тается, что антигены этих органов и тканей отграничены от лимфоидной ткани специальными
физиологическими барьерами, что и объясняет отсутствие к ним толерантности иммунокомпе-
тентной системы.
В основе развития аутоиммунных заболеваний лежит агрессия аутоанти-
тел, циркулирующих иммунных комплексов, содержащих аутоантигены, и эф-
фекторных иммунных клеток (лимфоцитов-киллеров) в отношении антигенов
собственных тканей организма. Поэтому аутоиммунные болезни называют
также аутоагрессивными.
Среди этиологических факторов ведущее значение придается
хронической вирусной инфекции и генетическим наруше-
ниям, о чем свидетельствует повышенная частота обнаружения опреде-
ленных антигенов HLA при аутоиммунных заболеваниях.
В основе патогенеза аутоиммунизации могут лежать три разных
механизма: 1) нарушение физиологической изоляции органов и тканей, по
отношению к которым иммунологическая толерантность отсутствует; 2) пер-
вичные нарушения в иммунокомпетентной системе, ведущие к потере способ-
ности различать «свои» и «чужие» антигены; 3) появление в организме новых,
чужеродных антигенов.
По механизму развития аутоиммунизации различаются три группы ау-

Рис. 97. Струма Хашимото (истинная аутоиммунная болезнь).
а — микроскопическая картина: инфильтрация лимфоцитами ткани щитовидной железы, разрушение
паренхиматозных элементов; б — электронограмма: миграция лимфоцита (Лц) междy клетками фоллику-
ла (КФ); множественные контакты и переплетения цитоплазматических отростков лимфоцита и фол-
ликулярных клеток (показано стрелкой); П p — просвет фолликула, х 10000 (по Ирвину и Муру).
тоиммунных заболеваний. В первую группу их входят: струма (болезнь)
Хашимото (рис. 97), энцефаломиелит, полиневрит, рассеянный склероз,
«идиопатическая» аддисонова болезнь, асперматогения, симпатическая оф-
тальмия. Это— органоспецифические аутоиммунные болезни, воз-
никновение которых провоцирует инфекция, особенно вирусная, хроническое
воспаление и другие факторы. Аутоиммунизация развивается в связи с по-
вреждением физиологических барьеров иммунологически обособленных ор-
ганов, что позволяет иммунной системе реагировать на их неизмененные ан-
тигены выработкой аутоантител и сенсибилизированных лимфоцитов. При
этом в органах развиваются морфологические изменения, характерные преиму-
щественно для ГЗТ — ткань органов инфильтрируется лимфоцитами, паренхи-
матозные элементы погибают (см. рис. 97), в финале развивается склероз.
Ко второй группе аутоиммунных заболеваний относят: ревматизм,
системную красную волчанку, ревматоидный артрит, системную склеродер-
мию, дерматомиозит (группа ревматических болезней, вторичную гемолити-
ческую пурпуру (болезнь Мошковича). Ведущими при этих органонеспе-
цифических аутоиммунных заболеваниях являются нарушения контроля
иммунологического гомеостаза лимфоидной системой, которые могут возни-
кать в связи с генетическими факторами, вирусной и бактериальной инфекций,
действием радиации. Аутоиммунизация развивается по отношению к антигенам
многих органов и тканей, не обладающих органной специфичностью и не спо-
собных вызывать продукцию антител при парентеральном введении. В орга-
нах и тканях при этих заболеваниях развиваются морфологические изменения,
характерные для реакций гиперчувствительности как замедленного, так и осо-
бенно немедленного типов.
Существуют аутоиммунные болезни, близкие заболеваниям первой или
второй группы — аутоиммунные заболевания промежуточно-
го типа. Это миастения гравис, синдромы Шегрена и Гудпасчера и др.
В третью группу аутоиммунных заболеваний включают: опреде-
ленные формы гломерулонефрита, гепатита, хронического гастрита и энтери-
та, цирроз печени, ожоговую болезнь, аллергические анемии, агранулоцитоз,
лекарственную аллергию. Появление аутоантигенов при этих заболеваниях
связывают с изменением антигенных свойств тканей и органов — денатура-
цией тканевых белков при ожоге, облучении, травме, хроническом воспале-
нии, вирусной инфекции. Образование аутоантигена возможно при воздей-
ствии бактериального антигена, особенно перекрестно реагирующего, как это
наблюдается, например, при гломерулонефрите, ревматизме. В образовании
аутоантигена большое значение придается гаптенному механизму, причем
в роли гапгена могут выступать как продукты обмена тела, так и микроорга-
низмы, токсины и лекарственные средства. Аутоиммунизация в этих условиях
определяет не возникновение заболевания, а прогрессирование характерных
для него локальных (органных) изменений, которые отражают морфологию
реакций гиперчувствительности замедленного и немедленного типов.
Как видно из изложенного, к аутоиммунным болезням следует относить
лишь заболевания первой и второй групп. Аутоиммунизация при заболева-
ниях третьей группы не является основным их содержанием. Возникая вторич-
но в связи с основным процессом, аутоиммунизация в таких случаях опреде-
ляет прогрессирование болезней и их исход. Такие заболевания принято
называть в последнее время не аутоиммунными, а болезнями с аутоим-
мунными нарушениями.
Иммунодефицитные синдромы
Иммунодефицитные синдромы являются крайним проявлением недо-
статочности иммунной системы. Они могут быть первичными,
обусловленными недоразвитием (гипоплазия, аплазия) иммунной системы —
наследственные и врожденные иммунодефицитные син-
дромы, или вторичными, возникающими в связи с болезнью или про-
водимым лечением,—приобретенные иммунодефицитные синдромы.
Первичные иммунодефицитные синдромы
Первичные иммунодефицитные синдромы могут быть выражением недо-
статочности: 1) клеточного и гуморального иммунитета; 2) клеточного имму-
нитета; 3) гуморального иммунитета.
Синдромы недостаточности клеточного и гуморально-
го иммунитета называют комбинированными. Они встречаются
у детей и новорожденных, наследуются по аутосомно-доминантному типу
(агаммаглобулинемия швейцарского типа, или синдром Гланцманна и Рини-
кера; атаксия-телеангиэктазия Луи-Бар). При этих синдромах находят гипо-
плазию как тимуса, так и периферической лимфоидной ткани (табл. 4), что
и определяет дефект клеточного и гуморального иммунитета. В связи с несо-
стоятельностью иммунитета у таких детей часты инфекционные заболевания,
которые имеют рецидивирующее течение и дают тяжелые осложнения (пнев-
мония, менингит, сепсис), отмечается задержка физического развития. При
комбинированных иммунодефицитных синдромах часто возникают пороки
развития и злокачественные мезенхимальные опухоли (атаксия-телеангиэкта-
зия Луи-Бар).
Синдромы недостаточности клеточного иммунитета
в одних случаях наследуются обычно, по аутосомно-доминантному типу (им-
Таблица 4

мунодефицит с ахондроплазией, или синдром Мак-Кьюсика), в других
являются врожденными (агенезия или гипоплазия тимуса, или синдром Дай-
джорджа). Помимо агенезии или гипоплазии тимуса и Т-зависимых зон пери-
ферической лимфоидной ткани, что определяет дефицит клеточного иммуни-
тета, для этих синдромов характерны множественные пороки развития (см.
табл. 4). Дети погибают от пороков развития либо от осложнений инфек-
ционных заболеваний.
Синдромы недостаточности гуморального иммунитета
имеют наследственную природу, причем установлена сцепленность их с X-
хромосомой (см. табл. 4). Болеют дети первых пяти лет жизни. Для одних
синдромов (агаммаглобулинемия, сцепленная с Х-хромосомой, или синдром
Брутона) характерна потеря способности к синтезу всех иммуноглобулинов,
что морфологически подтверждается отсутствием В-зависимых зон и клеток
плазмоцитарного ряда в периферической лимфоидной ткани, прежде всего
в лимфатических узлах и селезенке. Другим синдромам свойствен дефицит
одного из иммуноглобулинов (например, избирательный дефицит IgA, или
синдром Веста), тогда структура лимфоидной ткани остается сохранной. Од-
нако при всех синдромах недостаточности гуморального иммунитета разви-
ваются тяжелые бактериальные инфекции с преобладанием гнойно-деструк-
тивных процессов в бронхах и легких, желудочно-кишечном тракте, коже,
ЦНС, нередко заканчивающихся сепсисом.
Помимо иммунодефицитных, известны синдромы недостаточно-
сти системы моноцитарных фагоцитов, среди которых наиболее
изучена так называемая хроническая гранулематозная болезнь.
Вторичные иммунодефицитные синдромы
Вторичные (приобретенные) иммунодефицитные синдромы в отличие от
первичных возникают в связи с болезнью или определенным видом лечения;
встречаются они, как правило, у взрослых.
Среди заболеваний, ведущих к развитию вторичной недостаточности
иммунной системы, наиболее часты лейкозы, злокачественные лимфомы (лим-
фогранулематоз, лимфосаркома, ретикулосаркома), тимома, вирусные инфек-
ции, саркоидоз. При этих заболеваниях возникает недостаточность гуморально-
го и клеточного иммунитета в результате дефекта популяции как В-, так и Т-
лимфоцитов, а возможно, и их предшественников.
Среди видов лечения, ведущих к вторичной недостаточности иммун-
ной системы, наибольшее значение имеют лучевая терапия, применение кор-
тикостероидов и иммунодепрессантов, антилимфоцитарной сыворотки, тимэк-
томия, дренирование грудного протока и ряд других. Недостаточность
иммунной системы, развивающаяся в связи с лечением той или иной болезни,
рассматривается как патология терапии.
При вторичных, как и первичных, иммунодефицитных синдромах часто на-
блюдаются гнойные инфекции, обострение туберкулезного процесса, сепсис.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 3944; Нарушение авторских прав?; Мы поможем в написании вашей работы!