
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Практична робота. Дослід 1. Фракціонування білків плазми крові методом висолювання: визначення альбумінів і глобулінів плазми крові
|
|
|
|
Дослід 1. Фракціонування білків плазми крові методом висолювання: визначення альбумінів і глобулінів плазми крові.
Принцип методу. Білки можна виділити з розчинів у вигляді осадів. Існує багато різних способів осадження білків. Осадження білків концентрованими розчинами нейтральних солей (амонію сульфату, натрію хлориду тощо) називають висолюванням. Більшість реакцій висолювання, а також реакції зі спиртом, ацетоном є зворотними.
Якщо до розчинів білків додавати солі лужних і лужноземельних металів, то їх іони адсорбуються молекулами білків, знімають з них електричні заряди і перетворюють їх на електронейтральні. Надалі колоїдні частки укрупнюються, що зумовлює утворення осаду. Реакцію висолювання зумовлює дегідратація молекул білка з одночасною нейтралізацією електричних зарядів. Процес висолювання білків є оборотною реакцією, оскільки осад білка можна знову розчинити шляхом розведення його водою або зменшення концентрації солей діалізом. Для висолювання білків потрібна різна концентрація солей. Це дає змогу отримати різні білкові фракції.
Білки осаджують за різних концентрацій солей. Деякі з них вже випадають в осад за концентрації амонію сульфату приблизно до 1/10 від насичення, глобуліни – за напівнасичення, альбуміни – за повного насичення.
Матеріальне забезпечення: розчин сироватки крові, амонію сульфат, лійки, фільтри.
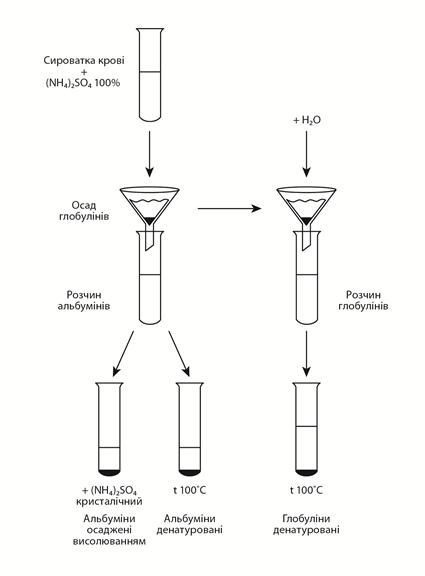 Хід роботи: У пробірку вливають 2 – 3 мл сироватки крові, додають рівний об’єм насиченого розчину амонію сульфату, перемішують. В осад випадають глобуліни (50 % насичення розчину), які мають відносно велику молекулярну масу і невеликий заряд. Осад відфільтровують. До осаду на фільтрі додають невелику кількість води, в отриманому розчині містяться глобуліни, наявність яких виявляють шляхом кип’ятіння, спостерігають утворення осаду. Фільтрат з розчином альбумінів розливають у дві пробірки.
Хід роботи: У пробірку вливають 2 – 3 мл сироватки крові, додають рівний об’єм насиченого розчину амонію сульфату, перемішують. В осад випадають глобуліни (50 % насичення розчину), які мають відносно велику молекулярну масу і невеликий заряд. Осад відфільтровують. До осаду на фільтрі додають невелику кількість води, в отриманому розчині містяться глобуліни, наявність яких виявляють шляхом кип’ятіння, спостерігають утворення осаду. Фільтрат з розчином альбумінів розливають у дві пробірки.
У першу пробірку додають кристалічний амоній сульфат до повного насичення (100 % насичення розчину). В осад випадають альбуміни. Вміст другої пробірки кип’ятять, спостерігають утворення осаду альбумінів.
Схема розділення альбумінів та глобулінів крові
шляхом висолювання амонію сульфатом
Фракціонування білків методом висолювання використовують у клінічній практиці для одержання нативних білків з біологічних рідин.
Фракційне розділення білків сироватки крові.
| Назва білка | Сіль, що використовується | Ступінь насичення | Утворення осаду |
| Глобуліни Альбуміни |
Пояснити отримані результати. Зробити висновок. Звернути увагу на використання фракційного осадження білків у медичній практиці.
Клініко-діагностичне значення. Визначення окремих фракцій білків сироватки крові має велике значення для клінічної діагностики. В нормі вміст альбумінів крові становить 40 – 45 г/л, глобулінів – 20 – 30 г/л. При різних захворюваннях печінки (цирози, гепатити), при нефрозах, хронічних захворюваннях шлунка, новоутвореннях травного тракту концентрація альбумінів крові знижується. При гострих інфекційних захворюваннях, ревматизмі зростає концентрація α2-глобулінів. Концентрація β – глобулінів зростає при гепатитах, мієломній хворобі, а γ – глобулінів – при хронічних процесах, хронічних поліартритах.
Осадження білків застосовується при виділенні їх з тканин, розділенні суміші білків, для виявлення у різних біологічних рідинах. Методом висолювання виділяють три фракції білків плазми крові: альбуміни, глобуліни, фібриноген. Під час денатурації відбувається руйнування нативної просторової структури білкової молекули, що проявляється зменшенням або повною втратою їх розчинності, зміною хімічних властивостей білків, втратою специфічної біологічної активності. Явище денатурації широко використовують у практиці. Так, денатуровані білки краще піддаються дії протеолітичних ферментів.
Під час денатурації втрачається біологічна активність білків (відбувається інактивація ферментів, гормонів, вірусів), тому водний розчин фенолу (карболової кислоти) застосовують як антисептик.
У практичній діяльності використовують в’яжучі речовини (танін, танальбін, протаргол тощо), які денатурують поверхневий шар білків слизової травного тракту з утворенням плівки коагульованого білка. Остання покриває слизову і таким чином зменшує її механічне та хімічне подразнення.
Явище денатурації білків широко використовують у промисловості (при випіканні хліба, дубінні шкіри тощо). Методом висолювання білків користуються для добування білків, що мають кристалічний вигляд, виділення препаратів ферментів і гормонів.
Реакції осадження білків мають важливе значення в практиці. Їх застосовують для вивчення властивостей білків, виділення білків із розчинів, виявлення наявності білків у сечі (при нефриті, серцевій декомпенсації тощо).
Дослід 2. Визначення залишкового азоту крові (метод Боданського).
Принцип методу. Залишковий азот крові визначають у безбілковому фільтраті після осадження білків крові; безбілковий фільтрат мінералізують концентрованою сульфатною кислотою. При цьому азот всіх азотовмісних сполук у вигляді аміаку зв’язується з сульфатною кислотою і утворює амонію сульфат, який з реактивом Несслера утворює сполуку жовто-оранжевого кольору. Інтенсивність забарвлення розчину пропорційна концентрації азоту.
Матеріальне забезпечення: кров, 10 % розчин трихлорацетатної кислоти, сульфатна кислота концентрована, гідрогену пероксид концентрований, 12,5 М розчин натрію гідроксиду, реактив Несслера, стандартний розчин (1 мл розчину амонію сульфату містить 0,05 мг азоту), лакмусовий папір, мікропіпетки, ФЕК, термостійкі пробірки.
Хід роботи:
1. Отримання безбілкового фільтрату.
У центрифужну пробірку наливають 2,8 мл 10 % розчину трихлорацетатної кислоти і 0,2 мл крові. Суміш ретельно перемішують, залишають на 15 хв і центрифугують.
2. Мінералізація.
У пробірку з тугоплавкого скла вносять 0,5 мл центрифугату, добавляють 0,05 мл концентрованої сульфатної кислоти. Спалювання здійснюють на пісочній бані. При спалюванні пробірка повинна торкатися тільки верхнього шару піску. Спочатку випаровується вода – досліджувана рідина буріє. Пробірку знімають з бані, дають їй охолонути, добавляють у пробірку 2 краплі гідрогену пероксиду концентрованого і знову ставлять для спалювання до знебарвлювання рідини. Слід перевірити колір рідини у пробірці після її охолодження, оскільки часто рідина, яка здається безбарвною у гарячому стані, при охолодженні темнішає.
Після охолодження мінералізат розводять дистильованою водою і нейтралізують до слабколужної реакції.
Кольорова реакція (несслеризація). У пробірку відбирають 4 мл досліджуваного розчину і добавляють 0,5 мл реактиву Несслера (К2HgІ4), внаслідок чого вміст пробірки забарвлюється у жовтий колір різної інтенсивності залежно від вмісту азоту:
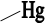 | |||
 | |||

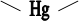 2 К2HgІ4 + 3 KOH + NH3 O NH2І + 7 KІ + 2 H2O
2 К2HgІ4 + 3 KOH + NH3 O NH2І + 7 KІ + 2 H2O
комплексна сполука
Одночасно з дослідною пробою обробляють стандартну пробу і контрольну (замість стандартного розчину амонію сульфату добавляють воду) проби. Дослідну і стандартну проби спектрофотометрують порівняно з контролем на реактиви при довжині хвилі 440 – 450 нм (фіолетовий світлофільтр) у кюветі товщиною 0,5 см.
Контрольні проби повинні мати легкий жовтуватий відтінок. Більш насичений колір контролю свідчить про наявність у дистильованій воді азоту (аміаку).
Розрахунок проводять за формулою:
Cд = Сст * (Ад/Аст) = 21,42 Ад/Аст,
де Сд – концентрація залишкового азоту в досліді, ммоль/л;
Ад – екстинкція дослідної проби;
Сст – концентрація залишкового азоту в стандарті (С ст = 21,4 ммоль/л);
Аст – екстинкція стандартної проби.
Вміст залишкового азоту в нормі в крові становить 14,3 – 25 ммоль/л, (20 – 35 мг %). Коефіцієнт перерахунку з мг/100 мл у ммоль/л – 0,714.
Пояснити отриманий результат. Зробити висновок.
Клініко-діагностичне значення. Визначення небілкового азоту і його окремих компонентів проводиться з метою: діагностики порушень видільної функції нирок та оцінки ступеня ниркової недостатності; оцінки сечовиноутворюючої функції печінки і виявлення печінкової недостатності; оцінки кількісних змін середніх молекул, які накопичуються в організмі при різних захворюваннях, що супроводжуються ендогенними інтоксикаціями.
Для початкових стадій деяких захворювань характерно не стільки підвищення залишкового азоту крові взагалі, скільки зміни у кількісному вмісті компонентів залишкового азоту, співвідношенням між ними та загальним азотом.
Ретенційна (ниркова) азотемія зустрічається при гломерулонефритах, пієлонефриті, туберкульозі та амілоїдозі нирок. Позаниркові ретенційні азотемії зумовлені порушенням гемодинаміки і, відповідно, зниженням клубочкової фільтрації. Вони виникають у результаті серцево-судинної декомпенсації, при локальному порушенні кровообігу в ниркових артеріях. Продукційна азотемія спостерігається при кахексії, лейкозах, новоутвореннях, кишковій непрохідності, лікуванні глюкокортикоїдами. Азотемія зустрічається у недоношених дітей.
Зменшення вмісту залишкового азоту спостерігається при недостатньому харчуванні, зокрема білковому, тяжкій печінковій недостатності, некрозі печінки, іноді при вагітності.
Дослід 3. Визначення рівня середніх молекул (СМ).
Рівень середніх молекул у сироватці крові визначають методами гель-хроматографії на сефадексі, високовольтного електрофорезу, іонообмінної хроматографії і спектрофотометрії.
Спектрофотометричний метод належить до експрес-методів.
Принцип методу. Полягає у вимірюванні на спектрофотометрі при λ=254 і λ=280нм оптичної густини сироватки крові, звільненої від високомолекулярних білків, ліпідів. Визначають дві фракції середніх молекул (СМ): ті, що містять ароматичні амінокислоти (виявляють при λ=280 нм), і ті, що не містять ароматичних амінокислот (виявляють при λ=254 нм).
Матеріальне забезпечення: сироватка крові, 10 % розчин трихлорацетатної кислоти, 10 % розчин натрію гідроксиду, мікропіпетки, піпетки, спектрофотометр.
Хід роботи: У центрифужну пробірку вміщують 1 мл сироватки крові, додають 0,5 мл 10 % розчину трихлорацетатної кислоти. Після перемішування проводять осадження білків на центрифузі при 3000 об/хв протягом 30 хв. До 0,5 мл центрифугату добавляють 4,5 мл дистильованої води, перемішують, вимірюють оптичну густину на СФ при λ=254 нм і 280 нм у кюветі з товщиною шару 1 см порівняно з контролем (контроль: 0,25 мл 10 % розчину трихлорацетатної кислоти змішують з 4,75 мл дистильованої води).
Рівень середніх молекул виражають у одиницях, що кількісно дорівнюють показникам екстинкції. Нормальним рівнем СМ у сироватці крові можна вважати значення до 0,246 ум.од. при λ=254 і до 0,296 ум.од. при λ=280.
Пояснити отриманий результат. Зробити висновок.
Клініко-діагностичне значення. Рівень СМ у сироватці крові хворих є одним з критеріїв клінічного перебігу і оцінки ефективності лікування цілого ряду захворювань. Кількість їх у крові значно збільшується при таких патологічних станах, як опікові хвороби, недостатність функції печінки і нирок, запальні процеси, ендогенна інтоксикація, злоякісні утворення тощо. Проведення ряду детоксикаційних заходів (гемодіаліз, гемосорбція тощо) впливає на рівень СМ, тому визначення їх рівня в динаміці захворювань і лікуванні необхідно використовувати тільки з метою оцінки ступеня тяжкості патології та ефективності лікувальних заходів, а не з метою діагностичного тесту.
Контроль виконання лабораторної роботи
1. Клініко-діагностичне значення визначення альбумінів і глобулінів крові.
2. Принцип методу визначення залишкового азоту крові. Клініко-діагностичне значення його визначення.
3. При гепатиті, інфаркті міокарда в плазмі крові різко зростає активність аланін- і аспартатамінотрансфераз. Які причини зростання активності цих ферментів?
А. Підвищення активності ферментів гормонами
В. Зростання швидкості синтезу амінокислот у тканинах
С. Збільшення швидкості розпаду амінокислот у тканинах
D. Нестача піридоксину
Е. Пошкодження мембран клітин і вихід ферментів у кров
4. При аналізі крові хворого визначені залишковий азот і сечовина.Частка сечовини в залишковому азоті значно зменшена. Для захворювання якого органа характерний даний аналіз?
А. Нирки
В. Серце
С. Кишечник
D. Печінка
Е. Шлунок
5. У хворого на гломерулонефрит спостерігається азотемія. На яку речовину припадає найбільше азоту?
А. Креатинін
В. Амінокислоти
С. Сечова кислота
D. Сечовина
Е. Амонійні солі
6. Вміст альбумінів у плазмі крові – 15 г/л. Як називається такий стан та які його наслідки для організму?
7. У хворих з постійною протеїнурією можуть з’явитися набряки. Пояснити причину такого стану.
8. Дитина перехворіла на інфекційне захворювання. Які зміни в білкових фракціях сироватки крові можна при цьому очікувати?
9. Як за вмістом залишкового азоту крові та загального азоту сечі диференціювати ретенційну і продукційну азотемії?
Приклади тестів „Крок-1”
1. У пацієнта вміст загального білка в плазмі крові в межах норми. Які серед наведених показників вірогідні для цього випадку?
А. 35-45 г/л
В. 50-60 г/л
С. 55-70 г/л
D. 65-85 г/л
Е. 85-95 г/л
2. При дослідженні крові хворого виявлено значне збільшення активності МВ-форм КФК (креатинфосфокінази) та ЛДГ1. Яка найбільш імовірна патологія?
А. Ревматизм
В. Інфаркт міокарда
С. Холецистит
D. Панкреатит
Е. Гепатит
3. У хворого діагностовано хворобу Вільсона-Коновалова, за якої спостерігається виділення іонізованої міді з сечею, відкладання її в органах і тканинах. Порушення синтезу якого білка плазми крові є найбільш вірогідною причиною цього захворювання?
А. Трансферину
В. Гаптоглобіну
С. Церулоплазміну
D. Пропердину
Е. Кріоглобуліну
Індивідуальна самостійна робота студентів
1. Роль білків та індикаторних ферментів плазми крові в нормі та при патології.
2. Оцінка показників азотистого обміну та зміни вмісту азотовмісних небілкових компонентів крові
3. Кількісні зміни залишкового азоту крові при парентеральному харчуванні, переливанні крові, застосуванні плазми, сироватки чи плазмозамінників.
4. Біохімічні аспекти використання деяких лікарських препаратів при азотемії.
Література
Основна:
1. Губський Ю. І. Біологічна хімія. – Київ-Тернопіль: Укрмедкнига, 2000. – 508 с.
2. Губський Ю. І. Біологічна хімія. – Київ-Вінниця: Новакнига, 2009. – С. 502 - 512.
3. Гонський Я.І., Максимчук Т.П. Біохімія людини. – Тернопіль: Укрмедкнига, 2001. – 736 с.
4. Гонський Я. І., Максимчук Т.П., Калинський М.І. Біохімія людини. – Тернопіль: Укрмедкнига, 2002. – 744 с.
5. Біологічна хімія. Тести та ситуаційні задачі. / За ред. О.Я. Склярова. – Львів: Світ, 2006. – 271 с.
6. Клінічна біохімія (лекції для студентів мед., стомат. та фарм. факультетів) / За ред. проф. Склярова О.Я. – Львів, 2004. – 295 с.
7. Практикум з біологічної хімії / За ред. О.Я. Склярова. – К.: Здоров’я, 2002. – 297 с.
Додаткова:
1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 1990. – 528 с.
2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 1998. – С. 567 – 598.
3. Бишевський А.Ш., Терсенов О.А., Біохімія для лікаря. – Київ, Укр. центр духовної культури, 2001. – 395 с.
4. Камышников В.С. Клинические лабораторные тесты от А до Я и их диагностические профили / МЕДпрессинформ – Москва, 2005. – 320 с.
5. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека. Т.2. – М.: Мир; Бином. Лаборатория знаний, 2009. – С. 319 – 331.
Тема № 5. Дослідження згортальної, антизгортальної та фібринолітичної систем крові. Дослідження біохімічних закономірностей реалізації імунних процесів. Імунодефіцитні стани.
Мета заняття: Знати роль компонентів згортальної, антизгортальної та фібринолітичної систем в підтриманні агрегатного стану крові. Давати характеристику біохімічним компонентам імунної системи, знати біохімічні механізми виникнення імунодефіцитних станів.
Актуальність теми: Згортання крові є складним фізіологічно-біохімічним процесом, захисною реакцією організму на крововтрату. Знання біохімічної характеристики згортальної, антизгортальної та фібринолітичної систем крові є необхідними для розуміння механізмів підтримання агрегатного стану крові за умов норми та при численних захворюваннях, а також для їх своєчасної корекції фармпрепаратами.
Конкретні завдання:
Ø Трактувати біохімічні механізми функціонування згортальної, антизгортальної та фібринолітичної систем крові.
Ø Оволодіти методами дослідження системи згортання крові та фібринолізу, вміти трактувати отримані результати.
Ø Знати роль компонентів загортальної, антизгортальної та фібринолітичної систем крові в патохімії синдрому дисемінованого внутрішньо судинного зсідання крові, атеросклерозу та гіпертонічної хвороби.
Ø Характеризувати клітинні та біохімічні компоненти імунної системи.
Ø Пояснювати механізми виникнення імунодефіцитних станів.
Теоретичні питання
1. Загальна характеристика системи гемостазу в організмі людини: судинно-тромбоцитарний і коагуляційний гемостаз.
2. Згортальна система крові; характеристика компонентів (факторів) згортання. Механізми активації та функціонування каскадної системи згортання крові; внутрішній та зовнішній шляхи коагуляції.
3. Роль вітаміну К у реакціях коагуляції (карбоксилування глутамінової кислоти, роль у зв’язуванні іонів кальцію). Лікарські засоби – агоністи та антагоністи вітаміну К.
4. Спадкові та набуті порушення судинно-тромбоцитарного та коагуляційного гемостазу.
5. Антизгортальна система крові, характеристика антикоагулянтів.
6. Фібринолітична система крові: етапи та компоненти фібринолізу. Лікарські засоби, що впливають на процеси фібринолізу. Активатори плазміногену та інгібітори плазміну.
7. Синдром дисемінованого внутрішньо судинного зсідання крові. Зсідання крові, тромбоутворення і фібриноліз при атеросклерозі та гіпертонічній хворобі.
8. Імуноглобуліни: структура, біологічні функції, механізми регуляції синтезу імуноглобулінів. Біохімічні характеристики окремих класів імуноглобулінів людини.
9. Медіатори та гормони імунної системи: інтерлейкіни, інтерферони, білково-пептидні фактори регуляції росту та проліферації клітин.
10. Біохімічні компоненти системи комплементу людини; класичний та альтернативний (пропердиновий) механізми активації.
11. Біохімічні механізми імунодефіцитних станів: первинні (спадкові) та вторинні імунодефіцити.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 935; Нарушение авторских прав?; Мы поможем в написании вашей работы!