
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электролиз и законы Фарадея
|
|
|
|
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
НА ЭЛЕКТРОДАХ
ЗАКОН ФАРАДЕЯ И ФАРАДЕЕВСКИЕ РЕАКЦИИ
Количественная связь между прошедшим через границу электрод – электролит электричеством и веществом, претерпевающим те или иные химические изменения на этой границе установлена М. Фарадеем и выражается законом, носящим его имя. Электродные реакции, подчиняющиеся закону Фарадея называются фарадеевскими.
Выделение вещества на электродах происходит в результате электролиза. Электролизом называется окислительно-восстановительный процесс, связанный с разложением вещества в результате прохождения постоянного электрического тока через растворы или расплавы электролитов.
Законами Фарадея называют законы электролиза, установленные им в тридцатых годах XIX века. Первый закон Фарадея может быть сформулирован следующим образом. Количество вещества m, образующегося в результате катодной или анодной реакции при электролизе, прямо пропорционально количеству электричества Q, прошедшему через электролизер:
m = kQ, (5.1)
где k – коэффициент пропорциональности, соответствующий количеству вещества, которое выделится при электролизе в расчете на единицу количества электричества. Эту величину называют электрохимическим эквивалентом вещества.
Количество электричества измеряется произведением силы тока I на время его прохождения t:
Q = I·t (5.2)
Единицей количества электричества является ампер-секунда (А∙с) или кулон (Кл). Если время измеряется в часах, то соответствующей единицей является ампер-час (А∙ч), равный 3600 Кл.
При прохождении через раствор электролита одного кулона электричества на электродах разряжаются 6,28∙1018 однозарядных ионов. Естественно, что на это требуется такое же количество электронов. Отсюда можно найти заряд электрона:
1/6,28∙1018=1.602∙10-19 Кл.
Подставив в равенство (1) значение Q, получим:
m = k·I·t. (5.3)
Второй закон Фарадея формулируется так. При затрате одинакового количества электричества количества веществ, образующихся при электролизе, пропорциональны их химическим эквивалентам 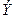 . Напомним: химическим эквивалентом простого или сложного вещества называют такое его количество, которое без остатка соединяется с 1 моль атомов водорода или замещает это же количество атомов водорода в химических реакциях.
. Напомним: химическим эквивалентом простого или сложного вещества называют такое его количество, которое без остатка соединяется с 1 моль атомов водорода или замещает это же количество атомов водорода в химических реакциях.
Для выделения одного эквивалента любого вещества потребуется затратить 6.02∙1023∙1.602∙10-19 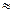 96500 Кл. Количество электричества, затрачиваемое на электролитическое выделение одного эквивалента любого вещества, составляет 96500 Кл и называется числом Фарадея. В соответствии с этим электрохимический эквивалент вещества может быть найден следующим образом:
96500 Кл. Количество электричества, затрачиваемое на электролитическое выделение одного эквивалента любого вещества, составляет 96500 Кл и называется числом Фарадея. В соответствии с этим электрохимический эквивалент вещества может быть найден следующим образом:
k = Э/96500. (5.4)
Подставив это значение в уравнение первого закона Фарадея, получим:
m = ItЭ/96500. (5.5)
Это выражение называют объединенным законом Фарадея. Оно отражает зависимость количества получающегося путем электролиза вещества от затраченного количества электричества и их химического эквивалента вещества.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 729; Нарушение авторских прав?; Мы поможем в написании вашей работы!