
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры решения задач. Пример 1. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй
|
|
|
|
Пример 1. Электрон в атоме водорода перешел с четвертого энергетического уровня на второй. Определить энергию испущенного при этом фотона.
Р е ш е н и е. Для определения энергии фотона воспользуемся сериальной формулой для водородоподобных ионов:
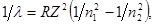 (1)
(1)
где l - длина волны фотона; R - постоянная Ридберга; Z - заряд ядра в относительных единицах (при Z = 1формула переходит в сериальную формулу для водорода); n1 - номер орбиты, на которую перешел электрон; n2 - номер орбиты, с которой перешел электрон (n1 и n2 - главные квантовые числа).
Энергия фотона e выражается формулой
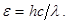
Поэтому, умножив обе части равенства (1) на hс, получим выражение для энергии фотона:
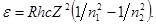
Так как Rhc есть энергия ионизации Eiатома водорода, то
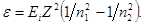
Вычисления выполним во внесистемных единицах: Ei = 13,6 эВ (см. табл. 1 Приложения); Z=1; n1=2; n2=4:
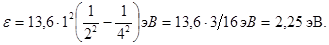
Пример 2. Электрон, начальной скоростью которого можно пренебречь, прошел ускоряющую разность потенциалов U. Найти длину волны де Бройля электрона для двух случаев: 1) U1 = 51 В; 2) U2 =510 кВ.
Р е ш е н и е. Длина волны де Бройля для частицы зависит от ее импульса pи определяется формулой
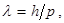 (1)
(1)
где h - постоянная Планка.
Импульс частицы можно определить, если известна ее кинетическая энергия T. Связь импульса с кинетической энергией различна для нерелятивистского случая (когда кинетическая энергия частицы много меньше ее энергии покоя) и для релятивистского случая (когда кинетическая энергия сравнима с энергией покоя частицы).
В нерелятивистском случае
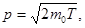 (2)
(2)
где m0 - масса покоя частицы.
В релятивистском случае
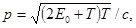 (3)
(3)
где E0 = m0c2 - энергия покоя частицы.
Формула (1) с учетом соотношений (2) и (3) запишется:
в нерелятивистском случае
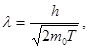 (4)
(4)
в релятивистском случае
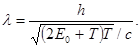 (5)
(5)
Сравним кинетические энергии электрона, прошедшего заданные в условии задачи разности потенциалов U1=51 В и U2=510кВ, с энергией покоя электрона и в зависимости от этого решим, какую из формул (4) или (5) следует применить для вычисления длины волны де Бройля.
Как известно, кинетическая энергия электрона прошедшего ускоряющую разность потенциалов U,

В первом случае T1 = eU = 51эВ = 0,51×10-4МэВ, что много меньше энергия покоя электрона Е0 = m0c2 = 0,51МэВ. Следовательно, в этом случае можно применить формулу (4). Для упрощения расчетов заметим, что Т1 = 10-4m0c2. Подставив это выражение в формулу (4), перепишем ее в виде

Учитывая, что h/m0c есть комптоновская длина волны L, получаем

Так как L = 2,43 пм (см. табл. 1 Приложения), то
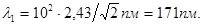
Во втором случае кинетическая энергия
T2 = eU2 = 510 кэВ = 0,51 МэВ, т.е. равна энергии покоя электрона. В этом случае необходимо применить релятивистскую формулу (5). Учитывая, что T2 = 0,51 МэВ= m0c2,по формуле (5) находим
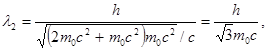
или

Подставим значение L и произведем вычисления:

Пример 3. Кинетическая энергия электрона в атоме водорода составляет величину порядка T = 10 эВ. Используя соотношение неопределенностей, оценить минимальные линейные размеры атома.
Р е ш е н и е. Соотношение неопределенностей для координаты и импульса имеет вид
 (1)
(1)
где Dx - неопределенность координаты частицы (в данном случае электрона); Dpx - неопределенность импульса частицы (электрона); 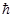 - постоянная Планка.
- постоянная Планка.
Из соотношения неопределенностей следует, что чем точнее определяется положение частицы в пространстве, тем более неопределенным становится импульс, а следовательно, и энергия частицы. Пусть атом имеет линейные размеры l, тогда электрон атома будет находиться где-то в пределах области с неопределенностью
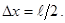
Соотношение неопределенностей (1) можно записать в этом случае в виде
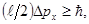
откуда
 (2)
(2)
Физически разумная неопределенность импульса Dpx во всяком случае не должна превышать значения самого импульса px,т.е. Dpx£px. Импульс px связан кинетической энергией Т соотношением 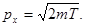 Заменим Dpxзначением
Заменим Dpxзначением  (такая замена не увеличит l). Переходя от неравенства к равенству, получим
(такая замена не увеличит l). Переходя от неравенства к равенству, получим
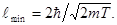 (3)
(3)
Проверим, дает ли полученная формула единицу длины. Для этого в правую часть формулы (3) вместо символов величин подставим обозначения их единиц:


Найденная единица является единицей длины.
Произведем вычисления:

Пример 4. Вычислить дефект массы и энергию связи ядра 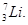
Р е ш е н и е. Масса ядра всегда меньше суммы масс свободных (находящихся вне ядра) протонов и нейтронов, из которых ядро образовалось. Дефект массы ядра Dm и есть разность между суммой масс свободных нуклонов (протонов и нейтронов) и массой ядра, т.е.
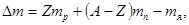 (1)
(1)
где Z - атомный номер (число протонов в ядре); A - массовое число (число нуклонов, составляющих ядро); mр, mn, mя- соответственно массы протона, нейтрона и ядра.
В справочных таблицах всегда даются массы нейтральных атомов, но не ядер, поэтому формулу (1) целесообразно преобразовать так, чтобы в нее входила масса mа нейтрального атома. Можно считать, что масса нейтрального атома равна сумме масс ядра и электронов, составляющих электронную оболочку атома: ma = mя + Zme, откуда
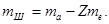 (2)
(2)
Выразив в равенстве (1) массу ядра по формуле (2), получаем
Dm =Zmp + (A - Z)mn - ma +Zme, или
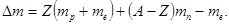
Замечая, что mp + me = mH, где mH - масса атома водорода, окончательно находим
 (3)
(3)
Подставив в выражение (3) числовые значения масс (см. табл. 13 и 15 Приложения), получим
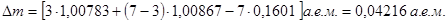
В соответствии с законом пропорциональности массы и энергии
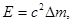 (4)
(4)
где с - скорость света в вакууме.
Коэффициент пропорциональности с2 может быть выражен двояко:
с2 = 9·1016 м2/с2, или с2 = DE/Dm = 9·1016 Дж/кг.
Если вычислить энергию связи, пользуясь внесистемными единицами, то с2 = 931МэВ/а.е.м. С учетом этого формула (4) примет вид
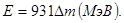 (5)
(5)
Подставив найденное значение дефекта массы ядра в формулу (5), получим
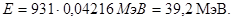
Примечание. Термин «дефект массы» часто применяют в другом смысле: дефектом массы D называют разность между массой нейтрального атома данного изотопа и его массовым числом A:
D = ma - A. Эта величина особого физического смысла не имеет, но ее использование позволяет в ряде случаев значительно упростить вычисления. В настоящем пособии всюду имеется в виду дефект массы Dm, определяемый формулой (1).
Пример 5. При соударении a - частицы с ядром бора 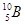 произошла ядерная реакция, в результате которой образовалось два новых ядра. Одним из этих ядер было ядро атома водорода
произошла ядерная реакция, в результате которой образовалось два новых ядра. Одним из этих ядер было ядро атома водорода 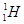 . Определить порядковый номер и массовое число второго ядра, дать символическую запись ядерной реакций и определить ее энергетический эффект.
. Определить порядковый номер и массовое число второго ядра, дать символическую запись ядерной реакций и определить ее энергетический эффект.
Р е ш е н и е. Обозначим неизвестное ядро символом  . Так как a-частица представляет собой ядро гелия
. Так как a-частица представляет собой ядро гелия 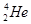 , запись реакции имеет вид
, запись реакции имеет вид

Применив закон сохранения числа нуклонов, получим уравнение
4 + 10 = 1 + A, откуда A = 13. Применив закон сохранения заряда, получим уравнение 2 + 5 = 1 + Z, откуда Z = 6. Следовательно, неизвестное ядро является ядром атома изотопа углерода 
Теперь можем записать реакцию в окончательном виде:

Энергетический эффект Qядерной реакции определяется по формуле

Здесь в первых круглых скобках указаны массы исходных ядер, во вторых скобках - массы ядер - продуктов реакции. При числовых подсчетах по этой формуле массы ядер заменяют массами нейтральных атомов. Возможность такой замены вытекает из следующих соображений.
Число электронов в электронной оболочке нейтрального атома равно его зарядовому числу Z. Сумма зарядовых чисел исходных ядер равна сумме зарядовых чисел ядер - продуктов реакции. Следовательно, электронные оболочки ядер гелия и бора содержат вместе столько же электронов, сколько их содержат электронные оболочки ядер углерода и водорода.
Очевидно, что при вычитании суммы масс нейтральных атомов углерода и водорода из суммы масс атомов гелия и бора массы электронов выпадут и мы получим тот же результат, как если бы брали массы ядер. Подставив массы атомов (см. Табл. 13 Приложения) в расчетную формулу, получим

Пример 6. Определить начальную активность A0 радиоактивного препарата магния 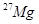 массой m = 0,2 мкг, а также его активность Aчерез время t = 6ч. Период полураспада T1/2 магния считать известным.
массой m = 0,2 мкг, а также его активность Aчерез время t = 6ч. Период полураспада T1/2 магния считать известным.
Р е ш е н и е. Активность Aизотопа характеризует скорость радиоактивного распада и определяется отношением числа dN ядер, распавшихся за интервал времени dt, к этому интервалу:
 (1)
(1)
Знак «-» показывает, что число N радиоактивных ядер с течением времени убывает.
Для того чтобы найти dN/dt,воспользуемся законом радиоактивного распада:
 (2)
(2)
где N - число радиоактивных ядер, содержащихся в изотопе, в момент времени t; N0 - число радиоактивных ядер в момент времени, принятый за начальный (t = 0); l - постоянная радиоактивного распада.
Продифференцируем выражение (2) по времени:
 (3)
(3)
Исключив из формул (1) и (3) dN/dt, находим активность препарата в момент времени t:
 (4)
(4)
Начальную активность A0препарата получим при t=0:
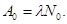 (5)
(5)
Постоянная радиоактивного распада l связана с периодом полураспада T1/2 соотношением
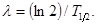 (6)
(6)
Число N0 радиоактивных ядер, содержащихся в изотопе, равно произведению постоянной Авогадро NA на количество вещества n данного изотопа:
 (7)
(7)
где m- масса изотопа; M- молярная масса.
С учетом выражений (6) и (7) формулы (5) и (4) принимают вид
 (8)
(8)
 (9)
(9)
Произведем вычисления, учитывая, что T1/2 = 10 мин = 600 с (см. табл. 14 Приложения), 1n2 = 0,693, t = 6ч = 6×3,6×103с = 2,16. 104с:


Пример 7. Вычислить максимальную энергию eF (энергию Ферми), которую могут иметь свободные электроны в металле (медь) при температуре T=0 К. Принять, что на каждый атом меди приходится по одному валентному электрону.
Р е ш е н и е. Максимальная энергия eF, которую могут иметь электроны в металле при T=0К, связана с концентрацией свободных электронов соотношением
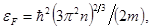 (1)
(1)
где  - постоянная Планка; m - масса электрона.
- постоянная Планка; m - масса электрона.
Концентрация свободных электронов по условию задачи равна концентрации атомов, которая может быть найдена по формуле
 (2)
(2)
где r - плотность меди; NA - постоянная Авогадро; M- молярная масса.
Подставляя выражение nв формулу (1), получаем

Произведем вычисления:
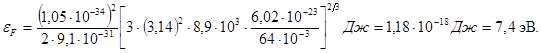
Пример 8. Кремниевый образец нагревают от температуры t1=0°С до температуры t2=10°С. Во сколько раз возрастает его удельная проводимость?
Р е ш е н и е. Удельная проводимость g собственных полупроводников связана с температурой Tсоотношением
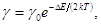
где g0 - константа; DE- ширина запрещенной зоны.
Следовательно,
 '
'
Полагая для кремния DE= 1,1 эВ, произведем вычисления:
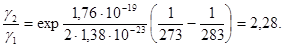
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 5738; Нарушение авторских прав?; Мы поможем в написании вашей работы!