
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинаміка реакцій утворення і дисоціації оксидів металів
|
|
|
|
У загальному вигляді реакція утворення оксиду для двовалентного металу має вигляд:
2Ме + О2 = 2МеО + Q, а реакція дисоціації 2МеО = 2Ме + О2, константа рівноваги якої
Кp =  .
.
Коли тверді або рідкі фази не утворюють між собою розчинів і не розчинені в інших речовинах, наприклад в шлаку або в металі, тобто знаходяться в чистому вигляді, то їх активності а Ме і а МеО рівні 1, а Кp = 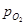 . Величина
. Величина 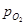 – рівноважний парціальний тиск кисню при даній температурі для даного оксиду називається пружністю дисоціації даного оксиду. Чим менше величина пружності дисоціації і менше величина Δ G 0 реакції утворення оксиду, тим міцніше даний оксид. Пружність дисоціації і величина Δ G 0 служать мірою спорідненості металу до кисню. Зменшення пружності дисоціації, так само як і зменшення Δ G 0, сприяє підвищенню спорідненості металу до кисню.
– рівноважний парціальний тиск кисню при даній температурі для даного оксиду називається пружністю дисоціації даного оксиду. Чим менше величина пружності дисоціації і менше величина Δ G 0 реакції утворення оксиду, тим міцніше даний оксид. Пружність дисоціації і величина Δ G 0 служать мірою спорідненості металу до кисню. Зменшення пружності дисоціації, так само як і зменшення Δ G 0, сприяє підвищенню спорідненості металу до кисню.
Напрям процесу, тобто здійснення реакції дисоціації або утворення оксиду залежить від співвідношення рівноважного значення 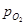 і фактичного парціального тиску кисню в газовій фазі, відповідно до рівняння Вант-Гоффа для реакції дисоціації
і фактичного парціального тиску кисню в газовій фазі, відповідно до рівняння Вант-Гоффа для реакції дисоціації 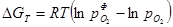 .
.

|
| Рис. 2.2 – Дисоціація оксидів залежно від температури |
На рис. 2.2 приведена залежність пружності дисоціації від температури 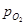 = f (T). В області I над кривою завжди
= f (T). В області I над кривою завжди  >
> 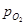 , внаслідок чого Δ G 0 > 0 і в цій області відбуватиметься утворення оксиду. В області II нижче за криву
, внаслідок чого Δ G 0 > 0 і в цій області відбуватиметься утворення оксиду. В області II нижче за криву  <
< 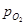 то Δ G 0 < 0 і відбуватиметься дисоціація оксиду.
то Δ G 0 < 0 і відбуватиметься дисоціація оксиду.
Дана двокомпонентна (Me – О) система складається з трьох фаз – двох твердих і однієї газоподібної. Тому за правилом фаз Гіббса С = К – Ф + 2 = 2 – 3 + 2 = 1.
Таким чином, кожній температурі відповідає певний тиск кисню, оскільки система має тільки один ступінь свободи.
На рис. 2.3 представлена залежність Δ G 0 реакцій утворення оксидів від температури. Елементи Cu, Ni, Co, Fe, Cr, Mn, V, Si, Ti, Al, Mg, Ca розташовані в порядку зростання їх спорідненості до кисню і збільшення міцності їх оксидів, що підтверджується зменшенням величини Δ G 0.

|
| Рис. 2.3 - Залежність зміни стандартних вільних енергій утворення оксидів металів від температури (на 1моль/О2). Температура фазових перетворень для металів: плавлення - П, кипіння - К, сублімація - С. Позначення для фазових перетворень оксидів узяті в рамку |
З підвищенням температури пружність дисоціації оксидів збільшується, а їх міцність відповідно зменшується. Проте, тільки у вуглецю із зростанням температури збільшується спорідненість до кисню, тому вуглець є універсальним відновником. З одного боку, із зростанням температури міцність оксидів падає, з другого боку спорідненість вуглецю до кисню зростає.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 686; Нарушение авторских прав?; Мы поможем в написании вашей работы!