
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Распределение Больцмана
|
|
|
|
До сих пор рассматривалось поведение идеального газа, не подверженного воздействию внешних силовых полей. Из опыта хорошо известно, что при действии внешних сил равномерное распространение частиц в пространстве может нарушиться. Так под действием силы тяжести молекулы стремятся опуститься на дно сосуда. Интенсивное тепловое движение препятствует осаждению, и молекулы распространяются так, что их концентрация постепенно уменьшается по мере увеличения высоты.
Выведем закон изменения давления с высотой предполагая, что поле тяготения однородно, температура постоянна и масса всех молекул одинакова. Если атмосферное давление на высоте h равно p, то на высоте h + dh оно равно p + dp (при dh > 0, dp < 0, так как p уменьшается с увеличением h).
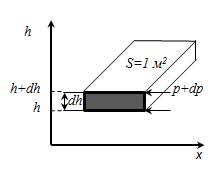 Разность давления на высотах h и h+dh мы можем определить как вес молекул воздуха заключённого в объёме с площадью основания равного 1 и высотой dh.
Разность давления на высотах h и h+dh мы можем определить как вес молекул воздуха заключённого в объёме с площадью основания равного 1 и высотой dh.
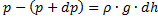
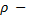 плотность на высоте h, и так как
плотность на высоте h, и так как 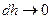 , то
, то 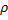 = const.
= const.
Тогда 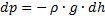
Из уравнения Менделеева-Клапейрона.

Тогда
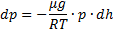
Или
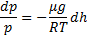
С изменением высоты от h1 до h2 давление изменяется от p1 до p2
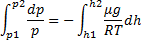
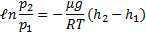
Пропотенцируем данное выражение (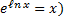
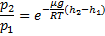
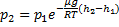
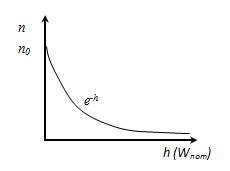
Барометрическая формула, показывает, как меняется давление с высотой
При 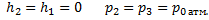
Тогда

Т.к.
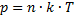 ,
,
а
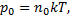
то
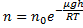
n 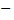 концентрация молекул на высоте h,
концентрация молекул на высоте h,
n0 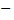 концентрация молекул на высоте h =0.
концентрация молекул на высоте h =0.
Т.к
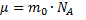
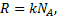
то
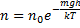
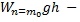 потенциальная энергия молекул в поле тяготения
потенциальная энергия молекул в поле тяготения
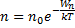
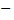 распределение Больцмана во внешнем потенциальном поле. Из него следует, что при T = const плотность газа больше там, где меньше потенциальная энергия молекул.
распределение Больцмана во внешнем потенциальном поле. Из него следует, что при T = const плотность газа больше там, где меньше потенциальная энергия молекул.
24.Реальный газ — газ, который не описывается уравнением состояния идеального газа Клапейрона — Менделеева.
Зависимости между его параметрами показывают, что молекулы в реальном газе взаимодействуют между собой и занимают определенный объём. Состояние реального газа часто на практике описывается обобщённым уравнением Менделеева — Клапейрона:
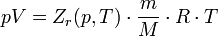
где p — давление; V — объем; T — температура; Zr = Zr (p,T) — коэффициент сжимаемости газа; m — масса; М — молярная масса; R — газовая постоянная.Также существует такое понятие как критическая температура, если газ находится при температуре выше критической (индивидуальна для каждого газа, например для углекислого газа примерно 304 К), то его уже невозможно превратить в жидкость, какое бы давление к нему не прилагалось. Данное явление возникает вследствие того, что при критической температуре силы поверхностного натяжения жидкости равны нулю. Если продолжать медленно сжимать газ при температуре большей критической, то после достижения им объёма, равного приблизительно четырем собственным объёмам молекул, составляющих газ, сжимаемость газа начинает резко падать.
25. Фазовые переходы. Фазовые переходы 1 и 2 рода. Диаграммы состояния вещества. Тройная точка. Классификация фазовых переходов При фазовом переходе первого рода скачкообразно изменяются самые главные, первичные экстенсивные параметры: удельный объём (т.е. плотность), количество запасённой внутренней энергии, концентрация компонентов и т. п. Подчеркнём: имеется в виду скачкообразное изменение этих величин при изменении температуры, давления и т. п., а не скачкообразное изменение во времени (насчёт последнего см. ниже раздел Динамика фазовых переходов). Наиболее распространённые примеры фазовых переходов первого рода: плавление и затвердевание, кипение и конденсация, сублимация и десублимация При фазовом переходе второго рода плотность и внутренняя энергия не меняются, так что невооружённым глазом такой фазовый переход может быть незаметен. Скачок же испытывают их вторые производные по температуре и давлению: теплоёмкость, коэффициент теплового расширения, различные восприимчивости и т. д. Фазовые переходы второго рода происходят в тех случаях, когда меняется симметрия строения вещества.
Тройная точка — точка на фазовой диаграмме, где сходятся три линии фазовых переходов. Тройная точка — это одна из характеристик химического вещества. Обычно тройная точка определяется значением температуры и давления, при котором вещество может равновесно находится в трёх (отсюда и название) агрегатных состояниях — твёрдом, жидком и газообразном. В этой точке сходятся линии плавления, кипения и сублимации.
ДИАГРАММА СОСТОЯНИЯ(фазовая диаграмма) - диаграмма, изображающая зависимость устойчивого фазового состояния одно- или многокомпонентного вещества от термодинамич. параметров, определяющих это состояние (темп-ры T, давления P, напряжённостей магн. H или электрич. E полей, концентрации с и др.). Каждая точка Д. с. (фигуративная точка) указывает на фазовый состав вещества при заданных значениях термодинамич. параметров (координатах этой точки). В зависимости от числа внеш. параметров Д. с. может быть двумерной, трёхмерной и многомерной. При исследовании равновесия фаз в условиях перем. давления строят изобарич. и изоконцентрац. сечения и проекции на плоскости T-P или Р-с. Наиб. полно изучены изобарич. Т-с сечения Т-Р-с Д. с., соответствующие атм. давлению.
26. Особенности поверхностного слоя жидкости. Коэффициент поверхностного натяжения.
Молекулы вещества в жидком состоянии расположены почти вплотную друг к другу. В отличие от твердых кристаллических тел, в которых молекулы образуют упорядоченные структуры во всем объеме кристалла и могут совершать тепловые колебания около фиксированных центров, молекулы жидкости обладают большей свободой. Каждая молекула жидкости, также как и в твердом теле, «зажата» со всех сторон соседними молекулами и совершает тепловые колебания около некоторого положения равновесия. Однако, время от времени любая молекула может переместиться в соседнее вакантное место. Такие перескоки в жидкостях происходят довольно часто; поэтому молекулы не привязаны к определенным центрам, как в кристаллах (см. §3.6), и могут перемещаться по всему объему жидкости. Этим объясняется текучесть жидкостей. Из-за сильного взаимодействия между близко расположенными молекулами они могут образовывать локальные (неустойчивые) упорядоченные группы, содержащие несколько молекул. Это явление называется ближним порядком.
Пове́рхностное натяже́ние — термодинамическая характеристика поверхности раздела двух находящихся в равновесиифаз, определяемая работой обратимого изотермокинетического образования единицы площади этой поверхности раздела при условии, что температура, объём системы и химические потенциалы всех компонентов в обеих фазах остаются постоянными.Поверхностное натяжение имеет двойной физический смысл — энергетический (термодинамический) и силовой (механический). Энергетическое (термодинамическое) определение: поверхностное натяжение — это удельная работа увеличения поверхности при её растяжении при условии постоянства температуры. Силовое (механическое) определение: поверхностное натяжение — это сила, действующая на единицу длины линии, которая ограничивает поверхность жидкости.
|
|
|
|
|
Дата добавления: 2014-11-08; Просмотров: 713; Нарушение авторских прав?; Мы поможем в написании вашей работы!