
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма
|
|
|
|
При взаимодействии токсиканта с биологическими структурами-мишенями могут образовываться различные типы химических связей (таблица 3).
Таблица 3. различные типы связей, формирующихся между токсикантами и молекулами-мишенями организма
| Вид связи | Пример | Энергия связи (кдж/мол) |
| Ионная | 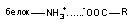
| |
| Ковалентная | 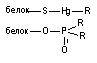
| 40 - 600 |
| Донорно-акцепторная | 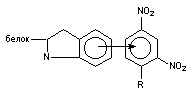
| 4 - 20 |
| Ион-дипольная | 
| 8 - 20 |
| Диполь-дипольная | 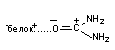
| 4 - 12 |
| Водородная | 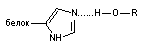
| 4 - 28 |
| Ван-дер-Ваальса | 
| 1 - 4 |
| Гидрофобная | 
| 1 - 6 |
Ионная связь. В водных растворах многие вещества диссоциируют с образованием ионов. Между положительно и отрицательно заряженными ионами токсиканта и эндогенными ионами-мишенями начинают действовать силы электростатического притяжения. Вследствие притяжения возникает химическая связь. Связь такого типа называется электровалентной или ионной. Образованные катионами и анионами вещества не несут электрического заряда.
А- + В+  АВ
АВ
Токсические последствия подобного взаимодействия в организме развиваются в случае образования не растворимого в воде комплекса иона-токсиканта с биологически значимым ионом-мишенью. Например, при интоксикации фторидами, ион фтора может вступать во взаимодействие с ионом кальция. В итоге образуется нерастворимый фторид кальция. Развивающаяся гипокальциемия имеет определенное значение для развития и проявления интоксикации. Аналогичным образом действует щавелевая кислота, образующаяся в организме в процессе метаболизма этиленгликоля при интоксикации последним:
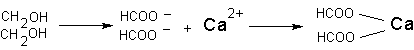
Поскольку степень диссоциации многих веществ в водном растворе существенно зависит от рН среды, количество образовавшихся за счет ионной связи комплексов токсикант-мишень также зависит от этого показателя.
Ковалентная связь. Для образования ковалентной связи, взаимодействующие атомы должны иметь на внешней электронной орбите неспаренные электроны. Эти электроны занимают одну и ту же орбиталь, а образовавшаяся общая пара формирует силу притяжения между атомами. В результате образования такой общей пары электронов каждый из взаимодействующих атомов приобретает "завершенный набор" электронов и образовавшееся соединение становится стабильным. Энергия ковалентной связи велика и составляет 200 - 400 кдж/мол
Высокая стабильность связи этого типа означает практически необратимый характер присоединения токсиканта к структуре-мишени. Примерами веществ, образующих с биомолекулами подобную связь, являются ФОС (взаимодействуют с серином, входящим в структуру активного центра ацетилхолинэстеразы), иприты (взаимодействуют с пуриновыми основаниями нуклеиеновых кислот), а также целый ряд других распространённых токсикантов (метилбромид, метилхлорид, этиленоксид и др.). Вследствие прочности образовавшейся связи, разрушение комплекса токсикант-биомишень возможно только с помощью специальных средств (например, реактиваторов ХЭ при интоксикации ФОС). Восполнение содержания поврежденной токсикантом биологической структуры возможно также за счет синтеза её de novo. Так, восстановление активности АХЭ в тканях лабораторных животных отравленных зоманом проходит со скоростью синтеза энзима нервными клетками.
Координационная связь - это ковалентная связь, в которой обобществленною пару электронов предоставляет только один из участвующих в связи атомов. Один из атомов является донором, а другой акцептором электронной пары, поэтому эту связь называют также донорно-акцепторной. Акцепторами часто являются катионы металлов, или атомы переходных металлов (Zn, Cu, Fe), входящих в состав молекулы. Таким образом, в частности, оксид углерода взаимодействует с железом гемоглобина, с образование карбоксигемоглобина.
Водородная связь. Ковалентная связь между атомом водорода и электроотрицательным атомом (кислород, азот, сера и т.д.) более или менее поляризована
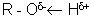
Вследствие этого атом водорода приобретает незначительный положительный заряд. Если в близи такого атома находится молекула или группа, содержащая анион или электроотрицательный атом, между ними образуется слабая связь, называемая водородной.
Водородная связь может образовываться как между молекулами, так и между атомами внутри молекул. Энергия связи не велика и в водном растворе составляет около 20 кдж/мол. Её прочность во многом зависит от строения взаимодействующих веществ, в частности, от степени электроотрицательности атомов, связанных с водородом. Электроотрицательность атомов возрастает в ряду:
Н = P < C = S = I < Br < Cl = N < O < F
2,1 2,1 2,5 2,5 2,5 2,8 3,0 3,0 3,4 4,0
Водородные связи имеют очень большое значение для поддержания пространственной структуры белков, нуклеиновых кислот и других высокомолекулярных соединений. Вещества, способные разрушать водородную связь, могут нарушать пространственную структуру макромолекул (явление интерколации: встраивание молекул акридина, этидиумбромида между плоскостями, образуемыми витками спирали молекулы ДНК).
В состав молекул токсикантов также входят группы, способные участвовать в образовании водородных связей. Если эти группы (Х-Н) являются структурными элементами "активного" радикала токсиканта, то они участвуют в образовании сложной связи вещества с молекулой-мишенью. Поскольку водородные связи являются по сути электростатическими, их сила ослабевает в присутствии веществ, обладающих свойствами диэлектриков ("неэлектролитов").
Связи Ван-дер-Ваальса. Форма электронного облака молекул квазистабильна, то есть не изменяется до тех пор, пока на неё не действуют внешние силы. Под влиянием электромагнитных полей электронные облака молекул деформируются. При этом безразлично вызвано ли появление деформируящих сил воздействием внешних полей или поле сформировано близлежащими ионами, диполями, аполярными молекулами. Степень деформированности электронного облака зависит от энергетических характеристик воздействующих полей и поляризуемости самой молекулы. Способность электронного облака к деформации (поляризуемость) зависит от размеров молекулы. У больших молекул она больше, чем у малых, поскольку сместить электроны, находящиеся на значительном удалении от ядра атома, легче.
Деформирующее воздействие полей превращает неполярные молекулы в диполи, так как центры максимальной плотности положительного и отрицательного зарядов молекулы несколько разъединяются в пространстве. Сформировавшийся диполь называют индуцированным или временным, поскольку он перестает существовать сразу после прекращения действия деформирующих сил. Две близлежащие неполярные молекулы могут взаимно индуцировать образование временных диполей и, таким образом взаимодействовать друг с другом. Силы взаимодействия, формирующиеся между временными диполями, называются силами Лондона - Ван-дер-Ваальса. Энергия образующейся связи мала, однако она существенно возрастает при увеличении числа участков контакта между взаимодействующими молекулами. Со стороны токсиканта это могут быть ароматические, гетероциклические, алкильные радикалы; со стороны рецептора - неполярные участки молекул аминокислот (лейцин, валин, аланин, пролин и др.). Вклад каждой -СН2- группы алкильной цепи во взаимодействие оценивается в 2 - 4 кдж/мол. При тесном контакте больших неполярных молекул энергия связи может достичь очень больших величин. Поэтому при образовании комплекса токсикант-биомишень силы Ван-дер-Ваальса могут обеспечивать очень прочную фиксацию ксенобиотика. Действующая сила, ответственная за формирование связи, обратно пропорциональна седьмой степени расстояния между взаимодействующими молекулами. Поэтому она не может обеспечить притяжение молекул токсиканта, свободно циркулирующих в биосредах, к рецептору. В этом процессе первостепенную роль играют силы электростатического взаимодействия. Однако после того как контакт между токсикантом и рецептором осуществился силы Ван-дер-Ваальса обеспечивают его ориентацию и плотную фиксацию.
Гидрофобное взаимодействие. Гидрофобные связи формируются в водной среде, когда молекулы взаимодействующих веществ контактируют друг с другом неполярными (гидрофобными) участками. В отличии от взаимодействия Ван-дер-Ваальса и донорно-акцепторного взаимодействия, которые также формируются при взаимодействии неполярных групп, образование гидрофобных связей обусловлено свойствами воды, без участия которой взаимодействие происходить не может. В соответствии с теорией, молекулы воды связаны друг с другом водородными связями, образуя трехмерную структуру (кластер), напоминающую структуру льда. На границе поверхности, разделяющей неполярную молекулу и молекулы воды, образование такой структуры затрудняется. При контакте двух неполярных молекул, растворенных в воде, общая площадь поверхности, разделяющей воду и эти молекулы уменьшается. Вследствие этого, мобилизуется часть молекул воды, организованных в кластер. В противоположность всем другим химическим связям и взаимодействиям гидрофобная связь, таким образом, обусловлена преобразованием растворителя (воды), а не растворенных взаимодействующих веществ. Движущей силой образования связи является рост энтропии целостной системы растворитель - растворенные молекулы. Структурная организация гидрофобных, взаимодействующих молекул возрастает (уменьшение энтропии), но при этом существенно дезорганизуется (энтропия возрастает) структура растворителя (воды).
Гидрофобные связи имеют большое значение при взаимодействии неполярных молекул ксенобиотиков с клеточными и внутриклеточными мембранами, для образования их комплексов с белками, при этом возможно нарушение конформации макромолекул.
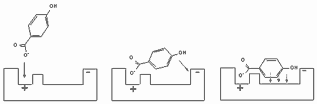
В процессе взаимодействия низкомолекулярного вещества с биомишенью практически всегда формируется несколько типов связей (рисунок 3), поскольку молекула токсиканта, как правило, включает полярный (иногда даже ионизированный), и неполярный фрагменты.

|
 + Щелкните для загрузки увеличенной копии (2,74кб, 528x174 GIF) + Щелкните для загрузки увеличенной копии (2,74кб, 528x174 GIF)
|
| Рисунок 3. Этапы взаимодействия молекулы токсиканта с биомишенью |

|
Ионные связи, за счет которых осуществляется притяжение молекулы к биомишени, мало специфичны (аналогично ион-дипольному и диполь-дипольному взаимодействию). Взаимодействие между неполярными группами также неспецифично. Однако, если в структуре мишени (например, рецепторе для эндогенных биорегуляторов) полярные и неполярные группы пространственно организованы, между этими участками и особыми участками молекулы токсиканта образуются специфичные связи, обусловленные пространственной организацией молекулы токсиканта. Такое взаимодействие можно сравнить с ориентацией намагниченных стрелок в магнитном поле. После ориентации молекулы с помощью ионного (диполь-дипольного) взаимодействия между ней и рецептором формируется тесный контакт, и образуются связи за счет водородных сил и сил Ван-дер-Ваальса. Образующийся комплекс тем более прочен, чем более комплементарна молекула токсиканта рецептору.
РАЗДЕЛ 2. ТОКСИКОДИНАМИКА
ГЛАВА 2.1. МЕХАНИЗМЫ ТОКСИЧЕСКОГО ДЕЙСТВИЯ
Взаимодействие токсиканта или продуктов его превращения в организме со структурными элементами биосистем, лежащее в основе развивающегося токсического процесса, называется механизмом токсического действия. Взаимодействие осуществляется за счет физико-химических и химических реакции.
Токсический процесс, инициируемый физико-химическими реакциями, как правило, обусловлен растворением токсиканта в определенных средах (водной или липидной) клеток и тканей организма. При этом существенно изменяются физико-химические свойства среды-растворителя (рН, вязкость, электропроводность, сила межмолекулярных взаимодействий и т.д.). Особенность данного типа взаимодействия - отсутствие строгой зависимости качества развивающегося эффекта от химических свойств молекулы токсиканта. Таким образом, действуют на ткани все кислоты, щелочи, сильные окислители, некоторые органические растворители и лишенные специфической активности высокомолекулярные соединения.
Чаще в основе токсического действия лежат химические реакции токсиканта с определенным структурным элементом живой системы. Структурный компонент биологической системы, с которым вступает в химическое взаимодействие токсикант, называется его "рецептором" или "мишенью".
Механизмы токсического действия подавляющего большинства химических веществ в настоящее время неизвестны. В этой связи, очень многие описываемые ниже классы молекул и молекулярных комплексов, образующих организм, рассматриваются, по большей части, лишь как вероятные рецепторы (мишени) действия ядов. Рассмотрение их в этом ракурсе правомочно, поскольку в основе действия некоторых хорошо изученных токсикантов лежит взаимодействие с представителями именно этих классов биомолекул.
1. Определение понятия "рецептор" в токсикологии
Понятие "рецептор" весьма емкое. Наиболее часто в биологии его используют в следующих смыслах:
1. Общее понятие. Рецепторы - это участки относительно специфического связывания на биосубстрате ксенобиотиков (или эндогенных молекул), при условии, что процесс связывания подчиняется закону действующих масс. В качестве рецепторов могут выступать целые молекулы белков, нуклеиновых кислот, полисахаридов, липидов или их фрагменты. В отношении фрагмента биомолекулы, которая непосредственно участвует в образовании комплекса с химическим веществом, часто используют термин - "рецепторная область". Например, рецептором оксида углерода в организме является молекула гемоглобина, а рецепторной областью - ион двухвалентного железа, заключенный в порфириновое кольцо гема.
2. Селективные рецепторы. По мере эволюционного усложнения организмов формируются специальные молекулярные комплексы - элементы биологических систем, обладающие высоким сродством к отдельным химическим веществам, выполняющим функции биорегуляторов (гормоны, нейромедиаторы и т.д.). Участки биологических систем, обладающие наивысшим сродством к отдельным специальным биорегуляторам, получили название "селективные рецепторы". Вещества, взаимодействующие с селективными рецепторами в соответствии с законом действующих масс, называются лигандами селективных рецепторов. Взаимодействие эндогенных лигандов с селективными рецепторами имеет особое значение для поддержания гомеостаза.
Многие селективные рецепторы состоят из нескольких субъединиц, из которых лишь часть имеет участки связывания лигандов. Нередко термин "рецептор" используют для обозначения только таких лиганд-связывающих субъединиц.
3. Постоянные рецепторы - это селективные рецепторы, строение и свойства которых кодируется с помощью специальных генов или постоянных генных комплексов. На уровне фенотипа изменение рецептора путем генной рекомбинации развивается чрезвычайно редко. Возникающие порой в ходе эволюции вследствие полигенетических трансформаций изменения аминокислотного состава белка, формирующего селективный рецептор, как правило, слабо сказывается на функциональных характеристиках последнего, его сродстве к эндогенным лигандам и ксенобиотикам.
К числу постоянных рецепторов относятся:
- рецепторы нейромедиаторов и гормонов. Как и другие селективные рецепторы, эти рецепторы способны избирательно взаимодействовать и с некоторыми ксенобиотиками (лекарствами, токсикантами). Ксенобиотики могут при этом выступать как в качестве агонистов, так и антагонистов эндогенных лигандов. В итоге активируется или подавляется некая биологическая функция, находящаяся под контролем данного рецепторного аппарата;
- энзимы - белковые структуры, селективно взаимодействующие с субстратами, превращение которых они катализируют. Энзимы также могут взаимодействовать с чужеродными веществами, которые в этом случае становятся либо ингибиторами, либо аллостерическими регуляторами их активности;
- транспортные протеины - избирательно связывают эндогенные лиганды определенного строения, осуществляя их депонирование или перенос через различные биологические барьеры. Токсиканты, взаимодействующие с транспортными протеинами, также выступают либо в качестве их ингибиторов, либо аллостерических регуляторов.
4. Рецепторы с изменяющейся структурой. В основном это антитела и антигенсвязывающие рецепторы Т-лимфоцитов. Рецепторы данного типа формируются в клетках предшественниках зрелых клеточных форм вследствие индуцированной внешними воздействиями рекомбинации 2 - 5 генов, контролирующих их синтез. Если рекомбинация осуществилась в процессе дифференциации клеток, то в зрелых элементах будут синтезироваться рецепторы только определенного строения. Таким способом формируются селективные рецепторы к конкретным лигандам, а пролиферация приводит к появлению целого клона клеток, содержащих эти рецепторы.
Как следует из приведенных определений, в биологии термин "рецептор" в основном используется для обозначения структур, принимающих непосредственное участие в восприятии и передаче биологических сигналов, и способных избирательно связывать помимо эндогенных лигандов (нейромедиаторов, гормонов, субстратов) некоторые чужеродные соединения.
В токсикологии (как и фармакологии) термином "рецептор" обозначают любой структурный элемент живой (биологической) системы, с которым вступает в химическое взаимодействие токсикант (лекарство). В таком прочтении это понятие ввел в химеобиологию в начале ХХ века Пауль Эрлих (1913).
Спектр энергетических характеристик рецептор-лигандного взаимодействия необыкновенно широк: от формирования слабых, легко разрушающихся связей, до образования необратимых комплексов (см. выше). Характер взаимодействия и структура сформировавшегося комплекса зависят не только от строения токсиканта, конформации рецептора, но и от свойств среды: рН, ионной силы и т.д. В соответствии с законом действующих масс, количество образовавшихся комплексов вещество-рецептор определяется энергией взаимодействия (сродством) и содержанием обоих компонентов реакции (вещества и рецептора к нему) в биологической системе.
Рецепторы могут быть "немыми" и активными. "Немой" рецептор - структурный компонент биологической системы, взаимодействие которого с веществом не приводит к формированию ответной реакции (например, связывание мышьяка белками, входящими в состав волос, ногтей). Активный рецептор - структурный компонент биологической системы, взаимодействие которого с токсикантом инициирует токсический процесс. Для того, чтобы избежать терминологических трудностей, для обозначения структурных элементов, взаимодействуя с которыми токсикант инициирует токсический процесс, вместо термина "рецептор", часто используют термин "структура-мишень".
Принимаются постулаты:
- токсическое действие вещества выражено тем сильнее, чем большее количество активных рецепторов (структур-мишеней) вступило во взаимодействие с токсикантом;
- токсичность вещества тем выше, чем меньшее его количество связывается с "немыми" рецепторами, чем эффективнее оно действует на активный рецептор (структуру-мишень), чем большее значение имеет рецептор и повреждаемая биологическая система для поддержания гомеостаза целостного организма.
Любая клетка, ткань, орган содержат огромное количество потенциальных рецепторов различных типов ("запускающих" различные биологические реакции), с которыми могут вступить во взаимодействие лиганды. С учетом вышесказанного, связывание лиганда (как эндогенного вещества, так и ксенобиотика) на рецепторе данного типа является избирательным лишь в определенном диапазоне концентраций. Увеличение концентрации лиганда в биосистеме приводит к расширению спектра типов рецепторов, с которыми он вступает во взаимодействие, а следовательно, изменению его биологической активности. Это также одно из фундаментальных положений токсикологии, доказанное многочисленными наблюдениями.
Мишенями (рецепторами) для токсического воздействия могут быть:
- структурные элементы межклеточного пространства;
- структурные элементы клеток организма;
- структурные элементы систем регуляции клеточной активности.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 1015; Нарушение авторских прав?; Мы поможем в написании вашей работы!