
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Метали в природі. Загальні способи добування металів
|
|
|
|
У вільному стані в природі зустрічаються тільки неактивні метали. Так у вигляді самородків зустрічаються золото й платина, іноді – срібло й мідь. Добування цих металів пов’язане лише з механічним відокремленням їх від домішок. Більшість металічних елементів легко окиснюються й існують в природі тільки у сполуках: оксидах (Fe3O4, Cr2O3), сульфідах (FeS2, ZnS), солях (NaCl, CaCO3). Саме з таких природних сполук і добувають метали шляхом їх хімічної переробки.
Природні мінеральні сполуки, з яких економічно доцільно видобувати метал у виробничих умовах називають рудами. Найважливішими рудами є оксиди, сульфіди і карбонати металічних елементів. Першим етапом переробки руд є видалення пустої породи — збагачення руди. Добування металів із руд ґрунтується на їх відновленні різними способами.
Найважливіший спосіб одержання металів із руд — відновлення оксидів відповідних металічних елементів вугіллям (коксом) при нагріванні:
SnO2 + C = Sn + CO2.
Досить часто оксидні руди відновлюють карбон(ІІ) оксидом, а інколи — воднем:
Fe2O3 + 3CO = 2Fe + 3CO2
WO3 + 3H2 = W + 3H2O.
Сульфідні руди спочатку випалюють, а потім відновлюють одержаний оксид:
2PbS + 3O2 = 2PbO + 2SO2
PbO + C = Pb + CO.
Важливим методом добування металів є відновлення менш активних металів активнішими металами і деякими неметалами при нагріванні. Відновлення алюмінієм називають алюмінотермією, відновлення магнієм — магнієтермією, силіцієм — силікотермією:
Fe2O3 + 2Al = 2Fe + Al2O3.
Зонна плавка (зонна перекристалізація) - метод очищення твердих речовин, заснований на різній розчинності домішок в твердій і рідкій фазах. Метод є різновидом спрямованої кристалізації, від якої відрізняється тим, що в кожний момент часу розплавленої є деяка невелика частина зразка. Така розплавлена зона пересувається за зразком, що призводить до перерозподілу домішок. Якщо домішка краще розчиняється в рідкій фазі, то вона поступово накопичується в розплавленої зоні, рухаючись разом з нею. В результаті домішка скупчується в одній частині вихідного зразка. У порівнянні з спрямованою кристалізацією цей метод має більшу ефективність. Метод був запропонований В. Дж. Пфанн в 1952 і з тих пір завоював велику популярність. В даний час метод використовується для очищення понад 1500 речовин.
Схема пристрою для зонної плавки в човнику наведена на рис. 1.
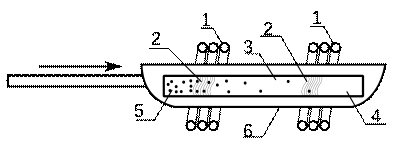
Рис. 1. Схема пристрою для зонного плавлення германію: 1 - індукційні котушки; 2 - розплавлені зони; 3 - очищений германій, 4 - надчистий германій, 5 - германій з підвищеним вмістом домішок; 6 - графітова човник;
Очищуване речовина поміщають у човник з тугоплавкого матеріалу. Основні вимоги до матеріалу човники:
- висока температура плавлення;
- матеріал човники не повинен розчинятися в очищуваному речовині або реагувати з ним.
Човник поміщають в горизонтальну трубу, у якої один кінець може бути запаяний або через нього подають інертний газ. Якщо він запаяний, то інший кінець труби з'єднаний з вакуумною установкою.
Один кінець зразка розплавляється, потім розплавлена зона починає рухатися вздовж злитку. Довжина розплавленої зони залежить від довжини злитка і становить кілька сантиметрів. Речовина плавиться або індукційними струмами, або теплопередачей в печі опору. Швидкість руху складає, як правило, від декількох міліметрів до декількох сантиметрів на годину. Рух може здійснюватися або за рахунок витягування човники через нерухому піч, або зміщенням зони нагріву. Іноді для підвищення ефективності збільшують число проходів зони або число зон. Розподіл домішки характеризується коефіцієнтом розподілу, що дорівнює
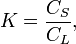
де С S - концентрація домішки в твердій фазі, З L - концентрація домішки в рідкій фазі.
Іноді замість коефіцієнта розподілу K використовують коефіцієнт поділу α, що дорівнює

Домішки, для яких коефіцієнт розподілу K <1, концентруються в розплавленої зоні і разом з нею переміщуються до кінця злитка. З іншого боку від розплавленої зони утворюються шари речовини, більш чистого щодо домішок, для яких K <1. Ті домішки, для яких K> 1, навпаки, концентруються на початку злитка. Якщо здійснити багаторазове проходження розплавленої зони, то домішки з K <1 зберуться в кінці злитка. Для домішок з К> 1 метод мало ефективний. Найчистіші частини зливка (з середини) використовуються для виготовлення приладів. Таким методом можна очистити германій до зразків з питомим опором близько 70 Ом см, в яких залишається приблизно один атом домішки на 10 жовтня атомів германію.
Якщо розплав вступає в реакцію з матеріалом тигля (човники), або очищуване речовина має високу температуру плавлення (> 1500 C), застосовують бестігельной зонну плавку.
Метод має низку недоліків. Основний недолік - неможливість масштабування, оскільки швидкість процесу визначається швидкістю дифузії домішки. Тому метод застосовується для кінцевої стадії очистки при отриманні особливо чистих речовин. Максимальні габарити човники - довжина 50 см, товщина 2-3 см, довжина розплавленої зони 5 см.
Рафінування металів — очищення первинних (чорнових) металів від домішок. Чорнові метали, що отримуються з сировини, містять 96—99% основного металу, решта припадає на домішки. Такі метали не можуть використовуватися промисловістю через низькі фізико-хімічні і механічні властивості. Домішки, що містяться в чорнових металах, можуть мати власну цінність. Так, вартість золота і срібла, що витягують з міді, повністю окупає всі витрати на Рафінування. Розрізняють 3 основних методи рафінування: пірометалургійний, електролітичний і хімічний. У основі всіх методів лежить відмінність властивостей елементів, що розділяються: температур плавлення, щільності, електронегативності тощо. Для отримання чистих металів нерідко використовують послідовно декілька методів рафінування.
Пірометалургійне рафінування
Здійснюється при високій температурі в розплавах і має ряд різновидів. Окислювальне рафінування засноване на здатності деяких домішок утворювати з O, S, Cl, F міцніші з'єднання, ніж з'єднання основного металу з тими ж елементами. Спосіб застосовується, наприклад, для очищення Cu, Pb, Zn, Sn. Так, при продуванні рідкої міді повітрям приміси Fe, Ni, Zn, Pb, Sb, As, Sn, що мають більшу спорідненість до кисню, ніж Cu, утворюють оксиди, які спливають на поверхню ванни і видаляються.
Лікваційне розділення засноване на відмінності температур плавлення і щільності компонентів, що складють сплав, і на малій їх взаємній розчинності. Наприклад, при охолоджуванні рідкого чорнового свинцю з нього при певних температурах виділяються кристали Cu (т.з. шлікери), які унаслідок меншої щільності спливають на поверхню і видаляються. Спосіб застосовується для очищення чорнового свинцю від Cu, Ag, Au, Bi, очищення чорнового цинку від Fe, Cu, Pb, при Р. Sn і інших металів.
При фракційній перекристалізації використовується відмінність в розчинності домішок металу в твердій і рідкій фазах з урахуванням повільної дифузії домішок в твердій фазі. Спосіб застосовується у виробництві напівпровідникових матеріалів і для отримання металів високої чистоти (наприклад, зонна плавка, плазмова металургія, витягування монокристалів з розплаву, направлена кристалізація).
У основі ректифікації, або дистиляції, лежить відмінність в температурах кипіння основного металу і домішки. Рафінування здійснюється у формі безперервного протиточного процесу, в якому операції сублімації і конденсації фракцій, що видаляються, багато разів повторюються. Використання вакууму дозволяє помітно прискорити рафінування. Спосіб застосовується при очищенні Zn від Cd, Pb від Zn, при розділенні Al і Mg, в металургії Ti і інших процесах. Вакуумна фільтрація рідкого металу через керамічні фільтри (наприклад, в металургії Sn) дозволяє видалити зважені в нім тверді домішки. При рафінуванні сталі в ковші рідкими синтетичними шлаками поверхня контакту між металом і шлаком в результаті їх перемішування значно більше, чим при проведенні рафінувальних процесів в плавильному агрегаті; завдяки цьому різко підвищується інтенсивність протікання десульфурації, дефосфорації, розкислювання металів, очищення його від неметалевих включень. Редагування сталі продуванням розплаву інертними газами використовується для видалення з металу зважених частинок шлаку або твердих оксидів, що прилипають до бульбашок газу і флотують на поверхню розплаву
Електролітичне рафінування
Електролітичне рафінування є електролізом водних розчинів або сольових розплавів і дозволяє отримувати метали високої чистоти. Застосовується для глибокого очищення більшості кольорових металів.
Електролітичне рафінування з розчинними полягає в анодному розчиненні металів, що очищаються, і осадженні на катоді чистих металів в результаті придбання іонами основного металу електронів зовнішнього ланцюга. Розділення металів під дією електролізу можливо внаслідок відмінності електрохімічних потенціалів домішок і основного металу. Наприклад, нормальний електродний потенціал Cu щодо водневого електроду порівняння, прийнятого за нуль + 0,346, у Au і Ag ця величина має більше позитивне значення, а у Ni, Fe, Zn, Mn, Pb, Sn, Co нормальний електродний потенціал негативний. При електролізі мідь осідає на катоді, благородні метали, не розчиняючись, осідають на дно електролітної ванни у вигляді шламу, а метали, що володіють негативним електродним потенціалом, накопичуються в електроліті, який періодично очищають. Іноді (наприклад, в гідрометалургії Zn) використовують електролітичне рафінування з нерозчинними анодами. Основний метал знаходиться в розчині, заздалегідь ретельно очищеному від домішок, і в результаті електролізу осідає в компактному вигляді на катоді.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 2673; Нарушение авторских прав?; Мы поможем в написании вашей работы!