
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электролизом называется окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через расплав или раствор электролита
|
|
|
|
ЭЛЕКТРОЛИЗ.
План
1. Сущность процессов протекающих при электролизе.
2. Виды электролиза:
2.1 электролиз расплавов,
2.2 электролиз водных растворов.
3. Последовательность разрядки ионов на электродах.
4. Явление перенапряжения.
5. Законы электролиза.
6. Применение электролиза.
Литература.
1. Фролов В.В. Химия. Гл.V, §51-56.
2. Лучинский Г.П. Курс химии. Гл.V, §8-12, гл. VI, §13-18
3. Общая химия под ред. Соколовской Е.М. и др. Гл.6, §1-11.
В растворах и расплавах электролитов разноименно заряженные ионы (анионы - отрицательно заряженные ионы, катионы - положительно заряженные ионы), находятся в хаотическом движении. Рассмотрим электролиз расплава хлорида натрия (NaCl). При плавлении хлорид натрия диссоциирует:
NaCl 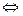 Na+ + Cl-
Na+ + Cl-
Если через такую систему пропустить постоянный электрический ток, то катионы натрия начнут упорядоченно перемещаться к катоду (К -), а анионы хлора - к аноду (А+). На электродах будет протекать окислительно-восстановительная реакция
 Восстановление К- Na++ē
Восстановление К- Na++ē 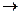 Na0 2 Na+ принимает электроны с у катода: катода
Na0 2 Na+ принимает электроны с у катода: катода
Окисление A + 2Cl - - 2ē 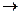 Cl201 Cl - отдает электроны аноду
Cl201 Cl - отдает электроны аноду
 у анода:
у анода:
2Na+ + 2Cl- 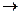 2Na + Cl2
2Na + Cl2
В этом заключается сущность электролиза.
Уравнение электролиза:2NaCl 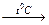 2Na+ + 2Cl-
2Na+ + 2Cl- 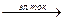 2Na + Cl2
2Na + Cl2 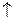 .
.
Восстановительные и окислительные свойства электрического тока во много раз сильнее действия химических восстановителей и окислителей. Например, окисление иона F- происходит только при электролизе KF в HF:
К- 2H+ + 2ē 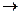 H2
H2
A+ 2F- - 2ē  F2.
F2.
Продуктами электролиза расплава являются составные части расплавленного электролита.
Электролиз растворов электролитов достаточно сложен, поскольку в электролите присутствуют всегда несколько видов катионов и анионов, а также недиссоциированные молекулы электрически активных веществ например, воды. Последовательность протекания электродных процессов определяется значениями их стандартных электродных потенциалов и величиной поляризации.
|
|
|
Восстановление ионов на катоде:
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 590; Нарушение авторских прав?; Мы поможем в написании вашей работы!