
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Регуляция клеточного цикла. Апоптоз. Онкогенетика. 1 страница
|
|
|
|
Митотический цикл и его регуляция. Роль циклинов и циклинзависимых киназ. Принципы передачи митогенного сигнала. Роль факторов роста, интегринов и кадгеринов. Контрольные точки митотического цикла. Апоптоз.
Генетические механизмы канцерогенеза. Общая характеристика генов, берущих участие в канцерогенезе: вирусные онкогены, протоонкогены, гены-супрессоры опухолей, гены-мутаторы. Канцерогенные факторы.
Митотический цикл и его регуляция. Казалось бы, давно известная вещь – фазы цикла (G1, S, G2, M), стадии митоза (профаза, метафаза, анафаза и телофаза), - все уже сто лет как описано и изучено.
Но что заставляет клетку «двигаться» по этому кругу? Как удается ей обеспечить строго упорядоченную смену множества событий, составляющих клеточный цикл? Какие механизмы запускают, например, синтез ДНК в S-фазе, а затем во время его останавливают, предупреждая повторное удвоение ДНК? Как и почему происходит разрушение ядерной оболочки в поздней профазе, а затем образование сразу двух таких оболочек в телофазе? И так далее – подобные вопросы уместны в отношении каждого процесса.
Долгое время все это было совершенно неясно. И только благодаря исследованиям последних лет перед нашим взором стала проступать, с одной стороны, чрезвычайно удивительная (по своей сложности и «продуманности»), а с другой стороны, вполне естественная картина под названием «Регуляция клеточного цикла».
На протяжении клеточного цикла разные клетки могут вступать в различные процессы.
Действительно, делящиеся клетки могут не только продолжать делиться или временно прекратить деления, впав в «спячку» (как бывает со стволовыми клетками). Их судьба, в зависимости от целого ряда обстоятельств (генетической программы, действия гистогормонов, влияние прочих внутренних и внешних факторов), может очень круто измениться. Вот наиболее драматические варианты:
- клетка вступает в процесс дифференцировки,
- в клетке запускаются механизмы самоуничтожения (апоптоза),
- клетка подвергается бласттрансформации, т. е. превращается в опухолевую клетку.
Все это процессы чрезвычайной биологической важности. И то, в какой именно из них вступит делящаяся клетка, определяется в ходе клеточного цикла.
Длительность клеточного цикла изменяется в зависимости от типа клетки и стадии развития организма. Например, клеточный цикл оплодотворенного яйца очень непродолжителен. Оплодотворенное яйцо лягушки делится очень быстро (около 30 минут). Большую часть этого времени занимают S и М фазы, а на фазы G1 и G2 затрачивается очень мало времени. Поскольку в яйце уже существует большой запас белков и других веществ, необходимых для клеточного деления, синтеза новых белков почти не требуется. Таким образом, G1,2- фазы укорачиваются.
На ранних стадиях развития необходимо сформировать как можно больше клеток за относительно короткий промежуток времени. Например, в оплодотворенном яйце лягушки в течение 6 часов происходит 12 дроблений и образуется эмбрион из 8192 клеток. Клетки делятся быстро, но увеличиваются в размерах незначительно. Тем не менее, за счет огромного количества клеток и некоторой ассиметрии деления, эмбрион формируется в течение нескольких часов. После того, как эмбрион сформирован, и закладка трех основных типов ткани завершена, время, необходимое для клеточного цикла, увеличивается за счет удлинения G-фаз. Синтез новых белков приводит к тому, что клетка увеличивается в размере и объеме.
Клеточный цикл оплодотворенного яйца человека, в отличие от яйца лягушки, длится значительно дольше. Первое деление длится 30 часов, а весь процесс дробления – 7 суток (у лягушки – 6 часов).
Однако примерная продолжительность стадий цикла для быстро делящихся клеток человека составляет:
S-период – 10 ч,
G2-период – 4,5 ч,
М-период – 0,5 ч,
G1-период – 9 ч.
Итого – 24 ч (рис.42.). Но, разумеется, это очень приблизительные оценки, и для каких-то клеток цикл может быть более продолжительным. В частности отмечалось, что для сперматогоний S-период длится 15 часов. И, соответственно, в 1,5 раза больше оказывается у них продолжительность цикла – примерно 1,5 суток. Так что на 10 митотических делений сперматогоний (происходящих на первом этапе сперматогенеза) требуется 2 недели.
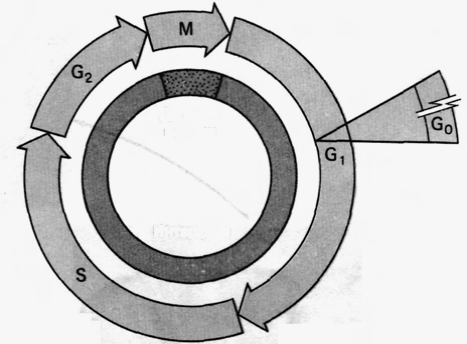
Рис.42. Клеточный цикл: митоз и цитокинез (клеточное деление) составляют М-фазу цикла, кульминацией, которой является образование двух дочерних клеток. Каждая дочерняя клетка вступает в G1-период интерфазы и может начать новый клеточный цикл. За периодом G1 следует S-фаза, во время которой ДНК и хромосомы дуплицируются, и далее – фаза G2. Начало митоза означает конец интерфазы. Покоящиеся клетки задерживаются в фазе G1 и, как говорят, находятся в фазе G0. Обычно эукариотические клетки, которые не остановились в фазе G0, завершают цикл за 24 ч.
Роль циклинов и циклинзависимых киназ. Исследования митотического цикла показали, что ключевую роль в поочередной смене его фаз играют специальные протеинкиназы - т.е. циклинзависимые киназы (Cdks - cyclin-dependent kinasis). Каждая из них фосфорилирует определенные белки, вовлеченные в соответствующую фазу цикла, и таким образом активирует или ингибирует их.
Молекула любой Cdk состоит лишь из одной субъединицы, которая сама по себе неактивна. Для активации же Cdk требуется связывание с ней специального белка - циклина (Ц). Имеется несколько разных циклинов, и, как считают, связавшийся с Cdk циклин не только активирует фермент, но и придает ему субстратную специфичность в отношении тех или иных белков.
Термин циклин отражает тот факт, что концентрации циклинов в клетке в течение клеточного цикла изменяются циклическим образом (рис.43).
В активной форме протеинкиназы представляют собой гетеродимерные комплексы циклин-Cdk (Ц-Cdk), где циклин служит активаторной, a Cdk - каталитической субъединицей. Данные образования не рассматривают как единые молекулы, а называют комплексами, из-за того, что могут быть разные сочетания конкретных циклинов и конкретных Cdk, причём каждое такое сочетание характерно для строго определённой фазы цикла.
Запускают цикл комплексы циклинD-Cdk4 и (или) циклинD-Cdk6. Разные циклины обозначаются латинскими буквами, а разные Cdk - арабскими цифрами. Названные комплексы функционируют на начальной стадии постмитотического (G1) периода и, вызывая соответствующие внутриклеточные события, способствуют переходу клеткой «точки рестрикции» (точка, предшествующая S-периоду, т.е. для постоянно делящихся клеток находится где-то в конце G1-периода, а для клетки, начинающей деление после перерыва, где-то в конце Go -периода). Аналогично, те же комплексы приводят к возврату «спящей» Go -клетки в митотический цикл.
Вторая половина G1 -происходит под управляющим влиянием комплекса циклин E-Cdk2.
В следующем - синтетическом (S) - периоде функционирующая циклинзависимая киназа остаётся той же (Cdk2), но она дважды меняет своих циклиновых партнёров - ими последовательно становятся циклин А и циклин В. Соответственно, меняются и те белковые субстраты, на которые действуют Cdk2.
В премитотическом (G2) периоде последний из вышеназванных циклинов (В) связывается с другой Cdk - Cdkl. Именно комплекс циклин B-Cdkl «вводит» клетку в митоз и «руководит» этим сложным процессом. Поэтому его еще называют митоз-стимулирующим фактором - MPF (от mitosis-promoting factor).
Из состава последних двух комплексов следует, что их
субстратная специфичность определяется не только циклином, но и самой Cdk, а вернее всего – одновременно тем и другим, т.е. имеющимся сочетанием циклина с Cdk.
Cdk1 нередко обозначается иначе - Cdk2. Дело в том, что мутации гена Cdkl, нарушая клеточный цикл, вызывают у дрожжей фенотип вида Сdc2 (при котором клетки становятся необычайно длинными). Поэтому, ещё до идентификации функции этого гена, он был обозначен как Сdc2.
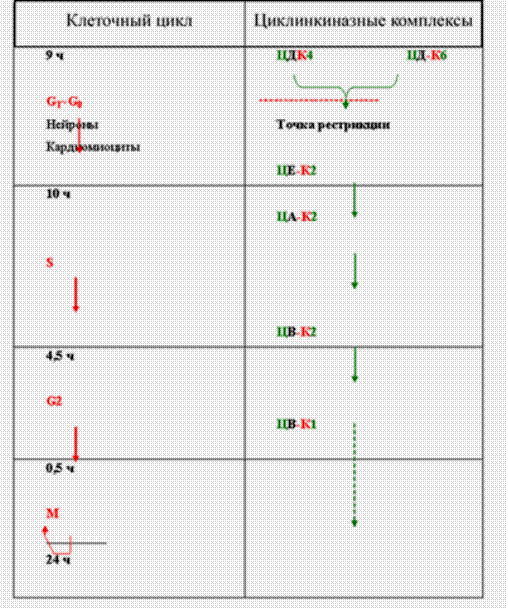
Рис.43. Схема динамики клеточного цикла
Итак, всё разнообразие событий клеточного цикла управляется относительно небольшим числом комплексов циклинов и Cdk.
Способы регуляции и активности Cdks. Ввиду исключительной функции циклинзависимых киназ (Cdks), их содержание и особенно активность находится под сложным контролем. Вот принципиальные способы этого контроля.
1. Регуляция синтеза Cdks. Видимо, не все Cdks одновременно присутствуют в клетке на разных стадиях её цикла. Поэтому очень важным моментом является активация гена той или иной Cdk.
Так, известно, что комплексы G1 периода (циклин D-Cdk4,6 и циклин E-Cdk2), помимо других многочисленных действий, запускают транскрипцию гена киназы Cdkl. Последняя же необходима для образования комплекса G2- периода и митоза (циклин B-Cdkl или MPF). Таким образом, о синтезе компонентов данного комплекса клетка «заботится» заблаговременно, ещё до репликации ДНК.
2. Регуляция активности Cdks. Способы этой регуляции достаточно разнообразны.
а) Один из них - связывание с какой-либо Cdk активаторной
субъединицы - циклина.
б) Второй способ - связывание (либо только с Cdk, либо со всем комплексом циклин-Cdk) ингибиторной субъединицы. В роли последней выступают специальные белки (р15, р16, р21, р27, р57). Известно, по крайней мере, два семейства таких белков. Белки семейства INK4 (р15 и р16) связываются с Cdk4,6 и тем самым препятствуют образованию комплексов (циклин D-Cdk4,6), запускающих клеточный цикл. Белки второго семейства, KIP1 (р21,р27, р57), связываются с уже сформированными комплексами - и это тоже приводит к ингибирующему эффекту.
с) Третий способ контроля активности Cdks - это их фосфорилирование и дефосфорилирование. Т.е. данные протеинкиназы (Cdks) сами способны регулироваться тем же самым способом, каким они управляют активностью «подведомственных» им белков.
Фосфорилирование по одним локусам Cdk обладает активирующим действием; фосфорилирование других участков, напротив, ингибирует фермент.
Но активность киназ восстанавливается под действием специфической фосфатазы, кодируемой геном cdc25a. Из обозначения следует, что это ещё один ген, мутация которого у дрожжей приводит к нарушению клеточного цикла и фенотипу cdc.
Выявлены также две тирозинкиназы (ТК), ингибирующие другую Cdk - Cdkl; одна из этих ТК, видимо, действует на свободную Cdkl, a другая - на весь комплекс циклин В -Cdkl.
3. Регуляция синтеза и распада активаторов и ингибиторов Cdks. В качестве примера обратимся вначале к циклинам.
а) Многие митогенные факторы, «побуждая» клетку к делению, запускают такие регуляторные цепи, которые, в конце концов, активируют ген циклина D (помимо многих других действий). На следующих стадиях клеточного цикла стимулируется синтез очередных циклинов и т.д.
б) Крайне интересным является также управление распадом циклинов. Оно осуществляется с помощью убиквитин зависимого механизма, который используется для короткоживущих белков.
Наиболее чётко роль этого механизма показана для циклина В, участвующего в образовании комплекса циклин В - Cdk2 и митоз-стимулирующего фактора (MPF, он же комплекс циклин B-Cdkl). Фосфорилируя определённые белки, MPF стимулирует вхождение клетки в митоз. Но для завершения митоза необходимы во многом прямо противоположные события. Т.е. содержание MPF должно снижаться. Это достигается с помощью быстрого распада циклина В.
Примерная последовательность событий. Максимальной активности комплекс MPF достигает в метафазе митоза. В это время он фосфорилирует, помимо других белков, так называемый фактор АРС (аnaphase-promotoring complex) т.е. фактор, обеспечивающий анафазу. А данный фактор является ничем иным, как убиквитинлигазой, специфичной в отношении MPF. Поэтому он начинает последовательно присоединять (одну за другой) молекулы убиквитина к циклину В. Меченный таким образом циклин В быстро разрушается в протеосомах. В итоге содержание комплекса циклин B-Cdkl значительно снижается, и в клетке благополучно совершаются события анафазы, а затем и телофазы. Затем в G1-периоде фактор АРС инактивируется, от чего скорость распада циклина В снижается, и данный циклин начинает накапливаться в клетке.
в) Контроль за синтезом веществ, ингибирующих Cdks (либо комплексы циклин-Cdk). Регуляция синтеза часто используется внеклеточными эффекторами для влияния на клеточный цикл - стимуляции или торможения пролиферации. Один из примеров: в некоторых регуляторных внутриклеточных цепочках фигурируют белки семейства Smad. Эти белки, образуя соответствующие транскрипционные факторы, стимулируют синтез ингибиторов р15, р21 и др. В итоге активность комплексов G1-периода тормозится и клетка прекращает деление.
Принципы передачи митогенного сигнала. Практически все сигнальные пути, регулирующие пролиферацию клеток, «нацелены» на комплексы G1-периода — в основном, циклин D—Cdk4,6 и, в меньшей степени, циклин Е—Cdk2. Это и понятно: как уже отмечалось, именно данные комплексы «запускают» очередной клеточный цикл.
Рассмотрим два митогенных сигнальных пути. Один из них относится к стволовым клеткам эпителия и начинается со связывания ЭФР — эпидермального фактора роста.
Второй путь активируется в Т-хелперах после их взаимодействия с АПК — антигенпредставляющими клетками.
Теперь на этих же двух примерах покажем «выход» подобных путей на комплексы циклин-Cdk.
В обоих случаях внешний сигнал приводит к активации
тирозинкиназы, ассоциированной с рецептором. Это ведет (через те или иные посредники) к запуску каскадов митогенактивируемых протеинкиназ (МАПК). Конечные ферменты данного каскада, фосфорилируя ряд транскрипционных факторов (Elk, Ets, ATF2, Tcf и др.), активируют их, а через них — и т. н. гены раннего ответа (FOS, JUN). В культуре клеток уже через 30 мин после начала действия митогена активность этих генов достигает максимального
уровня.
Продукты семейств генов FOS и JUN — это опять-таки
транскрипционные факторы, но специфичные уже в отношении других генов — т. н. генов замедленного ответа. Поэтому через некоторое время начинается экспрессия этих генов.
Среди последних-то и находятся наши «знакомые» — гены циклина D, Cdk4 и Cdk6, т.е. компонентов комплексов циклин-Cdk, специфичных для первой половины G1 - периода цикла.
Кроме того, активируются еще некоторые гены и среди них — ген белка Мус. 


 После своего синтеза белок Мус, в свою очередь, влияет на активность ряда генов. Так, он тормозит экспрессию гена белка р27 — ингибитора целого ряда комплексов циклин- Cdk. И одновременно белок Мус активирует ген Cdc25a, который кодирует специфическую фосфатазу. Последняя дефосфорилирует Cdk4 и Cdk2, что приводит к их активации.
После своего синтеза белок Мус, в свою очередь, влияет на активность ряда генов. Так, он тормозит экспрессию гена белка р27 — ингибитора целого ряда комплексов циклин- Cdk. И одновременно белок Мус активирует ген Cdc25a, который кодирует специфическую фосфатазу. Последняя дефосфорилирует Cdk4 и Cdk2, что приводит к их активации.
В результате мы получаем следующие эффекты:
увеличение содержания в клетке циклина D и реагирующих с ним киназ — Cdk4, Cdk6;
снижение содержания ряда ингибиторов Cdks;
повышение активности (в результате дефосфорилирования) тех же циклинзависимых киназ (Cdk4, Cdk6), а также Cdk2.
Все это и обеспечивает формирование в клетке достаточного количества активных комплексов циклин D—Cdk4,6, начинающих подготавливать клетку к делению.
Заметим, чтобы рассмотренные сигнальные пути «сработали», необходимо одно условие: клетка должна быть фиксирована на каком-либо внеклеточном матриксе.
Действие антимитогенов. Это действие ФНО (фактора некроза опухолей) на опухолевые клетки. ФНО «запускает» в клетках сразу несколько сигнальных путей, и среди них один содержит ферментативный каскад МАПК. Только теперь возбуждение соответствующего рецептора через ряд посредников (среди которых — сфингозин и ПК-С) приводит к торможению МАПК. Дальше — все как в предыдущих путях, но с противоположным знаком. Следовательно, в итоге в клетке будет резко снижаться количество активных комплексов циклин D—Cdk4,6, в результате чего деления прекратятся. Действие же ФНО через другие сигнальные пути будет инициировать апоптоз.
Второй пример: речь идет о ТФРр — трансформирующем факторе роста. Уже отмечалось, что он угнетает пролиферацию многих клеток. Рецепторы ТФРр, видимо, сходны по структуре с рецепторами ЭФР (эпидермального фактора роста). Это значит, что при связывании своего лиганда рецепторные субъединицы объединяются в димерные структуры, цитоплазматические домены каждой субъединицы обладают тирозинкиназной активностью, в активированном состоянии эти домены фосфорилируют друг друга. Отличие состоит лишь в том, что в данном случае модифицированные домены рецептора связывают иной комплекс цитоплазматических белков: теперь это комплекс Smad2+Smad3. Он тоже фосфорилируется рецепторной тирозинкиназой, после чего приобретает способность связывать третий белок — Smad4.
Затем весь этот тройной комплекс диффундирует в ядро и выполняет роль транскрипционного фактора для генов, кодирующих ингибиторы Cdks. Имеются в виду такие белки, как р15 и р21.
Накопление в клетке этих ингибиторов и приводит к торможению пролиферации.
Роль факторов роста, интегринов и кадгеринов. Клеткам низших организмов для вступления в S-фазу клеточного цикла необходимо наличие питательных веществ во внешней среде. При недостатке питательных веществ клетка не делится. У высших организмов наличие питательных веществ обычно не является лимитирующим фактором. Однако сигнал, инициирующий деление клетки, чаще бывает внешним, чем внутренним. Доказательства этого были получены в первых экспериментах с культурой клеток млекопитающих in vitro.
При разработке методики выращивания клеток млекопитающих в культуре было отмечено, что клетки растут лучше, если они находятся внутри кровяных сгустков. Из-за неудобства исследования растущих клеток внутри сгустка, после свертывания крови сгусток удаляется. Оставшаяся жидкость известна как сыворотка. Если удалить все клетки до того, как кровь свернется, и добавить полученную сыворотку к растущим клеткам, она не будет поддерживать рост. Это доказывает, что при свертывании из клеток крови высвобождается некий фактор, необходимый для деления клеток. Было показано, что это вещество высвобождается из тромбоцитов, и оно было названо тромбоцитарным фактором роста (PDGF). Оказывается, нормальные клетки млекопитающих содержат достаточное количество питательных веществ для деления. Таким образом, в клетки должен поступать дополнительный сигнал, стимулирующий пролиферацию. В случае с тромбоцитарным фактором роста этот белок секретируется тромбоцитами при свертывании крови после образовании раны. Для восполнения тканевого дефекта тромбоцитарный фактор роста, один из главных факторов роста организма, сигнализирует окружающим клеткам о необходимости приступить к делению.
К настоящему времени выделено и охарактеризовано большое число факторов роста: тромбоцитариый фактор роста; эпидермальный фактор роста (EGF); факторы роста фибробластов (FGF) (имеют девять изоформ и обладают небольшой клеточной специфичностью, однако еще относятся к группе малоспецифичных); фактор роста нервов (NGF) (этот фактор роста действует только на клетки нервной системы); эритропоэтин (ЕРО) (этот фактор роста стимулирует образование эритроцитов в костном мозге); иитерлейкин-2 и интерлейкин-3.
Все эти факторы роста действуют в основном на специфические клетки-мишени. Каждый фактор роста является лигандом, который связывается со специфическим поверхностным рецептором клетки и инициирует процесс передачи сигнала.
Большинство клеток млекопитающих находится в особой фазе клеточного цикла, называемой Go-фазой или компартментом клеточной дифференцировки. Эта фаза клеточного цикла представляет собой удлиненную фазу G1. Это означает, что гены, кодирующие белки, которые запускают пролиферацию клеток, находятся в «выключенном» состоянии. В этом положении метаболическая энергия клетки расходуется на образование специализированных белков, необходимых для осуществления дифференцировки. Таким образом, гены, кодирующие эти белки, находятся во «включенном» состоянии.
В большинстве типов клеток гены для клеточной пролиферации могут быть включены снова. Однако в некоторых клетках гены пролиферации никогда не запускаются повторно после выключения. При завершении пролиферации в клетках сердечной мышцы Cdk и циклины выключаются и больше никогда не включаются. То же справедливо и для всех типов нейронов.
Однако в соответствующих условиях многие клетки могут вернуться в цикл деления. Практически во всех тканях организма происходят клеточные «превращения». Обычно такие превращения происходят редко. Исключение составляют клетки крови и кишечного эпителия, в которых скорость обновления клеток очень высока.
Как показано выше, один из основных типов сигналов, активирующих Cdk и циклины, генерируют факторы роста. Однако, даже получив такой сигнал, организм должен регулировать ответ таким образом, чтобы поддерживать количество и пространственную организацию клеток. Если этого не происходит, наступают летальные изменения организма.
При исследовании нормальных клеток, выращенных в культуре ткани, было показано, что существуют различные факторы, определяющие число клеток, необходимых для поддержания архитектуры ткани, и качество соединения клеток с базальной мембраной. Если выращиваемые в культуре фибробласты заполняют всю чашку Петри, они перестают делиться и, очевидно, уходят в псевдо-Со-фазу. Если в стерильных условиях по поверхности культуры провести шпателем диагональную линию, клетки, расположенные на этой линии, погибают и остается бесклеточная диагональ. Клетки, находящиеся на краю «раны», начинают немедленно делиться и пролиферировать, заполняя свободное пространство. Как только пространство заполнено, деление снова прекращается.
На основе этого наблюдения был сделан вывод о том, что нормальные клетки делятся до достижения определенной плотности. После образования контактов с другими клетками на субстрате, внутрь клетки передается сигнал о том, что все контактные точки заняты, и гены, запускающие пролиферацию, выключаются.
Если клетке не давать соприкоснуться с поверхностью тарелки, она сохраняет округлую форму и не вступает в митоз. Если же клетка соприкасается с поверхностью и расплющивается, она формирует с поверхностью тарелки контакты, называемые фокальными контактами и фокальными адгезионными пластинками. В состав фокальной адгезионной пластинки входят важные компоненты цитоскелета, включая актиновые филаменты, микротрубочки и другие структурные белки. Спустя некоторое время эти клетки вступают в митоз.
Результаты этих и аналогичных экспериментов доказывают, что молекулы окружающей среды, например входящие в состав межклеточных контактов и контактов клеток с межклеточным веществом, участвуют в управлении клеточной пролиферацией.
Теперь рассмотрим такие сигнальные пути, которые начинаются от адгезивных мембранных белков. Одни из этих путей стимулируют пролиферацию клеток; другие, наоборот, тормозят.
Многие клетки способны делиться, только будучи прикрепленными к внеклеточной структуре – базальной мембране (эпителиоциты), коллагеновым волокнам (фибробласты) и т.д.
Информация же о связи клетки с такой структурой поступает от интегринов. Это адгезивные белки с двумя неравными субъединицами.
При связывании с внеклеточным матриксом меньшая (р-) субъединица интегрина активирует одну из тирозинкиназ — FAK (Focal Adhesion Kinase), а та, в свою очередь, еще одну тирозинкиназу — Src. Последняя относится к классу нерецепторных тирозинкиназ, поскольку не входит в состав рецепторного комплекса и даже не взаимодействует напрямую с рецепторами.
Непосредственным субстратом Src является белок SHC, который связывает данный сигнальный путь (идущий от интегринов) с сигнальными путями от рецепторов митогенов. Общей же частью последних путей являются многократно упоминавшиеся выше каскады МАПК (митогенактивируемых протеинкиназ). Следовательно, адаптерный белок SHC должен стимулировать прохождение сигнала по данным каскадам.
Однако не вполне ясно, какой именно член каскадов активируется белком SHC. Есть предположение, что это тот же комплекс белков (GRB, SOS, Ras, Raf), что и в случае действия ЭФР (эпидермального фактора роста).
Но, с нашей точки зрения, надо учесть следующее обстоятельство. Для того, чтобы клетка млекопитающих стала делиться, необходимо одновременное выполнение двух условий: прикрепление клетки к какой-либо поверхности и действие на нее ростового фактора.
Причем в неприкрепленной клетке прохождение сигнала от ростового фактора блокируется на одной из МАПК, а конкретно — на киназе МЕК (МЕК1).
Отсюда следует, что:
а) сигнал от интегринов идет именно к этому звену МАПК — киназе МЕК;
б) данная киназа активируется только при действии на нее сразу двух белков: предыдущей киназы из семейства МАПК и белка SHC (после действия на него Src).
Тогда и получается, что сигналы от ростового фактора и интегринов взаимно дополняют друг друга, а каждый из них в отдельности не способен индуцировать деление клетки.
Эффект прикрепления клетки к опоре включает еще одно важное событие. Оно касается «знаменитого» транскрипционного фактора — белка р53.
Последний активирует гены, останавливающие деления (в частности, ген белка р21 — ингибитора комплексов циклин- Cdk), а также гены апоптоза. Поэтому неудивительно, что идущий от интегринов сигнал приводит к снижению содержания в клетке такого «вредного» белка.
В случае белка р53 обычно регулируется не синтез, а распад. Поэтому под действием сигнала от интегринов, видимо, тем или иным способом ускоряется протеолиз этого белка. По некоторым данным, это может быть связано со снижением содержания другого белка (ARF), ингибирующего распад белка р53.
Контактное торможение пролиферации. Если же клетка устанавливает контакт не с внеклеточным матриксом, а с другими клетками, то наблюдается эффект, прямо противоположный предыдущему, — прекращение делений. Это обозначается как контактное торможение.
После очередного пересева клеток в плоский стеклянный сосуд («матрас») они вначале — в течение нескольких часов прикрепляются ко дну сосуда и лишь после этого входят в клеточный цикл (стимуляция делений).
Когда же на дне сосуда не остается свободного места и клетки вступают в контакт друг с другом, деления прекращаются (контактное торможение).
Сигнал о межклеточном контакте, видимо, идет от кадгеринов — адгезивных белков, участвующих в образовании таких контактов. Вероятно, у кадгеринов меняется при этом конфигурация; поэтому их цитоплазматические домены приобретают способность связывать белок р-катенин.
Предполагают, что данный белок — транскрипционный фактор. Когда он свободен от связи с кадгерином (т. е. когда клетка еще не контактирует с другими клетками), он образует активный комплекс с еще одним транскрипционным фактором — белком Tcf4. Комплекс мигрирует в ядро и здесь прямым или (скорее всего) опосредованным способом стимулирует транскрипцию генов циклина D и белка Мус.
Это вновь те самые гены, которые активируются в ранее рассмотренных сигнальных путях — идущих от ростовых факторов и от интегринов. Те пути сходятся и взаимно дополняют друг друга на каскадах митогенактивируемых киназ (МАПК).
Но путь, содержащий β-катенин, тоже является необходимым для деления. При улавливании β-катенина кадгерином деления прекращаются. Следовательно, этот путь также необходимо дополняет предыдущие. С нашей точки зрения, все объясняется и встает на свои места при следующих предположениях:
· в начале любого клеточного цикла должен образоваться некий (всегда один и тот же) промитотический комплекс транскрипционных факторов (ПМКТФ), специфичный в отношении генов раннего ответа;
· в состав этого комплекса входят β-катенин и белок Tcf4, что возможно лишь тогда, когда β-катенин не связан кадгерином (нет межклеточных контактов);
· кроме того, комплекс содержит факторы, активируемые каскадом МАПК; причем этот каскад сам, по предыдущему нашему предположению, требует двойного сигнала от интегринов (клетка прикреплена к внеклеточной структуре) и от ростового фактора.
В итоге число условий, необходимых для деления клетки (в принципе способной к делению), возрастает уже до трех: это не только прикрепление к поверхности и действие ростового фактора, но и отсутствие контактов с другими клетками.
Лишь при выполнении этих условий активируются гены раннего ответа, и запускается механизм клеточного цикла, в частности, образуется «вторая очередь» транскрипционных факторов, а затем и продукты стимулируемых ими генов — циклин D, Cdk4,6 и т. д.
Но этим перипетии внутриклеточных регуляторных путей, связанные с β-катенином, не исчерпываются. Установлено еще, по крайней мере, два интересных факта.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 3583; Нарушение авторских прав?; Мы поможем в написании вашей работы!