
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Исследование нуклеиновых кислот. Методы ДНК-диагностики 2 страница
|
|
|
|
В последнее время в практике нашел применение метод гибридизации в растворе с зондами, мечеными акридином. Результаты гибридизации регистрируют по испусканию меткой света определенной длины волны после обработки щелочью.
В настоящее время ведутся интенсивные разработки по совершенствованию методов гибридизации в следующих направлениях:
· Упрощение процедуры генного зондирования до одной — двух стадий процесса.
· Отказ от сорбции на мембране.
· Повышение чувствительности гибридизационных методов за счет использования процедуры амплификации сигнала с зонда.
Активные разработки по третьему направлению стали возможными лишь с момента появления и внедрения в практику методов амплификации нуклеиновых кислот.
Клонирование фрагментов нуклеиновых кислот in vitro. Полимеразная цепная реакция (ПЦР). В большинстве случаев для успешной диагностики болезни или гетерозиготного состояния достаточно исследовать лишь небольшой фрагмент генома, поэтому для проведения анализа необходимо получить достаточное количество таких фрагментов, т.е. амплифицировать (умножить) их. Ранее эта задача решалась с помощью трудоёмкого подхода: создание рекомбинантной плазмиды - введение плазмиды в бактериальную клетку - размножение бактериальных клеток - выделение заданных фрагментов ДНК. Теперь эта задача - накопление нужных фрагментов ДНК - решается с помощью ПЦР. Открытие данной реакции совершило подлинную революцию в изучении генома человека и в молекулярно-генетической диагностике наследственных болезней.
Полимеразная цепная реакция (ПЦР) — метод амплификации ДНК in vitro. В течение нескольких часов можно размножить определённую последовательность ДНК в количестве, превышающем исходное в миллион раз и более. Следовательно, исходно требуется очень незначительное количество материала. Необходимым условием для проведения ПЦР является знание нуклеотидной последовательности амплифицируемого фрагмента или, по крайней мере, этого фрагмента (рис.50).
В соответствии с нуклеотидной последовательностью концов исследуемого участка синтезируется два олигонуклеотидных праймера (затравки). Длина праймеров составляет 20—30 пар нуклеотидов.
Процесс амплификации заключается в осуществлении повторяющихся циклов. Каждый цикл включает 3 стадии: температурная денатурация ДНК (разделение двухцепочечной ДНК на одноцепочечные молекулы) - присоединение праймеров к комплементарным последовательностям одноцепочечных молекул (отжиг) - синтез полинуклеотидных цепей на одноцепочечных молекулах в границах присоединенных праймеров с помощью полимеразы.
Впервые состав ингредиентов, входящих в реакционную смесь для постановки полимеразной цепной реакции, и основные принципы использования праймеров для получения копий ДНК были описаны Kleppe с соавт. в 1971 году. Однако тогда еще не была продемонстрирована основная черта ПЦР - экспоненциальное увеличение количества копий фрагмента исходной ДНК как результат реакции. Это было осуществлено в 1985 г. Последующее использование в ПЦР термостабильной ДНК-полимеразы существенно расширило возможности ее применения, как в научных целях, так и в клинике. Метод стал настолько популярен, что сегодня уже трудно представить работу в области молекулярной биологии без его использования. Особенно бурное развитие метод полимеразной цепной реакции получил благодаря международной программе «Геном человека». Были созданы современные лазерные технологии сиквенирования (расшифровки нуклеотидных последовательностей ДНК). Если в недавнем прошлом для расшифровки последовательности ДНК размером в 250 пар нуклеотидов (п.н.) требовалась неделя, то современные лазерные секвенаторы позволяют определять
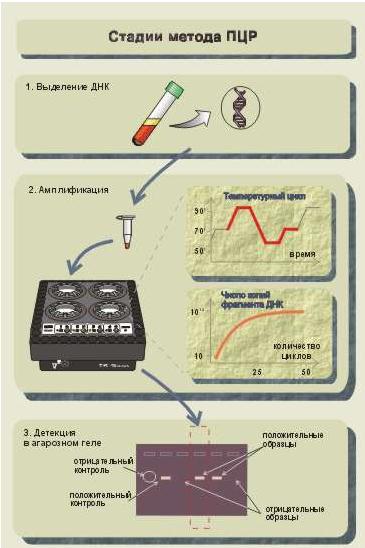
Рис.50. Три этапа ПЦР-анализа
до 5000 п.н. в день. Это в свою очередь способствует значительному росту информационных баз данных, содержащих последовательности ДНК. В настоящее время предложены всевозможные модификации ПЦР, показана возможность создания тест-систем для обнаружения микроорганизмов, выявления точечных мутаций, описаны десятки различных применений метода. В настоящее время ПЦР используется при диагностике: генетических, инфекционных и онкологических заболеваний; патогенов в пище; идентификации личности; в судебной медицине, криминалистике; при трансплантации органов и тканей; определении отцовства. В отличие от иммуноферментного анализа, который широко используется для диагностики инфекционных заболеваний, ДНК-диагностика позволяет определять непосредственно возбудителя заболевания. С помощью усовершенствованных схем постановки ПЦР можно выявлять патогенные микроорганизмы в очень низкой концентрации.
ДНК-диагностика рака ограничивается небольшим, но активно возрастающим количеством сведений о генах, ассоциированных с раком. В рамках проекта «Геном человека» ученые продолжают поиски мутаций, ассоциированных с этим типом заболеваний.
Полимеразная цепная реакция - это осуществляемая in vitro специфическая амплификация нуклеиновых кислот, инициируемая синтетическими олигонуклеотидными праймерами; ее основные этапы представлены на рис. ПЦР-цикл состоит из тепловой денатурации ДНК, ее отжига с праймером и удлинения цепи (элонгации); смена этих этапов происходит в результате простого изменения температуры. Праймеры при этом ориентируются на матрице так, что число раундов репликации растет экспоненциально, соответственно увеличивается и число копий специфической нуклеотидной последовательности.
Применение молекулярных методов для целей клинической диагностики ограничивается их невысокой чувствительностью и длительностью анализа. Так, для выявления нуклеиновой кислоты-мишени методом гибридизации in situ с присутствовала в препарате в нескольких тысячах копий. Нередко число аномальных последовательностей в клиническом препарате диагностически- значимо, но меньше этой величины и гибридизация может дать ложноотрицательный результат. В отличие от этого ПЦР позволяет выявить уникальную нуклеотидную последовательность. Для этого в реакционную смесь добавляют в большом избытке специфичные для данной последовательности олигонуклеотидные праймеры («амплимеры»), которые образуют с ней комплекс, и проводят репликацию ДНК in vitro. Поскольку амплимеры гибридизуются с обеими цепями ДНК, то и нативная последовательность, и синтезируемые ПЦР-продукты могут служить матрицами в последующих раундах репликации, в результате чего число копий уникальной последовательности экспоненциально увеличивается. Благодаря этому последовательности, присутствующие в клиническом препарате в минимальном количестве (одна или несколько копий) и не обнаруживаемые никакими другими методами, легко выявляются с помощью ПЦР. ПЦР позволяет найти всего одну аномальную последовательность на 100000-1000000 нормальных клеток.
Экспоненциальное увеличение числа копий молекулы-мишени не только обеспечивает высокую чувствительность метода, но и облегчает их выявление. Каждый раунд ПЦР занимает от 2 до 5 мин, и обычно для достижения необходимой чувствительности достаточно 25-50 раундов, т. е. 2-4 ч (рис.51). Кроме того, поскольку содержание ПЦР-продуктов достаточно велико, можно использовать неизотопные методы детекции.
Амплификация РНК. Возможность использования РНК в качестве мишени для ПЦР существенно расширяет спектр применения этого метода. Например, геномы многих вирусов (гепатита С, вирус инфлюэнцы, пикорнавирусы и т.д.) представлены именно РНК. При этом в их жизненных циклах отсутствует промежуточная фаза превращения в ДНК. Для детекции РНК необходимо в первую очередь перевести ее в форму ДНК. Для этого используют обратную транскриптазу, которую выделяют из двух различных вирусов: avian myeloblastosis virus и Moloney murine leukemia virus. Использование этих ферментов связано с некоторыми трудностями. Прежде всего, они термолабильны и поэтому могут быть использованы при температуре не выше 42° С. Так как при такой

Рис.51. Полимеразная цепная реакция
температуре молекулы РНК легко образуют вторичные структуры, то эффективность реакции заметно снижается и по разным оценкам приблизительно равна 5%. Предпринимаются попытки обойти этот недостаток используя в качестве обратной транскриптазы термостабильную полимеразу, полученную из термофильного микроорганизма Thermus thermophilus, проявляющего транскриптазную активность в присутствии Mn2+. Это единственный известный фермент, способный проявлять как полимеразную, так и транскриптазную активность.
Для проведения реакции обратной транскрипции в реакционной смеси также как и в ПЦР должны присутствовать праймеры в качестве затравки и смесь 4-х дНТФ, как строительный материал.
После проведения реакции обратной транскрипции, полученные молекулы кДНК могут служить мишенью для проведения ПЦР.
Подбор праймеров. ПЦР-праймеры, или амплимеры, обычно имеют размер от 18 до 25 нуклеотидов. Их можно синтезировать с помощью автоматических синтезаторов ДНК, имеющихся в большинстве крупных исследовательских центров. Количества получаемых таким образом олигонуклеотидов (0,2—1 мкмолей) обычно достаточно для проведения нескольких сотен или тысяч ПЦР-реакций. Часто в 5’-концевой участок праймеров для упрощения клонирования ПЦР-амплифицированной ДНК вводят сайты узнавания для рестриктирующих эндонуклеаз.
Подбор праймеров - ключевое звено ПЦР, поскольку именно ими определяется возможность амплификации и выявления нужной последовательности, а также чрезвычайная гибкость метода. Простое варьирование праймеров позволяет выявлять многие патогенные микроорганизмы и генетические нарушения при минимальных изменениях в методике.
ПЦР-амплифицированные фрагменты ДНК имеют разный размер. Он определяется суммой размера праймеров и расстояния между их 3’-концами и в большинстве случаев лежит в диапазоне 100—300 нуклеотидов. Возможна амплификация (но обычно менее успешная) последовательностей-мишеней длиной более 1000 п.н. Скорость репликации с помощью ДНК-полимеразы Tag составляет 35—100 нуклеотидов в секунду.
Таg-полимераза. В 1980 году полимеразная активность была открытая у некоторых форм термофильных бактерий. Таg-полимераза была выделена из бактерий вида Thermus aquaticus, способных расти при температуре 70-75°С. Молекулярный вес очищенного протеина 94 кД и оптимальная температура полимеразной активности 70-80°С. Активность фермента уменьшается, но полимераза не денатурируется при 90°С, при снижении температуры до 70-80°С уровень активности восстанавливается.
Tag-полимераза имеет очень высокую скорость синтеза. При оптимальных условиях фермент может достраивать до 150 основ на секунду. При низкой температуре активность падает до 2 основ на секунду. Время полужизни Таg-полимерази при 95°С составляет 40 минут.
Секвенирование ДНК — определение нуклеотидной последовательности. В настоящее время разработаны методы определения полной нуклеотидной последовательности любой молекулы ДНК. При решении этой задачи необходимо иметь большое количество идентичных фрагментов молекул ДНК. Наработку интересующих последовательностей можно осуществить клонированием соответствующего фрагмента, например, методом ПЦР. Метод секвенирования по Максаму — Гилберту основан на химическом расщеплении ДНК по определенному основанию. Другой ферментативный метод (метод Сэнгера) базируется на применении аналогов нуклеотидов, прерывающих синтез комплементарной цепи ДНК по одноцепочечной матрице в месте встраивания в цепь соответствующего аналога. Секвенирование позволяет определить полную нуклеотидную последовательность всех хромосом, всего ДНК любого генома, любого организма. Это уже почти полностью сделано для некоторых бактерий, мухи дрозофилы, мыши и человека. Кроме того, этот метод позволяет определить последовательность нуклеотидов любых генов, что дает возможность их синтеза.
Методы ДНК-диагностики. Прямые и косвенные методы ДНК-диагностики. Виды ДНК-диагностики: подтверждающая, пресимптоматическая, носительства, пренатальная.
Принципиально различают прямую и косвенную ДНК-диагностику моногенных наследственных болезней. Прямые методы возможны лишь при условии, что ген заболевания клонирован, известна его экзон-интронная организация или нуклеотидная последовательность полноразмерной комплементарной ДНК. При прямой диагностике предметом анализа являются мутации гена. Главным преимуществом прямых методов диагностики является почти 100% эффективность.
Однако в большинстве случаев наследственных заболеваний ген не клонирован или заболевание является генетически гетерогенным, т.е. обусловлено повреждениями в разных генах, либо молекулярная организация гена не позволяет использовать прямые методы. Эти трудности могут быть преодолены с помощью косвенных методов ДНК-диагностики, основанных на использовании сцепленных с геном полиморфных маркёров. В этом случае определяется гаплотип хромосомы, несущей мутантный ген в семьях высокого риска, т.е. у родителей больного и его ближайших родственников. Такой подход возможен практически для всех моногенных заболеваний с известной локализацией гена.
Прямые методы поиска мутаций. В ДНК-диагностике в настоящее время используются разнообразные прямые методы. Наиболее просто обнаруживаются мутации, изменяющие длину амплифицированных фрагментов ДНК, которые выявляются при электрофоретическом анализе.
Для выявления точковых мутаций, небольших делеций и инсерций в исследуемых генах используется множество различных подходов, основанных на методе ПЦР, благодаря которому можно многократно увеличить уникальную последовательность ДНК, а затем проанализировать её на предмет мутации. С помощью специфических олигонуклеотидных праймеров проводят амплификацию кодирующих участков геномной ДНК в случае, если известна экзон-ннтронная структура исследуемого гена.
Если структура гена не известна, то получают кДНК-продукты путем обратной транскрипции мРНК, выделенной из клеток больных. Продукты амплификации являются объектами дальнейшего поиска мутаций с помощью ряда методов, позволяющих выявлять небольшие структурные изменения.
Методы, основанные на технологии ПЦР. В общем случае секвенирование полноразмерной кДНК, или всех экзонов, для определения мутаций у отдельных пациентов достаточно трудоемко, дорого и требует больших затрат времени. Поэтому на практике чаще проводят предварительный отбор более простыми методами амплификации фрагментов ДНК, предположительно содержащих мутации, а затем секвенируют только эти участки ДНК. Методы поиска фрагментов ДНК, содержащих мутации, основаны на сравнительном анализе мутантных и нормальных последовательностей по целому ряду физических и химических характеристик, которые в значительной степени варьируют в зависимости от типа мутационного повреждения. Следует подчеркнуть, что независимо от метода детекции мутации точные молекулярные характеристики каждой мутации могут быть получены только путем прямого секвенирования.
Наиболее просто обнаруживаются мутации, изменяющие длину амплифицированных фрагментов, так как подобные нарушения легко выявляются при электрофоретическом анализе. Протяженные делеции, захватывающие целые экзоны в генах, сцепленных с полом, могут успешно выявляться при использовании так называемого мультиплексного варианта ПЦР. Разница в размерах и числе амплифицированных фрагментов позволяет легко идентифицировать такие мутации при электрофорезе. Данный подход применим к анализу делеций в аутосомных генах только в тех случаях, когда возможно дополнить ПЦР количественной оценкой результатов амплификации. Оригинальный метод идентификации подобных делеций у гетерозигот основан на использовании в качестве матричной ДНК для ПЦР кДНК, полученной путем обратной транскрипции мРНК, изолированной из экспрессирующих данный ген тканей пациента. В отличие от нормального гомолога, в мутантной молекуле кДНК экзоны граничащие с делецией сближены. Для обнаружения гетерозигот по протяженным внугригенным делециям проводят мультиплексную ПЦР с использованием системы олигопраймеров, полностью перекрывающих всю молекулу кДНК. Наличие делеций регистрируют по появлению продуктов амплификации необычного размера.
После выявления различий между нормальной и мутантной ДНК по длине амплифицированного фрагмента необходимо провести секвенирование необычного фрагмента с целью определения изменений в нуклеотидной последовательности предположительно мутантной ДНК.
При мутациях гена, представляющих собой замену одного или нескольких нуклеотидов, длины амплифицированных фрагментов остаются постоянными, однако некоторые физико-химические свойства мутантных молекул меняются. С учетом этих особенностей разработаны различные варианты поиска мутантных фрагментов ДНК и идентификации в них точковых мутаций. Ведущими из этих методов являются: метод анализа информационного полиморфизма однонитевой ДНК (SSCP), метод анализа гетеродуплексов (НА), денатурирующий градиентный гель-электрофорез (DGGE) и метод химического расщепления некомплементарных сайтов (ССМ).
SSCP (Single Strand Conformation Polymorphism) — метод анализа конформа-ционного полиморфизма однонитевой ДНК — основан на регистрации различий в электрофоретической подвижности однонитевых ДНК, одинаковых по величине, но различающихся вследствие нуклеотидных замен по пространственной организации молекул. Конформация небольших однонитевых ДНК зависит от нуклеотидной последовательности, поэтому замена даже одного нуклеотида приводит к изменению пространственной структуры. Метод включает амплификацию фрагментов ДНК размером до 300 пар нуклеотидов, денатурацию продуктов ПЦР и высокоразрешающий электрофорез в полиакриламидном геле.
Конформационный метод выявления точковых мутаций получил широкое распространение вследствие относительной простоты и возможности обнаруживать любые типы замен. Однако ограничением применения этого метода является размер исследуемого фрагмента ДНК, так как высокая эффективность детекции мутаций, составляющая 80—95%, показана при длине фрагментов менее 200 пар нуклеотидов, в то время как для фрагментов более 400 пар нуклеотидов вероятность обнаружения мутаций уменьшается до 50%.
В настоящее время разрешающая способность метода значительно повышена. В частности, разработаны подходы для идентификации точковых мутаций методом SSCP-анализа в амплифицированных фрагментах ДНК размером до 800 пар нуклеотидов. Для этого используется полиакриламидный гель с низким значением рН.
НА (Heteroduplex Analysis) позволяет выявлять мутации, находящиеся в гетерозиготном состоянии, а также инсерции и делеции. Принцип этого метода заключается в следующем.
При амплификации фрагментов генов гетерозигот, последующей денатурации и медленной ренатурации полученных продуктов ПЦР в амплификационной смеси наряду с двумя типами гомодуплексов образуются гетеродуплексы между нормальной и мутантной цепями ДНК. Такие гетеродуплексные молекулы отличаются по электрофоретической подвижности от гомодуплексов за счет конформационных особенностей в местах несовпадения нуклеотидов, поскольку электрофоретическая подвижность гетеродуплексов значительно ниже, чем гомодуплексов. Эти различия обнаруживаются при электрофорезе в обычном полиакриламидном геле.
На сегодняшний момент наиболее распространенным способом скрининга мутаций является комбинация анализа гетеродуплексов и метода однонитевого конформационного полиморфизма, позволяющая выявить точковые мутации почти в 100% случаев и не требующая больших затрат времени.
DGGE — денатурирующий градиентный гель-электрофорез. В этом методе ДНК-дуплексы подвергаются миграции в геле с градиентом денатурирующих условий (может быть использован и температурный градиент). Миграция продолжается до тех пор, пока ДНК-дуплексы не достигают в геле точки плавления и не разделяются, после чего миграция фрагментов останавливается. Однонуклеотидные различия в нормальной и тестируемой ДНК выявляются по различной электрофоретической подвижности в геле. Высокая чувствительность метода (95%) достигается благодаря специфическим праймерам с так называемым GC-зажимом, представленным чередованием гуанина и цитозина в количестве до 20 нуклеотидов. За счет этого температура плавления продукта амплификации сильно увеличивается, что повышает эффективность определения мутации. Однако праймеры с GC-зажимом достаточно дороги, поэтому метод используется ограниченно.
ССМ (chemical cleavage of mismatch) — метод химического расщепления неспаренных оснований. Метод основан на гибридизации радиоактивно меченой ДНК-пробы с тестируемой ДНК. Места ошибок затем выявляют с помощью серии химических реакций (модификация с использованием тетрахлорида осмия), которые происходят с однонитевой ДНК в сайтах неправильного спаривания. Этот метод может быть применен для тестирования фрагментов ДНК размером до 1 тыс. пар нуклеотидов, выявляет локализацию ошибки и является довольно чувствительным. Однако он не нашел широкого распространения вследствие токсичности применяемых химических реагентов и методической сложности. Подобное расщепление неспаренных нуклеотидов может быть и энзиматическим, что позволяет избежать токсических химикатов. Метод основан на расщеплении неспаренных оснований в гетеро-дуплексе, образуемом между тестируемой ДНК и нормальной последовательностью посредством таких ферментов, как резолваза фага Т4 или эндонуклеаза VII. Однако этот метод еще более «капризный», чем ССМ.
Заключительным этапом анализа мутаций является их секвенирование, т. е. определение нуклеотидной последовательности фрагмента ДНК, показавшего аномальную электрофоретическую подвижность. Последовательность нуклеотидов этого фрагмента сравнивается с нормой, в результате чего патология приобретает свою окончательную характеристику.
Метод секвенирования. Любые типы мутаций могут быть обнаружены путем прямого секвенирования мутантной кДНК или отдельных экзонов, и часто первичный поиск нарушений в кодирующих областях гена осуществляют именно таким образом. Для некоторых генов, имеющих небольшие размеры, метод прямого секвенирования с успехом применяется как основной метод сканирования мутаций. Так, в частности, особенно удобным оказалось его применение для детекции мутаций в сравнительно небольших по размеру генах, таких, как ген фактора IX свертывания крови (гемофилия В).
Разработанные в последние годы модификации методов ПЦР значительно облегчили секвенирование амплифицированных фрагментов и повысили его эффективность. Так, в частности, предложен вариант асимметричной ПЦР, когда при амплификации концентрация одного из олигопраймеров в несколько десятков раз превосходит концентрацию другого праймера, в результате чего синтезируется преимущественно только одна, нужная для секвенирования цепочка ДНК.
Врач лаборант-генетик заранее определяет стратегию поиска исходя из оснащенности лаборатории.
Многие мутации прерывают синтез белкового продукта. В этих случаях образуются укороченные полипептидные цепи, функционально незначимые. Для диагностики таких мутаций можно применять метод «трансляции белкового продукта». Он проводится в системе in vitro на основе полученной специфической мРНК с добавлением лизата ретикулоцитов (в нём содержатся все необходимые компоненты для синтеза белка). В этой системе синтезируется белковый продукт соответствующего гена. Продукт трансляции анализируют с помощью электрофореза. Изменение электрофоретической подвижности белка свидетельствует о наличии мутации (нонсенс-мутация, нарушение сплайсинга РНК, сдвиг рамки считывания), приводящей к «обрыву» синтеза полипептидной цепочки.
Косвенное выявление мутаций. Косвенное выявление мутаций применяется в тех случаях, когда нуклеотидная последовательность гена ещё не известна и вместе с тем имеется информация об относительном положении гена на генетической карте. Фактически это соответствует диагностике с помощью метода сцепления генов.
Косвенная ДНК-диагностика по существу сводится к анализу полиморфных генетических маркёров у больных и здоровых членов семьи. Маркёры должны быть расположены в том хромосомном регионе, где и ген болезни, т.е. они сцеплены. Такими маркёрами могут быть участки ДНК, существующие в популяции в нескольких аллельных вариантах. Отличия могут быть по составу нуклеотидов, по числу динуклеотидных повторов. На основе вариабельности состава маркерных участков ДНК можно дифференцировать материнское или отцовское происхождение конкретного варианта маркёра, сцепленного с геном болезни. Сцепление означает, что маркёр и ген болезни располагаются близко друг от друга; они передаются в составе одного хромосомного сегмента. Благодаря анализу полиморфных генетических маркёров можно проследить в ряду поколений наследование каждой из родительских хромосом.
Технические приёмы в косвенной диагностике те же самые, что и в прямой диагностике (получение ДНК, рестрикция, электрофорез и т.д.). Естественно, к этому добавляется математический анализ сцепления признаков.
Использование косвенных подходов оказалось возможным благодаря существованию в геноме полиморфных участков (локусов) ДНК. Нуклеотидные замены достаточно часто встречаются в некодирующих участках ДНК. Значительное число нуклеотидных замен приводит к изменению мест рестрикции. Эти изменения можно выявить с помощью блот-гибридизации по Саузерну, поскольку изменяется длина рестриктных фрагментов. Эта разновидность полиморфизма ДНК получила название полиморфизма по длине рестриктных фрагментов.
Расположенный вблизи изучаемого гена или внутри него полиморфный сайт может служить маркёром аллельных вариантов этого гена, в том числе маркёром патологических мутаций.
Полиморфизм, обусловленный нуклеотидными заменами или делециями, как правило, диаллелен, а значит, его информационная ценность ограничена. Более информативными являются кластеры тандемных повторов, которые обусловливают полиморфизм по количеству копий (VNTR — variable number of tandem repeates), так называемый полиморфизм мини- и микросателлитных последовательностей.
Микросателлиты — короткие тандемные повторы, обычно дву-гексануклеотидные. Самым распространённым из них является СА-повтор. Показано, что кластеры СА-повторов встречаются в среднем 1 на 30 тыс. пар нуклеотидов. Они локализованы, как правило, в некодирующих районах ДНК. Блоки СА-повторов демонстрируют менделевское наследование в семьях и не обнаруживают новых мутаций. Немаловажным положительным фактором является относительная простота обнаружения таких повторов в геноме человека. Кроме СА-повторов, достаточно распространены GA-повторы и другие кластеры тандемных повторов (ТТТА)п; (ТСТА)п; (ТТТС)п, также обнаруживающие вариабельность по числу повторов. Широкая распространённость в геноме (частота различных микросателлитов, взятых вместе, составляет 1 на 6 тыс. пар нуклеотидов), высокий уровень полиморфизма делают микро- и минисателлиты идеальными полиморфными маркёрами для картирования генов наследственных заболеваний и проведения косвенной ДНК-диагностики.
Полиморфные ДНК-маркёры и интегральная карта их расположения позволяют определить и проследить в поколениях хромосому, несущую патологический ген, а также подробнейшим образом охарактеризовать определённый хромосомный район, выявить субмикроскопические перестройки, определить наименьший район их перекрывания и локализовать ген-кандидат, ответственный за заболевание.
Основной недостаток косвенных методов диагностики — обязательное предварительное изучение генотипа (гаплотипа) хотя бы одного поражённого родственника. В случае отсутствия поражённых родственников, «доступных» для обследования, проведение диагностики (за редким исключением) становится невозможным.
Итак, даже из схематического описания нетрудно понять, что существует достаточно много молекулярно-генетических методов диагностики наследственных болезней. Эти методы оказались настолько универсальными, что нашли применение не только в медицинской генетике, но и в диагностике инфекционных заболеваний. Для каждого из методов имеется много вариантов. Одни и те же болезни можно диагностировать разными методами. Отсюда нетрудно заключить, что есть большие возможности для диагностики болезни даже в трудных случаях (невозможность обследования родителей, малое количество биологического материала, отсутствие сведений о гене и т.д.).
Автоматизация существующих и разработка принципиально новых подходов к изучению структуры нуклеиновых кислот наряду с ускоренными темпами изучения генома человека и клонирования генов, ответственных за развитие моногенной патологии, позволяют прогнозировать появление в недалеком будущем средств диагностики большинства известных наследственных болезней человека.
Микрочипы. ДНК-микрочипы позволяют осуществлять автоматизированный и высокопроизводительный анализ сложных геномов. Эта технология в ее различных вариантах развивается очень интенсивно. Кратко рассмотрим принципы технологии и ее применения к медицинским проблемам. Простейший принцип микрочипа: в разные квадраты твердой подложки помещаются олигонуклеотиды, соответствующие разным аллелям одного гена. Например, представлено 3 аллельных олигонуклеотида, различающихся одной заменой, которые ковалентно прикреплены к подложке. Эти олигонуклеотиды соответствуют трем вариантам мононуклеотидного полиморфизма (SNP, single nucleotide polymorphism). Таким образом, каждому аллелю отведен на подложке свой квадрат. Зададимся вопросом, какой аллель или какие аллели данного локуса представлены в ДНК пациента. Этот вопрос решается с помощью гибридизации меченной радиоактивно или флюоресцентно пробы ДНК от пациента с микрочипом. Если в этой пробе представлен, например, только аллель 1, то гибридизация будет происходить только с тем квадратом, где иммобилизован олигонуклеотид 1. Если в пробе представлены 2 аллеля (1 и 2), то гибридизация будет происходить с двумя квадратами (1 и 2) и т. д. Микрочипы, содержащие связанные с подложкой олигонуклеотиды, будем далее определять как олигонуклеотидные микрочипы. ДНК-олигонуклеотидный чип, содержащий тысячи олигонуклеотидов, создается современными методами в течение 1 дня. Может быть приготовлена серия микрочипов, содержащая сотни тысяч олигонуклеотидов с заданной последовательностью. Как и в приведенном выше схематическом примере, техника анализа основана на физической гибридизации исследуемой ДНК с множеством олигонуклеотидов, иммобилизованных на твердой подложке. Такой подход предполагает заведомое знание структур аллелей. Его определяют как «приобретение пробы» (gain of probe). Незамедлительным применением такого подхода может стать анализ сцеплений. Если в семье с болезнью сцеплен один из аллелей маркера, тогда как другой аллель (аллели) сцеплен со здоровым геном, то анализ сцеплений может быть выполнен следующим образом:
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 2715; Нарушение авторских прав?; Мы поможем в написании вашей работы!