
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фазовые диаграммы
|
|
|
|
Фазовое равновесие бинарных систем в процессах перегонки.
Если система состоит из двух компонентов (К=2) и между ними не происходит химического взаимодействия, то при наличии жидкой и паровой фаз число фаз Ф=2. Согласно правилу фаз, число степеней свободы такой системы составляет: С = К + 2 – Ф = 2 + 2 – 2 = 2
Следовательно, из трёх независимых параметров, полностью определяющих состояние системы, - температуры, давления и концентрации одной из фаз – можно произвольно выбрать любые два; при этом определится значение третьего параметра, которое уже не может быть произвольным. Однако при анализе и расчёте процессов перегонки жидкостей одну из переменных обычно закрепляют и строят так называемые фазовые диаграммы в плоской системе координат. При этом возможны следующие варианты фазовых диаграмм: Р – t (x=const); P – x (t=const); t – x (P=const). Вид этих зависимостей определяется взаимной растворимостью компонентов жидкой смеси и другими их свойствами. Смеси с неограниченной взаимной растворимостью компонентов делятся на идеальные и реальные. Идеальными называются растворы, подчиняющиеся закону Рауля. При смешивании компонентов идеального раствора тепловой эффект отсутствует и объём смеси практически не изменяется.
Для технических расчётов наиболее важной является диаграмма t – x,y, т.к. обычно процессы перегонки в промышленных аппаратах протекают при P=const, т.е. в изобарных условиях. На этой диаграмме по оси абсцисс отложены концентрации жидкой х и паровой у фаз, отвечающие разным температурам.
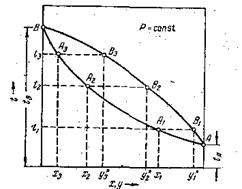
| Рис. 29. Зависимость температур кипения и конденсации от состава фаз (диаграмма t – x,y) |
Для построения зависимости температур кипения и конденсации соответственно от состава жидкости или пара, т, е. диаграммы t – x,y, (рис. 29), откладывают на оси ординат при постоянном внешнем давлении, температуры кипения t1, t2, t3, соответствующие составам жидких смесей х1, х2, х3, отложенным на оси абсцисс. Через полученные точки и точки, отвечающие температурам кипения чистых компонентов tA и tB, откладываемых на крайних ординатах диаграммы, проводят линию кипения АА1А2А3В.
Затем на оси абсцисс откладывают определенные по закону Рауля равновесные составы паров у1*, у2*, у3* и проводят из соответствующих им точек прямые до пересечения с изотермами, отвечающими температурам t1, t2, t3. Соединив точки пересечения В1, В2, В3..., с точками А и В плавной кривой, получают линию конденсации А В1В2В3В.
При пользовании диаграммой на оси абсцисс откладывают состав жидкой смеси и проводят из соответствующей точки вертикаль до пересечения с линией кипения. Далее из точки пересечения проводят горизонталь вправо до пересечения с линией конденсации. Абсцисса точки пересечения указывает состав равновесного пара.
На фазовой диаграмме у—х (рис. 30) наносится линия равновесия выражающая в данном случае зависимость между равновесными составами (по низкокипящему компоненту) жидкой (хА) и паровой (уА*) фаз. Процессы перегонки осуществляют обычно при постоянном внешнем давлении. Поэтому диаграмма строится при Р = соnst, т. е. для переменных температур кипения, изменяющихся в зависимости от изменения состава жидкой смеси.
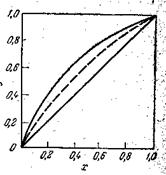
| Рис. 30. Диаграмма равновесия пар – жидкость (диаграмм у – х). |
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 864; Нарушение авторских прав?; Мы поможем в написании вашей работы!