
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Типы ядерных превращений
|
|
|
|
При написании уравнений реакций заряд частицы указывается в единицах элементарного заряда слева внизу от символа. В устаревший форме записи заряд и масса указывались справа от символа, но масса – вверху; заряд – внизу. Протоны и нейтроны входят в состав ядра и определяют свойства элемента.
Ядра элементов при написании уравнений реакций записываются в виде
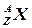 (
( ,
, 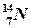 ),
),
где  – символ элемента;
– символ элемента;
Z – зарядовое число, которое показывает число протонов в ядре и определяется как порядковый номер элемента из ПСМ;
А – массовое число, показывает число нуклонов в ядре и определяется как атомная масса элемента из ПСМ, округлённая до целого значения;
N – число нейтронов в ядре, равное 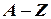 .
.
Если ядра двух атомов содержат одинаковое количество протонов, но разное количество нейтронов, они обозначаются обычно одним символом, обладают одинаковыми химическими свойствами и называются изотопами ( ,
, 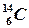 ).
).
Изотопы различаются по физическим свойствам, следовательно, химические свойства элемента зависят от числа протонов в ядре
 .
.
Известно около 280 устойчивых изотопов и более 1500 неустойчивых. Чем более устойчив изотоп, тем больше он распространён в природе, поэтому взятые в ПСМ массовые числа соответствуют наиболее стабильному изотопу данного элемента.
Ядра, у которых одинаковое количество нуклонов, но различное содержание протонов и нейтронов, называются изобарами
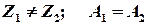 .
.
Изобары обозначаются различными символами, имеют различные химические и близкие физические свойства и не различимы при масс-спектрометрическом анализе. В природе изобары обычно встречаются парами. Известно около 60 устойчивых изобарных пар, в которых обычно чётные A и Z.
Два одинаковых по составу ядра, находящихся в различных энергетических состояниях, называют изомерами
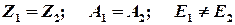 .
.
Изомерные состояния наблюдаются у всех ядер. Переход ядра из одного энергетического состояния в другое называется изомерным переходом. Изомерный переход из возбуждённого состояния в устойчивое является источником γ-излучений.
В соответствии с видами радиоактивных излучений существуют несколько видов радиоактивного распада (типов радиоактивных превращений). Радиоактивному превращению подвергаются элементы, в ядрах которых слишком много протонов или нейтронов. Рассмотрим виды радиоактивного распада.
1. Альфа–распад характерен для естественных радиоактивных элементов с большим порядковым номером (т.е. с малыми энергиями связи). Известно около 160 α–активных видов ядер, в основном порядковый номер которых более 82 (Z > 82).
Альфа–распад сопровождается испусканием из ядра неустойчивого элемента α–частицы, которая представляет собой ядро атома гелия Не (в его составе 2 протона и 2 нейтрона). Заряд ядра уменьшается на 2, массовое число – на 4.
Приводим общее уравнение α–распада и составление уравнений распада для урана и радия:
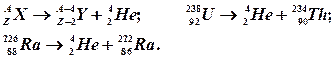
Альфа – распаду подвергается более 10% радиоактивных изотопов.
2. Бета–распад. Ряд естественных и искусственных радиоактивных изотопов претерпевает распад с испусканием электронов или позитронов.
Бета–распад может быть трех видов:
а) электронный β–распад характерен как для естественных, так и для искусственных радионуклидов, которые имеют излишек нейтронов. Этот распад в основном характерен для тяжелых радиоактивных изотопов. Электронному β–распаду подвергается около 46 % всех радиоактивных изотопов. При этом один из нейтронов превращается в протон, а ядро испускает электрон и антинейтрино. Заряд ядра и, соответственно, атомный номер элемента при этом увеличиваются на единицу, а массовое число остается без изменения.
Приводим общие уравнения β–– распада:
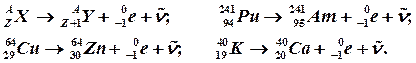
При испускании β–частиц ядра атомов могут находиться в возбужденном состоянии, когда в дочернем ядре обнаруживается избыток энергии, которая не захвачена корпускулярными частицами. Этот излишек энергии высвечивается в виде g–квантов
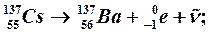
б) позитронный β+–распад. Наблюдается у некоторых искусственных радиоактивных изотопов, у которых в ядре имеется излишек протонов. Он характерен для 11 % радиоактивных изотопов, находящихся в первой половине таблицы Д.И.Менделеева (Z<45). При позитронном β–распаде один из протонов превращается в нейтрон, заряд ядра и, соответственно, атомный номер уменьшаются на единицу, а массовое число остается без изменений. Ядро испускает позитрон и нейтрино.
Приводим общее уравнение β+– распада:

Позитрон, вылетев из ядра, срывает с оболочки атома «лишний» электрон или взаимодействует со свободным электроном, образуя пару «позитрон–электрон», которая мгновенно превращается в два g–кванта с энергией, эквивалентной массе частиц. Процесс превращения пары «позитрон–электрон» в два g–кванта получил название аннигиляции (уничтожения), а возникающее электромагнитное излучение – аннигиляционного. В данном случае происходит превращение одной формы материи (частиц вещества) в другую – g–фотоны;
в) электронный К–захват. Это такой вид радиоактивного превращения, когда ядро атома захватывает электрон из ближайшего к ядру энергетического К–уровня (электронный К–захват) или, реже, в 100 раз – из L уровня. В результате один из протонов ядра нейтрализуется электроном, превращаясь в нейтрон. Порядковый номер нового ядра становится на единицу меньше, а массовое число не изменяется. Ядро испускает антинейтрино. Освободившееся место, которое занимал в К или L–уровне захваченный электрон, заполняется электроном из более удаленных от ядра энергетических уровней. Избыток энергии, освободившийся при таком переходе, испускается атомом в виде характеристического рентгеновского излучения.
Приводим общие уравнения К–захвата:
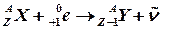 – рентгеновское излучение;
– рентгеновское излучение;
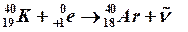 – рентгеновское излучение;
– рентгеновское излучение;
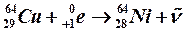 – рентгеновское излучение.
– рентгеновское излучение.
Электронный К–захват характерен для 25% всех радиоактивных ядер, но в основном для искусственных радиоактивных изотопов, расположенных в другой половине таблицы Д.И. Менделеева и имеющих излишек протонов (Z = 45 – 105). Только три естественных элемента претерпевают К–захват: калий–40, лантан–139, лютеций–176 (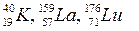 ).
).
Некоторые ядра могут распадаться двумя или тремя способами: путем α и β–распада и К–захвата.
Калий–40 подвергается, как уже отмечалось, электронному распаду –88% и К–захвату – 12%. Медь–64 (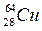 ) превращается в никель (позитронный распад – 19%, К-захват – 42%; (электронный распад – 39%).
) превращается в никель (позитронный распад – 19%, К-захват – 42%; (электронный распад – 39%).
3. Испускание g–излучения не является видом радиоактивного распада (при этом не происходит превращение элементов), а представляет собой поток электромагнитных волн, возникающих при α– и β–распаде ядер атомов (как естественных, так и искусственных радиоактивных изотопов), когда в дочернем ядре оказывается избыток энергии, не захваченный корпускулярным излучением (α– и β– частицей). Этот избыток мгновенно высвечивается в виде g–квантов, что показано в нижеприведенных уравнениях:
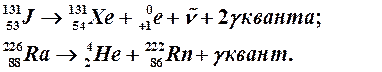
4. Протонная радиоактивность – испускание протона из ядра в основном состоянии. Этот процесс может наблюдаться у искусственно полученных ядер с большим дефицитом нейтронов:
лютеций — 151 ( ) — в нем на 24 нейтрона меньше, чем в стабильном изотопе
) — в нем на 24 нейтрона меньше, чем в стабильном изотопе 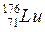
Таблица 1.2.
Сравнительная таблица ионизирующих излучений.
| Вид излучения | α- излучение | β- излучение | γ- излучение |
| Тип излучения | Непосредственно ионизирующее | Косвенно ионизирующее | |
| Природа излучения | Ядра гелия | Электроны или позитроны | Жесткое электромагнитное излучение |
| Источники излучения | Распад тяжелых ядер при участии сильных взаимодействий | Взаимные превращения нуклонов в легких и тяжелых ядрах при участии слабых взаимодействий | Изомерный переход ядра из возбужденного состояния в основное |
| Энергия излучения | 4 – 9 МэВ | 100КэВ – 3МэВ | 10КэВ – 3МэВ |
| Проникающая способность в воздухе | До 10 см. | До 1 м. | До 1000 м. |
| Проникающая способность в биологических тканях | Несколько микрон (мкм) | До 1 см. | До 1 м. |
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 2190; Нарушение авторских прав?; Мы поможем в написании вашей работы!