
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диспергаційні методи одержання дисперсних систем
|
|
|
|
МЕТОДИ ОДЕРЖАННЯ КОЛОЇДНО-ДИСПЕРСНИХ СИСТЕМ
Колоїдний розчин (золь) – це ультрамікрогетерогенна система, у якій дисперсійним середовищем є рідина, а дисперсною фазою – тверді частинки розміром
10–7 – 10–9 м.
Колоїдні розчини за ступенем дисперсності займають проміжне місце між грубодисперсними системами та молекулярно-йонними системами (істинними розчинами). Тому золі можна одержати або шляхом подрібнення відносно великих частинок до колоїдних розмірів, або внаслідок об'єднання окремих молекул чи атомів розчиненої речовини істинних розчинів. Відповідно до цього методи одержання колоїдно-дисперсних систем поділяють на диспергаційні та конденсаційні (рис. 2.1):
Грубодисперсні системи → Колоїдний розчин ← Істинні розчини
(d > 10–7 м) (d = 10–7–10–9) (d < 10–9 м)
Методи диспергування Методи конденсації.
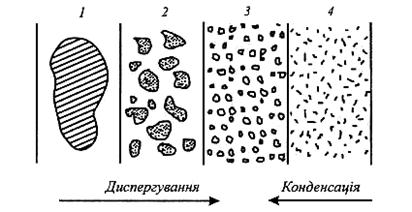
Рис. 2.1. Диспергаційні та конденсаційні методи одержання колоїдних розчинів: 1 – речовина; 2 – частинки грубої суспензії; 3 – міцели (колоїдний розчин); 4 – молекули та йони (істинний розчин)
В окрему групу виділено метод одержання колоїдних розчинів за допомогою пептизації.
Суть цих методів зводиться до подрібнення крупніших частинок до колоїдного ступеня дисперсності. При диспергуванні речовини витрачається робота на створення нової поверхні, що супроводжується збільшенням вільної поверхневої енергії. Залежно від виду витраченої енергії, ці методи поділяють на механічні, електричні та акустичні.
Механічне диспергування полягає у подрібненні, розтиранні речовини у спеціальних промислових і лабораторних пристроях – млинках. Найпоширенішими є кульові і планетарні млинки (грубе диспергування до частинок розміром 10–4–10–5 м), а також вібромлинки і колоїдні млинки, в яких речовина подрібнюється до колоїдного стану. Краще диспергування твердих речовин здійснюється при змочуванні їх рідинами з додаванням поверхнево-активних речовин, високомолекулярних сполук, електролітів. Останні виступають не тільки як стабілізатори, а й забезпечують розклинювальний ефект (ефект Ребіндера), який полегшує диспергування.
Електричні методи диспергування ґрунтуються на тому, що крізь рідке дисперсійне середовище, наприклад воду, пропускають електричний струм між електродами, які виготовлені з металу, колоїдний розчин якого хочуть одержати. Ці методи поєднують процеси диспергування, і конденсації: за температури вольтової дуги (метод Бредіга), або в іскровому високочастотному розряді (метод Свердберга) матеріал електродів диспергується і випаровується, а потім пара конденсується в охолодженому дисперсійному середовищі з утворенням колоїдного розчину.
Акустичні методи диспергування ґрунтуються на використанні спрямованого ультразвукового поля, тобто коливань великої частоти (105–106 Гц), які утворюються за допомогою спеціальних приладів. Диспергування відбувається внаслідок кавітаційного руйнування, тобто швидкого чергування стиснень і розріджень, і великого імпульсного тиску (порядку тисяч атмосфер). Так одержують високодисперсні емульсії і суспензії, придатні для внутрішньовенного введення. Крім того, під дією ультразвуку відбувається стерилізація колоїдних розчинів, суспензій, емульсій, тому що кавітація викликає руйнування мікроорганізмів.
Фізико-хімічне диспергування (пептизація). Пептизацію тільки умовно можна віднести до диспергаційних методів одержання колоїдних розчинів, оскільки в цьому методі відсутній процес подрібнення частинок великого розміру до колоїдного ступеня дисперсності. Процес пептизацїі полягає в дезагрегації частинок свіжодобутого осаду під дією пептизатора – стабілізатора, яким є електроліт, який надає системі агрегативної стійкості. Так одержують золі зі свіжодобутих осадів гідроксидів Цинку, Феруму, Алюмінію.
Розрізняють три способи пептизації: адсорбційну (безпосередню), дисолюційну (хімічну або посередню), а також промивання осаду розчинником (дисперсійним середовищем).
Адсорбційна пептизація відбувається тоді, коли до промитого дистильованою водою осаду додають електроліт, який містить йон, що може вибірково адсорбуватись на агрегаті, утворюючи міцелу. Наприклад, золь ферум (ПІ) гідроксиду можна одержати за реакцією:
FeCl3 + 3NH4OH = Fe(OH)3 (т) + 3NH4Cl
одержують червоно-бурий осад Fe(OH)3. Осад фільтрують, декілька разів промивають дистильованою водою, вимиваючи йони електролітів. При додаванні невеликої кількості пептизатора – солі FeCl3 – осад дезагрегується, утворюючи червоно-бурий золь Fe(OH)3. Будова міцели золю така:
{[(m Fe(OH)3) nFe3+]3n+ 3(n– x)Cl–}3 x + 3 x Cl–
Такого самого ефекту можна досягти, використовуючи в ролі пептизатора розчин лугу.
За дисолюційної пептизації на частинках осаду адсорбуються не йони використаного електроліту, а продукти його взаємодії з поверхневими молекулами осаду. За такої пептизації дуже важливо, щоб кількість реагенту, який розчиняє осад, була малою, інакше може розчинитись весь осад.
Пептизація може також спостерігатись при додаванні до осаду неелектролітів (наприклад, багатоатомних спиртів), карбонових кислот. Молекули неелектролітів адсорбуються на частинках осаду і захищають їх від злипання.
Пептизації промиванням розчинником (дисперсійним середовищем) зазнають осади, які були одержані за умови значного надлишку одного із реагентів. У цьому випадку подвійний електричний шар на частинках осаду дуже стиснутий і електростатичні сили відштовхування між частинками осаду не виявляються. Щоб відновити останні і створити нормальну структуру подвійного електричного шару, необхідно зменшити концентрацію електроліту шляхом промивання осаду розчинником або дисперсійним середовищем. За цих умов надлишок електроліту вимивається і утворюється стійкий золь.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 6021; Нарушение авторских прав?; Мы поможем в написании вашей работы!