
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термические и калорические свойства реальных газов
|
|
|
|
Параметры состояния реального газа р, Т, v определяются через значения двух других параметров, т.е.
р=f1(v, T); v=f(р,T); T=f3(v, p), которые являются различными формами уравнения состояния. Поскольку эти параметры обладают свойствами функций состояния, можно их представить через полные дифференциалы:
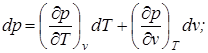
 ;
;
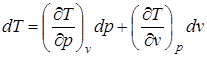 . (2.6)
. (2.6)
Из шести частных производных, приведенных в уравнениях, самостоятельное значение имеют только три, которые называются термическими коэффициентами
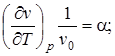
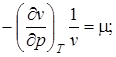
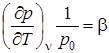 , (2.7)
, (2.7)
где 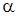 -термический коэффициент расширения (при р- const), характеризует интенсивность увеличения объема при нагревании;
-термический коэффициент расширения (при р- const), характеризует интенсивность увеличения объема при нагревании;
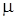 -термический коэффициент сжатия, характеризует интенсивность изменения объема при изменении давления в условиях T – const;
-термический коэффициент сжатия, характеризует интенсивность изменения объема при изменении давления в условиях T – const;
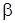 -термический коэффициент давления, характеризует интенсивность изменения давления при (v -const) изохорическом нагревании тела.
-термический коэффициент давления, характеризует интенсивность изменения давления при (v -const) изохорическом нагревании тела.
В указанных выше выражениях р0 и v0 – давление и удельный объем при температуре 0ºС.
Названные коэффициенты связаны между собой соотношением
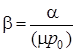 .
.
Последнее выражение позволяет вычислить коэффициент упругости, который экспериментально установить трудно, в то время, как 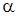 и
и 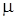 легко определяются опытным путем.
легко определяются опытным путем.
Калорические свойства газов описываются зависимостями через параметры состояния реального газа р, v. T следующего вида:
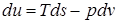 ;
;  ;
;
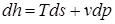 ;
;  ; (2.8)
; (2.8)
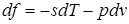 ;
; 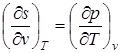 ;
;
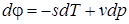 ;
; 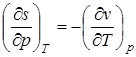 .
.
Эти дифференциальные зависимости называются уравнениями Максвелла.
Связь между теплоемкостями ср и сv для реального газа через термические коэффициенты описывается следующей формулой:
 . (2.9)
. (2.9)
Приведенное уравнение позволяет на основе экспериментальных значений ср вычислить сv, которую из опыта определить трудно.
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 811; Нарушение авторских прав?; Мы поможем в написании вашей работы!