
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Осмотическое давление растворов полимеров
|
|
|
|
Осмотическое давление растворов полимеров, как и у коллоидных растворов, имеет очень малую величину по сравнению с истинными растворами. Это объясня-ется малой численной концентрацией их в растворе из-за большего размера макро-молекул. Однако с увеличением концентрации раствора осмотическое давление растворов полимеров возрастает гораздо больше, чем это следует по закону Вант-Гоффа.
 Рис.5. Зависмость осмотического давления раствора от концентрации
Рис.5. Зависмость осмотического давления раствора от концентрации
| Такое непрямолинейное увеличение осмоти-ческого давления объясняется тем, что макро-молекула благодаря жесткости ведет себя в растворе как несколько более коротких молекул, т.е. самостоятельной подвижной единицей выступает не сама макромолекула, а её сегмент (отрезок цепи). Согласно Галлеру число таких сегментов увеличивается с повышением концентрации. Отсюда следует, что чем гибче макромолекула, тем |
больше осмотическое давление раствора полимера. Для расчёта осмотического давления растворов полимеров Галлер предложил уравнение:
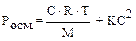
где М – молекулярная масса полимера, С – концентрация раствора, К – коэффи-циент, учитывающий длину, разветвленность и гибкость макромолекулы полимера.
Из всех коллигативных свойств растворов полимеров осмометрический метод оказался наиболее удобным при определении молекулярной массы полимера. Молекулярную массу полимера определяют графически по данным измерений осмотического давления растворов разной концентрации.

| С этой целью уравнение Галлера можно представить в виде уравнения прямой линии, поделив обе части его на концентрацию:
 и построить график зависимости Росм./С от концентрации. Отрезок, отсекаемый прямой на оси ординат равен RT/M, а тангенс угла наклона прямой равен К.
и построить график зависимости Росм./С от концентрации. Отрезок, отсекаемый прямой на оси ординат равен RT/M, а тангенс угла наклона прямой равен К.
|
Часть осмотического давления, создаваемого белками (альбумин, глобулины) как ВМС в плазме крови имеет большое физиологическое значение. Это давление называется онкотическим давлением. Его величина составляет 0,04 атм., тогда как общее осмотическое давление плазмы крови 7,4-7,8 атм. Онкотическое давление обеспечивает механизм всасывания межклеточной жидкости в капилляры венозной системы. При заболеваниях почек, печени, сопровождающихся потерями белка крови с мочой или недостатком его синтеза, онкотическое давление крови снижается. Это приводит к задержке жидкости в тканях и возникновению отёков. Применяемые при этом растворы альбумина снижают отёки и повышают онкотическое давление.
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 2445; Нарушение авторских прав?; Мы поможем в написании вашей работы!