
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экспериментальная часть. Дополнительная литература
|
|
|
|
Дополнительная литература
7.2.1. Бурштейн Э. А. Люминесценция белковых хромофоров. – М.: ВИНИТИ. Биофизика. Т.6,1976. – 216 с.
7.2.2. Аранович Г. И. и др. Справочник по физико-химическим методам исследования объектов окружающей среды. – Л.: Судостроение, 1979. – 648 с.
7.2.3. Скоупс Р. Методы очистки белков. – М.: Мир, 1985. – С. 310 – 315.
7.2.4. Практикум по биохимии. Под ред. С. Е. Северина и Г. А. Соловьевой. – М.: Изд-во Московского университета, 1989. – С. 80 – 88.
7.2.5. Троицкий Г. В. Дефектные белки. Постсинтетическая модификация. – Киев.: Наукова думка, 1991. – 232 с.
7.2.6. Tиц Н. и др. Руководство по клиническим лабораторным тестам. – М.: Пер. с англ. под ред. В. В. Меньшикова, 1997. – 960 с.
7.2.7. Камышников В. С. Справочник по клинико-биохимическим исследованиям и лабораторной диагностике. – МЕДПРЕСС-ИНФОРМ, 2004. – 920 с.
7.3.1. Количественное исследование белковых фракций крови биуретовым методом
Принцип метода: Пептидные группы денатурированных белков образуют в щелочной среде с ионами двухвалентной меди комплексы фиолетового цвета. Как видно из таблицы 7.2, интенсивность окраски пропорциональна количеству пептидных связей в пробах, в широком диапазоне концентраций белка. Однако, фотометрии мешают соли аммония, а йодиды и гликоляты меди, как и медные соли органических кислот, лучше сохраняют реагент и, специфичней к реакции с пептидными связями, чем ее сульфат. Поэтому многочисленные модификации метода различаются добавками в биуретовый реактив: йодида калия (KJ), полиолов (чаще глицерол) или солей ди- и трикарбоновых кислот (реактив Бенедикта).
Внимание! Помнить об агрессивности гидроксида натрия и приготовленного на нем биуретового реактива. В случае попадания их капель в глаза и на кожу, во избежание ожогов, промывать пораженное место проточной водой не менее 15 мин. По возможности нейтрализовать действие щелочи разбавленным (1-2 %) раствором уксусной или борной кислоты.
Ход работы: 1. В соответствии с таблицами 7.3 и 7.4, провести сквозную маркировку 8 пробирок.
2. Получить у лаборанта свои препараты белковых фракций крови, выделенных на предыдущем занятии и поместить их в штатив на рабочем столе.
3. Внести в пробирку с тенями эритроцитов 1 мл. 1н раствора гидроксида натрия, а в пробы с белковыми фракциями плазмы – по 1 мл 0,85% раствора хлорида натрия (физиологического раствора) и, оставить их в штативе, периодически помешивая.
4. В соответствии с таблицей 7.3, пипеткой на 1 мл внести в пробирки 1-5 указанные объемы основного стандартного раствора белка.
Таблица 7.3
Подготовка рабочих стандартных растворов для построения
калибровочного графика концентраций белка
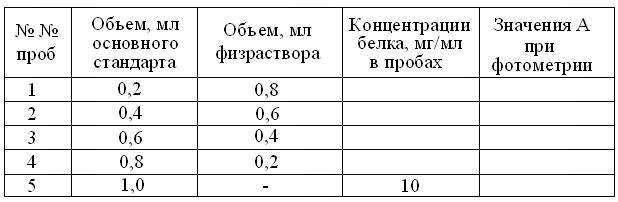
5. Другой пипеткой на 1 мл, довести с помощью физиологического раствора объемы рабочих стандартов до 1мл.
6. В соответствии с таблицей 7.4, полуавтоматическим дозатором на 100 мкл, соответственно меняя наконечники, внести в пробирки 6-8 соответствующие объемы образцов раствора Hb, теней эритроцитов, цельной плазмы крови.
Таблица 7.4
Содержание в крови белковых фракций
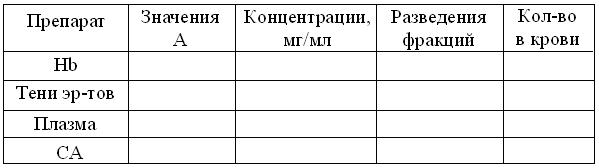
7. В каждую из 8 рабочих пробирок внести по 5 мл биуретового реактива.
8. Тщательно перемешать их содержимое и оставить в штативе на 30 мин. для развития окраски.
9. За это время, рассчитать для таблицы 7.3 полученные концентрации рабочих стандартов белка и вычертить соответствующую сетку координат калибровочного графика.
10. За 15 мин. до начала фотометрии, соответственно разделу 4.3.1, дежурный убеждается в исправности ФЭКа КФК-2 и включает его в электросеть для прогрева.
11. Фотометрию всех рабочих растворов проводить в строгом соответствии с разделом 4.3.1, в кювете толщиной 10 мм при зеленом светофильтре (540 – 560 нм), против биуретового реактива, занося значения А рабочих стандартных растворов в таблицу 7.3 протокола занятия.
12. Значения А всех растворов препаратов внести в таблицу 7.4, для
последующих расчетов содержания соответствующих фракций в крови.
13. По данным таблицы 7.3 построить калибровочный график зависимости между величинами абсорбции и концентрациями растворов рабочих стандартов белка.
14. С помощью калибровочного графика определить концентрации белка в растворах фракций крови.
15. При желании, с учетом объема субстратов и добавленных к ним реагентов (Занятие 6), подсчитать разведения фракций и рассчитать их концентрации в исходном образце крови.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 423; Нарушение авторских прав?; Мы поможем в написании вашей работы!