
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет горения топлива
|
|
|
|
ЗАДАНИЕ.
ОПРЕДЕЛЕНИЕ РАСХОДА ТОПЛИВА. ТЕПЛОВОЙ БАЛАНС ПЕЧИ
Расход топлива наиболее точно можно определить на основании расчета теплового баланса, состоящего из двух количественно одинаковых частей: приходной Qпpиx и расходной Qpacx. В соответствии с законом сохранения энергии Qпpиx = Qpacx. В приходную часть входят статьи подвода теплоты с топливом, подогретым воздухом и экзотермическими реакциями, а в расходную — расход ее на нагрев обрабатываемого материала и на потери в окружающую среду.
Перед расчетом теплового баланса необходимо иметь эскиз рассчитываемой печи с размерами кладки, окон и каналов для удаления продуктов сгорания.
Для печей непрерывного действия баланс составляют на 1 с или 1 ч работы печи, а периодического действия — на цикл работы или операцию (отжиг и т. д.).
Зависимости необходимы для расчета теплового баланса печи рассмотрены в п.5 - «Тепловой баланс. Определение расхода топлива».
ДАННЫЕ ДЛЯ ВЫПОЛНЕНИЯ ЗАДАНИЯ
Все студенты получают индивидуальное задание в соответствии с порядковым номером в журнале академической группы. Исходные данные приведены в приложении 2.
Выполненное задание должно содержать следующие разделы:
1. Расчет горения топлива.
2. Расчет времени нагрева заданной заготовки для ковки (штамповки) в камерной печи
3. Определение размеров рабочего пространства печи. Эскиз пода печи (с расположенными на нем заготовками).
4. Выбор кладки. Компоновка печи. Эскиз печи.
5. Тепловой баланс. Определение расхода топлива.
6. Основные технико-экономические показатели работы печи.
Исходные данные для выполнения расчетного задания приведены в таблице 1 (Приложение 3).
3.1. Расчет горения газообразного топлива.
3.1.1 Записать состав топлива соответствующий заданию (№ варианта):
CH4 + СmHn + СО + Н2 + H2S + SO2 + CO2 + О2 + N2 = 100 %.
3.1.2 Определение количества воздуха необходимого для полного сгорания топлива.
1) Количество кислорода необходимое для горения:
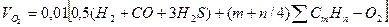
2) Количество теоретически необходимого воздуха:
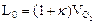 ,
,
где k- отношение объемного содержания азота к кислороду в обычном воздухе, не обогащенного кислородом, k = 3,76
3) Действительное количество воздуха необходимого для горения:
Lα = αL0,
где α – коэффициент избытка воздуха заданный в условии задачи, предусматривающий некачественное смесеобразование.
3.1.3 Количество и состав продуктов горения (ПГ):
Продукты горения содержат следующие элементы и соединения: RO2 (RO2=CO2+SO2), Н2О, N2 и О2.
1) Объем RO2 (RO2=CO2+SO2), в м3/м3:
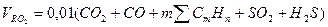 .
.
2) Водяной пар образуется при горении углеводородов, водорода и сероводорода. Тогда количество водяного пара в продуктах полного горения, м3/м3:
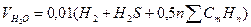 .
.
3) Объем азота, м3/м3:
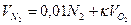 .
.
4) Объем избыточного кислорода, м3/м3:
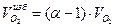
5) Объем избыточного азота, м3/м3:
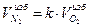
6) Суммарный объем азота, м3/м3:
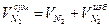
7) Теоретическое количество продуктов сгорания (дыма):
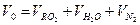
8) Общее количество продуктов сгорания (дыма):
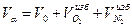
9) Состав продуктов сгорания (дыма), %:
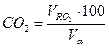
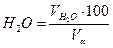
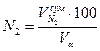
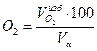
10) Плотность продуктов сгорания, кг/м3:
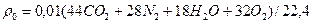
3.1.4 Определение температуры горения топлива по формуле Менделеева:
1) Теплота сгорания газа, кДж/м3:
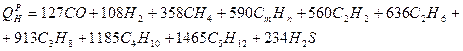
2) Химическая энтальпия продуктов сгорания, кДж/м3:
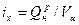
3) Энтальпия воздуха, кДж/м3(в случае его подогрева):
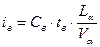 ,
,
где С – теплоемкость воздуха при заданной температуре tв, находим ее из таблицы приведенной ниже, tв – температура воздуха заданная в условии задачи.
| t,0C................... | |||||
| C, кДж/(м3.0С).. | 1,298 | 1,302 | 1,309 | 1,318 | 1,330 |
4) Энтальпия продуктов сгорания, кДж/м3:
i = ix+iв
5) Теоретическая температура сгорания, 0С:
Определив энтальпию продуктов сгорания i, методом интерполирования на интервале находим по таблице теоретическую температуру сгорания:
| i, кДж/м3 | |||||||||||
| t,0C……. |
Принцип метода интерполирования рассмотрим на примере:
Допустим мы получили i = 3055 кДж/м3
1. По таблице выбираем интервал на котором присутствует i = 3055 кДж/м3, это интервал между 2955 кДж/м3 и 3170 кДж/м3.
2. Затем определяем сколько 0С приходится на 1 кДж/м3 на этом интервале, делаем это следующим образом: (1900-1800)/(3170-2955)=0,4651 0С
3. Определяем сколько 0С приходится на участок от 2955 кДж/м3 до 3055 кДж/м3
tint=(3055-2955)*0,4651=100*0,4651=46,51 0С
4. Находим температуру соответствующую i = 3055 кДж/м3. Т.к. При i = 2955 кДж/м3 температура t = 1800 0С, а на интервале от 2955 кДж/м3 до 3055 кДж/м3 приходится Δt = 46,51 0С. То наша искомая температура t = 1800+46,51 = 1846,51 0С
6) Действительная температура сгорания, 0С:
Действительная температура горения tn, наблюдаемая в печи, всегда ниже теоретической, так как процесс горения сопровождается потерей теплоты печью в окружающую среду: чем больше теряется теплоты, тем ниже практическая температура сгорания:
tn=ηt
где η − пирометрический коэффициент; для нагревательных печей он равен 0,65—0,75.
Меньшие значения η принимают для камерных печей, большие – для
методических, карусельных и т.п. печей. В нашем случае используется камерная печь, η принимаем равным 0,65. Если же температура горения недостаточна, то коэффициент η необходимо повысить, приведя соответствующую мотивировку или повысить температуру подогрева воздуха.
3.2. Расчет горения жидкого топлива.
3.2.1 Определить состав рабочей массы топлива:
Следует сразу отметить что содержание азота и кислорода задано в виде (О2+N2)Г, поэтому для дальнейших расчетов необходимо разделить азот и кислород 50:50. Например вам задан (О2+N2)Г=0,9% тогда после разделения мы получим О2Г=0,45% и N2Г=0,45 %
В условиях заданий состав топлива зада в виде горючей массы топлива (СГ, НГ, SГ, О2Г, N2Г), поэтому необходим пересчет состава топлива на рабочую массу, формула для пересчета имеет следующий вид:
ХР=ХГ(100-WР-АР)/100
3.2.2 Записать состав рабочей массы заданного топлива:
Ср + Нр + Ор + Nр + Sр + Ар + Wр = 100%
3.2.3 Определение количества воздуха необходимого для полного сгорания топлива.
1) Количество кислорода необходимое для горения:
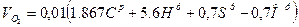
2) Количество теоретически необходимого воздуха:
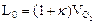 ,
,
где k- отношение объемного содержания азота к кислороду в обычном воздухе, не обогащенного кислородом, k = 3,76
3) Действительное количество воздуха необходимого для горения:
Lα = αL0,
где α – коэффициент избытка воздуха заданный в условии задачи
3.2.4 Количество и состав продуктов горения (ПГ):
1) Объем СO2, м3/кг:
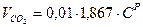 .
.
2) Суммарное количество водяного пара в продуктах горения, м3/кг:
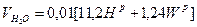 ,
,
где WФ водяной пар вносимый в топливо при разогреве. В нашем случае считаем что топливо не требует разогрева, принимаем WФ=0.
3) Объем SO2, м3/кг:
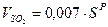 .
.
4) Объем избыточного кислорода, м3/кг:
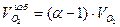
5) Объем азота, м3/кг:
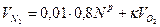
6) Объем избыточного азота, м3/м3:
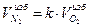
7) Суммарный объем азота, м3/м3:
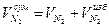
8) Теоретическое количество продуктов сгорания (дыма):
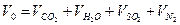
9) Суммарный объем продуктов сгорания, м3/кг:
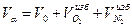
10) Состав влажных продуктов сгорания), %:
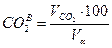
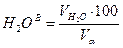
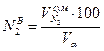
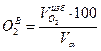
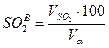
11) Состав сухих продуктов сгорания, %:
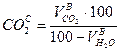
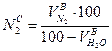
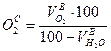
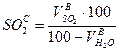
Результаты расчетов влажных и сухих продуктов сгорания записать в таблицу:
| CO2 | H2O | SO2 | O2 | N2 | Сумма, % | |
| Влажные | ||||||
| Сухие | – |
12) Плотность продуктов сгорания, кг/м3:
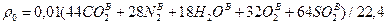 ,
,
где 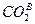 ,
, 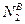 ,
, 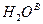 ,
, 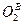 ,
, 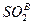 - процентное содержание соединений во влажных ПГ.
- процентное содержание соединений во влажных ПГ.
3.2.5 Определение температуры горения топлива:
1) Теплота сгорания мазута, кДж/м3:
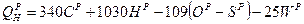
2) Химическая энтальпия продуктов сгорания, кДж/м3:
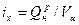
3) Энтальпия воздуха, кДж/м3:
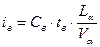 ,
,
где С – теплоемкость воздуха при заданной температуре tв, находим ее из таблицы приведенной ниже, tв – температура воздуха заданная в условии задачи.
| t,0C................... | |||||
| C, кДж/(м3.0С).. | 1,298 | 1,302 | 1,309 | 1,318 | 1,330 |
4) Энтальпия продуктов сгорания, кДж/м3:
i = ix+iв
5) Теоретическая температура сгорания, 0С:
Определив энтальпию продуктов сгорания i, методом интерполирования на интервале находим по таблице теоретическую температуру сгорания:
| i, кДж/м3 | |||||||||||
| t,0C……. |
Примечание: принцип метода интерполирования был рассмотрен ранее, п.3.1.4.
6) Действительная температура сгорания, 0С:
Действительная температура горения tn, наблюдаемая в печи, всегда ниже теоретической, так как процесс горения сопровождается потерей теплоты печью в окружающую среду: чем больше теряется теплоты, тем ниже практическая температура горения:
tn=ηt
где η − пирометрический коэффициент; для нагревательных печей он равен 0,65—0,75.
Меньшие значения η принимают для камерных печей, большие – для методических, карусельных и т.п. печей. В нашем случае используется камерная печь, η принимаем равным 0,65. Если же температура горения недостаточна, то коэффициент η необходимо повысить. Если же температура горения недостаточна, то коэффициент η необходимо повысить, приведя соответствующую мотивировку или повысить температуру подогрева воздуха.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 1660; Нарушение авторских прав?; Мы поможем в написании вашей работы!