
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Бериллий
|
|
|
|
Литий
Гелий
Гелий занимает вторую позицию в таблице Менделеева после водорода. Атомная масса гелия — 4,0026. Он представляет собой инертный газ без цвета. Его плотность — 0,178 грамм на литр. Сжижается гелий труднее всех известных газов лишь при температуре минус 268,93 градуса Цельсия и практически не отвердевает. Охлажденный до минус 270,98 градуса Цельсия гелий приобретает сверхтекучесть. Образуется гелий чаще всего в результате распада крупных атомов. На Земле он распространен в малых количествах, но на Солнце, где идет интенсивный распад атомов, гелия очень много. Все эти данные являются как бы паспортными и хорошо известны.
Займемся топологий гелия, и для начала определим его размеры. Учитывая, что атомная масса гелия в четыре раза больше водородной, а атом водорода в 1840 раз тяжелее электрона, получим массу атома гелия равной 7360 электронам; следовательно, общее количество эфирных шариков в атоме гелия составляет приблизительно 22 000; длина шнура атома и диаметр исходного тора соответственно равны 7360 и 2300 эфирным шарикам. Чтобы зримо представить соотношение толщины шнура исходного тора атома гелия и его диаметра, изобразим на листе бумаги ручкой окружность диаметром в 370 миллиметров, и пусть след от ручки имеет ширину в одну треть миллиметра; полученная окружность даст нам указанное представление. Один электрон (строенные эфирные шарики) будет занимать на нарисованной окружности всего лишь 0,15 миллиметров.
Скручивание исходного тора в законченную форму атома гелия происходит следующим образом. Сначала окружность сплющивается в овал, потом — в форму гантели, далее — в восьмерку, а затем петли восьмерки развертываются так, что возникает перехлест. Между прочим, перехлест у более крупных атомов не образуется, и объясняется это тем, что длина шнура у атома гелия пока еще не большая, и при стремлении средних точек шнура сблизиться — края (петли) вынуждены развернуться. Далее края изогнутся и начнут сближаться.
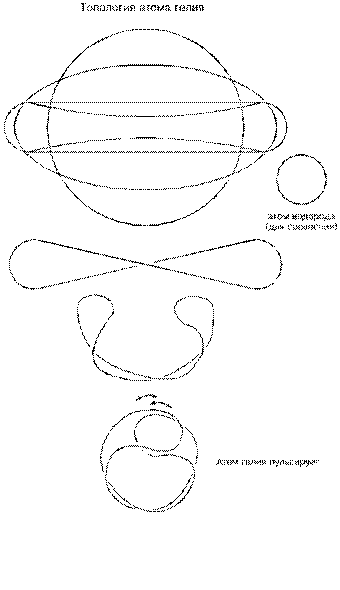
До этого момента топология атома гелия, как мы видим, схожа с топологией атома изотопа водорода — трития, но если у трития не хватало сил на замыкание краев (не хватало длины его шнура), то у гелия петли надвигаются одна на другую и таким образом замыкаются. Для того, чтобы убедиться в надежности соединения петель, достаточно проследить за расположением их присасывающих сторон: у внутренней петли она будет снаружи, а у внешней — изнутри.
Топологию атомов очень удобно представлять в виде проволочных моделей; для этого достаточно использовать в меру упругую, но достаточно пластичную проволоку. Атом водорода изобразится в виде обычного кольца. Увеличим длину куска проволоки в четыре раза (во столько раз атом гелия тяжелее атома водорода), свернем его в кольцо, спаяем концы и продемонстрируем процесс скручивания атома гелия. При скручивании мы должны постоянно помнить, что радиусы гибки не должны быть меньше радиуса кольца, представляющего собой атом водорода; это как бы условие, задаваемое упругостью шнура — торовых оболочек. (В натуре, напомним, минимальный радиус равнялся 285 эфирным шарикам.) Принятый минимальный радиус гибки определяет топологию всех атомов; и еще: следствием одинаковых радиусов гибки будут одинаковые размеры присасывающих петель (своего рода — их стандартизация), и поэтому-то они образуют устойчивую валентность, выраженную в способности соединять различные атомы между собой. Если бы петли имели различные размеры, их соединение было бы проблематичным.
Доводя процесс скручивания проволочной модели атома гелия до конца, мы обнаружим, что соединенные внахлест петли надвинуты одна на другую не до упора. Точнее говоря, они предпочли бы закрутиться еще дальше, но не пускает упругость шнура, то есть условие минимального радиуса. И при всякой попытке петель продвинуться навстречу еще дальше упругость шнура отбросит их назад; отскочив, они снова устремятся вперед, и снова упругость отбросит их назад; при этом атом гелия будет то съеживаться, то распускаться, то есть возникает пульсация. Пульсация, в свою очередь, породит стоячее тепловое поле вокруг атома и сделает его пушистым; так мы пришли к выводу, что гелий — газ.
На основании топологии можно объяснить и прочие физические и химические характеристики гелия. О его инертности, например, говорит то, что его атомов нет ни открытых присасывающих петель, ни присасывающих желобов: он не способен вообще соединяться с другими атомами, поэтому — всегда атомарен и практически не отвердевает. Цвета гелий не имеет потому, что у его атомов нет прямых “звучащих” участков шнуров; а сверхтекучесть у него возникает вследствие всякого отсутствия вязкости (слипание атомов), округлой формы и малого размера атома.
Как и у водорода, у гелия атомы не имеют одного размера: одни из них больше, другие — меньше, а в общем они занимают почти все весовое пространство от водорода (трития) до следующего за гелием лития; менее прочные изотопы гелия, конечно, давно уже распались, но и существующих в настоящее время можно насчитать не одну сотню.
В таблице Менделеева гелий лучше располагать не в конце первого периода — в одном ряду с водородом, а в начале второго периода перед литием, потому что его атом, как и атомы всего этого периода, представляет собой одиночную конструкцию (одиночный клубочек), в то время как атом следующего инертного газа неона выглядит уже в виде спаренной конструкции, похожей по этому признаку на атомы третьего периода.
Литий занимает третий номер в таблице Менделеева; его атомная масса равна 6,94; он относится к щелочным металлам. Литий — самый легкий из всех металлов: его плотность составляет 0,53 грамма в сантиметре кубическом. Он серебристо-белого цвета, с ярким металлическим блеском. Литий мягок и легко режется ножом. На воздухе он быстро тускнеет, соединяясь с кислородом. Температура плавления лития равна 180,5 градуса Цельсия. Известны изотопы лития с атомными весами 6 и 7. Первый изотоп используется для получения тяжелого изотопа водорода — трития; другой изотоп лития используется в качестве теплоносителя в котлах ядерных реакторов. Таковы общие физико-химические данные лития.
Топологию атомов лития начнем опять же с уяснения размеров исходного тора. Теперь мы знаем, что у каждого химического элемента, и в том числе у лития, существует большое количество изотопов, измеряемое сотнями и тысячами; поэтому размеры атомов будем указывать от … и до …. Но что значат эти пределы? Можно ли их определить точно? Или они указываются приблизительно? И каково количественное соотношение изотопов? Сразу скажем: однозначных ответов на поставленные вопросы нет; всякий раз необходимо внедряться в конкретную топологию атомов. Разберемся в этих вопросах на примере лития.
Как мы заметили, переход от протия к гелию с точки зрения топологии происходит планомерно: с увеличением размера исходного тора –постепенно изменяется окончательная конфигурация атомов. Но физические и, особенно, химические свойства атомов при переходе от протия к гелию изменяются более чем существенно, скорее — радикально: от всеобщей притягательности протия до полной инертности гелия. Где, на каком изотопе это произошло?
Подобные скачки свойств связаны с размерными скачками изотопов. Большой атом водорода (тритий), приобретающий очертания атома гелия, оказывается радиоактивным, то есть непрочным. Вызвано это тем, что его загнутые края петель не достигают друг друга, и можно представить, как они трепыхаются, устремленные навстречу. Они напоминают руки двух людей в расходящихся лодках, бессильно стремящихся дотянуться и сцепиться. Внешнее эфирное давление будет давить на консоли трепыхающихся петель атомов так сильно, что это до добра не доведет; получив со стороны даже небольшое дополнительное сдавливание, консоли отломятся — не выдержат крутого изгиба шнура, и атом разрушится; так оно и происходит. Поэтому можно сказать, что среди изотопов на границах существующих физико-химических переходов наблюдаются провалы: там изотопов просто нет.
Подобный провал существует между гелием и литием: если атом — уже не гелий, но еще не литий, то он непрочен, и его уже давно в земных условиях нет. Поэтому изотоп лития с атомным весом, равным шести, то есть с длиной шнура тора в 11 эфирных шариков, встречается очень редко и, как было сказано, используется для получения трития: его легко разорвать, укоротить и получить в результате изотоп водорода.
Таким образом, мы, вроде, определились с наименьшими размерами атома лития: это — 11 связанных электронов. Что же касается его верхнего предела, то тут возникает некоторая загвоздка: дело в том, что, согласно топологии, атом лития не имеет особых отличий от атома следующего за ним бериллия (мы в этом скоро убедимся), и между изотопами того и другого элементов нет никакого провала. Поэтому пока не станем указывать верхний предел размера атома лития.
Проследим за формообразованием атома лития. Исходная окружность только что возникшего микрозавихрения с указанными выше размерами будет стремится превратится в овал; только у лития овал — очень длинный: приблизительно в 8 раз длиннее диаметра концевого закругления (будущей петли); это — очень вытянутый овал. Начало свертывания атома лития похоже на такое же начало у больших атомов водорода и у гелия, но дальше происходит отклонение: восьмерка с перехлестом, то есть с разворотом петель, не возникает; дальнейшее сближение длинных сторон (шнуров) овала до полного их соприкосновения сопровождается одновременным загибом концов навстречу друг другу.
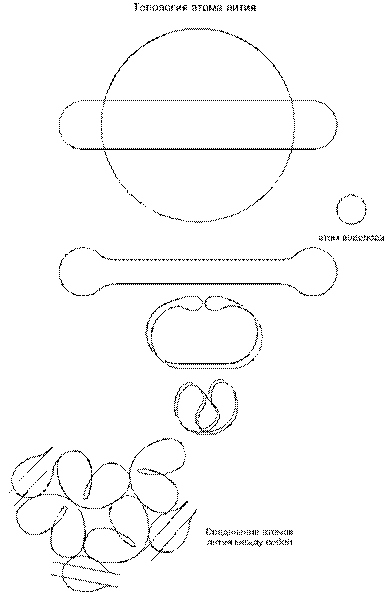
Почему не образуется восьмерка с перехлестом? Прежде всего потому, что овал очень длинный, и даже его полный прогиб в гантелю до соприкосновения шнуров в середине не вызывает их сильных изгибов; поэтому потенция разворота крайних петель — очень слабая. А во-вторых, развороту в какой-то степени противодействует начавшийся загиб концов овала. Другими словами: активный момент сил, стремящийся развернуть концевые петли, очень мал, а момент сопротивления развороту — большой.
Для наглядности воспользуемся резиновыми кольцами, например теми, что применяются в уплотнениях машин. Если пережимать кольцо малого диаметра, то оно обязательно свернется в восьмерку с перехлестом; а если выбрать кольцо большого диаметра, то его пережим до полного соприкосновения шнуров разворот концевых петель не вызывает. К слову: эти резиновые кольца также очень удобны для моделирования топологии атомов; если, конечно, имеется их широкий набор.
Загиб концов овала вызывается, как мы уже знаем, возмущением эфира между ними: чуть-чуть стронувшись с идеально прямого положения, они уже вынуждены будут сближаться до полного соприкосновения. Значит, в разные стороны концы отгибаться не могут. Но с направлением загиба у них есть выбор: либо так, что присасывающие стороны концевых петель окажутся снаружи, либо — изнутри. Первый вариант более вероятен, та как момент от сил отталкивания вращающихся оболочек шнура от прилегающего эфира на внешних точках петель будет больше, чем на внутренних.
Сближающиеся боковые стороны овала очень скоро войду в соприкосновение, смычка шнуров распространится от центра к концам и остановится только тогда, когда на концах окончательно сформируются петли с минимально допустимыми радиусами изгиба. Одновременно происходящие загибы и взаимное сближение этих петель приводят к столкновению их вершин, после чего в дело вступают их присасывающие стороны: петли, присасываясь, ныряют вглубь; и завершается процесс формирования конфигурации атома лития тем, что сместившиеся петли упираются своими вершинами в спаренные шнуры ровно по центру конструкции. Отдаленно такая конфигурация атома напоминает сердечко или, точнее, яблоко.
Напрашивается сам собой первый вывод: атом лития начинается тогда, когда вершины спарившихся первичных петель, нырнувшие внутрь конструкции, дотянутся до шнуров середины атома. А до того был еще не литий, а какой-то иной элемент, которого теперь уже нет в природе; его атом был крайне неустойчив, очень сильно пульсировал, был поэтому пушистым и относился к газам. Но и атом самого начального изотопа лития (мы его определили состоящим из 11 000 связанных электронов) тоже получается не очень прочным: радиусы изгиба его петель — предельные, то есть упругие шнуры изогнуты до предела, и при всяком внешнем воздействии они готовы лопнуть. У более крупных атомов это слабое место устраняется.
Представляя по результатам топологии образ атома лития, можно оценить то, что получилось. Две первичные петли замкнулись и нейтрализовались, также нейтрализованными оказались вторичные петли по обе стороны от первичных. Спаренные шнуры создали желоб, и этот желоб идет по всему контуру атома — он как бы замкнут в кольцо, — и его присасывающая сторона оказалась снаружи. Отсюда следует, что атомы лития могут соединяться и между собой и с другими атомами только с помощью своих присасывающих желобов; петлевое молекулярное соединение атом лития образовать не может.
Сильно выпуклые присасывающие желоба атомов лития могут соединяться между собой только на коротких участках (теоретически — в точках), и поэтому пространственная конструкция из соединившихся между собой атомов лития получается очень рыхлой и разреженной; отсюда — малая плотность лития: он почти в два раза легче воды.
Литий — металл; его металлические свойства вытекают из особенностей форм его атомов. Можно сказать по-другому: те особые свойства лития, которые обусловлены особыми формами его атомов и которые делают его непохожим физически и химически на другие вещества, названы металлическими; рассмотрим часть из них:
- электропроводность: она возникает по той причине, что атомы имеют кольцеобразную форму из спаренных шнуров, создающих присасывающие желоба, открытые наружу, охватывающие атомы по контуру и замыкающиеся сами на себе; электроны, прилипшие к этим желобам, могут беспрепятственно перемещаться по ним (напомним еще раз; что трудности возникают при отрыве электронов от атомов); а так как атомы соединяются между собой теми же желобами, то у электронов есть возможность перескакивать с атома на атом, то есть смещаться по телу;
- теплопроводность: упруго-изогнутые шнуры атома образуют чрезвычайно жесткую упругую конструкцию, которая практически не поглощает низкочастотные крупноамплитудные (тепловые) удары соседних атомов, а передает их дальше; и если бы не было в толще атомов всевозможных нарушений в их контактах (дислокаций), то тепловая волна распространялась бы с огромной скоростью;
- блеск: высокочастотные малоамплитудные удары световых волн эфира легко отражаются от напряженно изогнутых шнуров атомов и уходят прочь, подчиняясь законам волнового отражения; у атома лития нет прямых участков шнуров, поэтому у него нет собственного “звучания”, то есть нет собственного цвета — литий поэтому серебристо-белый с сильным блеском на срезах;
- пластичность: округлые атомы лития могут соединяться между собой как угодно; они могут, не разрываясь, обкатываться друг по другу; и это выражается в том, что тело из лития может менять свою форму, не теряя своей целостности, то есть быть пластичным (мягким); в результате литий режется без особого труда ножом.
На примере отмеченных физических особенностей лития можно уточнить само понятие металла: металл есть вещество, состоящее из атомов с круто изогнутыми шнурами, образующими контурные присасывающие желоба, открытые наружу; атомы ярко выраженных (щелочных) металлов не имеют открытых присасывающих петель и прямых или плавно изогнутых участков шнуров. Поэтому литий в нормальных условиях не может соединиться с водородом, так как атом водорода представляет собой петлю. Их соединение может быть только гипотетическим: при глубоком холоде, когда водород отвердевает, его молекулы могут соединяться с атомами лития; но по всему видно, что их сплав был бы таким же мягким, как сам литий.
Заодно уточним понятие пластичности: пластичность металлов определяется тем, что их округлые атомы могут обкатываться друг по другу, изменяя взаиморасположение, но не теряя контакты между собой.
Бериллий занимает четвертую позицию в таблице Менделеева. Его атомная масса равна 9,012. Он представляет собой светло-серый металл с плотностью 1,848 грамма в кубическом сантиметре и температурой плавления 1284 градуса Цельсия; он — твердый и в то же время хрупкий. Конструкционные материалы на основе бериллия обладают одновременно и легкостью, и прочностью, и стойкостью к высоким температурам. Сплавы бериллия, будучи в 1,5 раза легче алюминия, тем не менее прочнее многих специальных сталей. Свою прочность они сохраняют до температуры 700 … 800 градусов Цельсия. Бериллий стоек к радиации.
По своим физическим свойствам, как видно, бериллий сильно отличается от лития, но по топологии атомов они почти не различимы; отличие лишь в том, что атом бериллия как бы “сшит с запасом”: если атом лития напоминает тесный костюм школьника на взрослом человеке, то атом бериллия, наоборот, — просторный костюм взрослого на фигуре ребенка. Избыточная длинна шнура атома бериллия при одинаковой конфигурации его с литием образует более пологие очертания с радиусами изгибов, превышающими минимальные критические. Такой “запас” кривизны у атомов бериллия позволяет их деформировать вплоть до выхода на предел изгибов шнуров.
Топологическое сходство атомов лития и бериллия говорит о том, что четкой границы между ними нет; и невозможно сказать, какой наибольший размер имеет атом лития и какой наименьший — атом бериллия. Ориентируясь только на табличный атомный вес (а он усредняет все значения), можно считать, что шнур среднего по размерам атома бериллия состоит приблизительно из 16 500 связанных электронов. Верхний предел размеров атомов изотопов бериллия упирается в минимальный размер атома следующего элемента — бора, конфигурация которого резко отличается.
Запас по радиусам кривизны шнуров атомов бериллия сказывается в первую очередь на соединении их между собой в момент затвердевания металла: они примыкают друг к другу уже не короткими (точечными) участками как у лития, а длинными границами; контуры атомов как бы подстраиваются друг под друга, деформируясь и прилегая друг к другу максимально возможным образом; поэтому такие соединения очень прочны. Свою упрочняющую способность атомы бериллия проявляют и в соединениях с атомами других металлов, то есть в сплавах, в которых бериллий используется в качестве присадок к тяжелым металлам: заполняя пустоты и присасываясь своими гибкими желобами к атомам основного металла, атомы бериллия скрепляют их как клей, делая сплав очень прочным. Отсюда следует, что прочность металлов определяется длинами слипшихся участков присасывающих желобов атомов: чем длиннее эти участки, тем прочнее металл. Разрушение металлов происходит всегда по поверхности с самыми короткими слипшимися участками.
Запас по радиусам изгиба шнуров атомов бериллия позволяет им деформироваться без изменения соединений между собой; в результате деформируется все тело; это уже — упругая деформация. Упругая она потому, что в любом исходном состоянии атомы имеют наименее напряженные формы, а при деформации вынуждены терпеть некоторые “неудобства”; и стоит только деформирующей силе исчезнуть, как атомы возвратятся в свои исходные менее напряженные состояния. Следовательно, упругость металла определяется избытком длин шнуров его атомов, позволяющим их деформировать без изменения участков взаимного соединения.

С упругостью бериллия связана его жаропрочность; она выражается в том, что тепловые движения атомов могут происходить в пределах упругих деформаций, не вызывающих изменение соединений атомов между собой; поэтому в общем жаропрочность металла определяется, как и упругость, избытком длин шнуров его атомов. Снижение прочности металла при высоком нагреве объясняется тем, что тепловые движения его атомов уменьшают участки соединений их между собой; а когда эти участки полностью исчезают, происходит плавление металла.
Упругости бериллия сопутствует его хрупкость. Хрупкость может рассматриваться в общем случае как антипод пластичности: если пластичность выражается в возможности атомов изменять свои взаиморасположения с сохранением соединяющих участков, то хрупкость выражается, в первую очередь, в том, что у атомов такой возможности нет. Всякое взаимное смещение атомов хрупкого материала может происходить только при полном разрыве их связей; у этих атомов нет иных вариантов соединений. У упругих материалов (у металлов) хрупкость характеризуется еще и тем, что она — как бы прыгающая: возникшая в результате чрезмерных напряжений трещина с быстротой молнии распространяется по всему сечению тела. Для сравнения: кирпич под ударами молотка может крошиться (это — тоже хрупкость), но не раскалываться. “Прыгающая” хрупкость бериллия объясняется тем, что его атомы соединены между собой не лучшим образом, и все они напряжены; и стоит только нарушиться одной какой-то связи, как граничные атомы стремительно начнут “выпрямляться” в ущерб соединений со своими соседями; связи последних также начнут разрушаться; и этот процесс примет цепной характер. Следовательно, хрупкость упругих металлов зависит от степени деформаций соединенных между собой атомов и от отсутствия возможности изменения связей между ними.
Радиационная стойкость бериллия объясняется все тем же запасом в размерах его атомов: шнур атома бериллия имеет возможность спружинить под жестким радиационным ударом, не доходя до своей критической кривизны, и тем самым сохраниться неразрушенным.
И тем же можно объяснить светло-серый цвет бериллия и отсутствие у него яркого металлического блеска, такого, например, как у лития: световые волны эфира, падая на нежесткие шнуры поверхностных атомов бериллия, поглощаются ими, и только часть из волн отражается и создает рассеянный свет.
Плотность бериллия почти в четыре раза больше чем у лития только потому, что плотность шнуров его атомов выше: они соединяются между собой не в точках, а длинными участками. В то же время в сплошной своей массе бериллий — достаточно рыхлое вещество: он всего лишь в два раза плотнее воды.
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 945; Нарушение авторских прав?; Мы поможем в написании вашей работы!