
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение магния
|
|
|
|
Магний. В поверхностные воды магний поступает в основном за счет процессов химического выветривания и растворения доломитов, мергелей и других минералов. Значительные количества магния могут поступать в водные объекты со сточными водами металлургических, силикатных, текстильных и других предприятий.
| В речных водах содержание магния обычно колеблется от нескольких единиц до десятков миллиграммов в 1 дм3. |
Содержание магния в поверхностных водах подвержено заметным колебаниям: как правило, максимальные концентрации наблюдаются в меженный период, минимальные — в период половодья.
| ПДКвр ионов Мg2+ составляет 40 мг/дм3. |
Для определения содержания магния в незагрязненных поверхностных и грунтовых природных водах, как и в большинстве речных вод, можно применять расчетный метод по разности результатов определения общей жесткости и концентрации катиона кальция. Для анализа загрязненных вод на содержание магния необходимо применять прямое определение магния.
Массовую концентрацию катиона магния (Смг) в мг/л определяют расчетным методом, производя вычисления по формуле:
СМГ = (СОЖ – СКА•0,05) •12,16,
где СОЖ и СКА – результаты определения общей жесткости (мг-экв/л) и массовой концентрации катиона кальция (мг/л) соответственно; 0,05 – коэффициент пересчета концентрации катиона кальция в миллиграмм-эквивалентную форму; 12,16 – эквивалентная масса магния.
Полученный результат округлите до целых чисел (мг/л).
Карбонаты и гидрокарбонаты. Основным источником гидрокарбонатных и карбонатных ионов в поверхностных водах являются процессы химического выветривания и растворения карбонатных пород типа известняков, мергелей, доломитов, например:
CaCO3 + CO2 + H2O Û Сa2+ + 2HCO3-;
MgCO3 + CO2 + H2O Û Mg2+ + 2HCO3-.
Некоторая часть гидрокарбонатных ионов поступает с атмосферными осадками и грунтовыми водами. Гидрокарбонатные и карбонатные ионы выносятся в водоемы со сточными водами предприятий химической, силикатной, содовой промышленности и т.д.
По мере накопления гидрокарбонатных и особенно карбонатных ионов последние могут выпадать в осадок:
Ca(HCO3)2 Þ CaCO3 + H2O + CO2;
Сa2+ + CO32- Þ CaCO3.
| В речных водах содержание гидрокарбонатных и карбонатных ионов колеблется от 30 до 400 мг HCO3-/дм3, в озерах – от 1 до 500 мг HCO3-/дм3, в морской воде – от 100 до 200 мг/дм3, в атмосферных осадках – от 30 до 100 мг/дм3, в грунтовых водах – от 150 до 300 мг/дм3, в подземных водах – от 150 до 900 мг/дм3. |
Как отмечалось выше (в разделе «Щелочность и кислотность»), карбонаты и гидрокарбонаты представляют собой компоненты, определяющие природную щелочность воды. Их содержание в воде обусловлено процессами растворения атмосферного СО2, взаимодействия воды с находящимися в прилегающих грунтах известняками и, конечно, жизненными процессами дыхания всех водных организмов.
Определение карбонат- и гидрокарбонат-анионов является титриметрическим и основано на их реакции с водородными ионами в присутствии фенолфталеина (при определении карбонат-анионов) или метилового оранжевого (при определении гидрокарбонат-анионов) в качестве индикаторов. Используя эти два индикатора, удается наблюдать две точки эквивалентности: в первой точке (рН 8,0-8,2) в присутствии фенолфталеина полностью завершается титрование карбонат-анионов, а во второй (рН. 4,1-4,5) – гидрокарбонат-анионов. По результатам титрования можно определить концентрации в анализируемом растворе основных ионных форм, обуславливающих потребление кислот (гидроксо-, карбонат- и гидрокарбонат-анионов ), а также величины свободной и общей щелочности воды, т.к. они находятся в стехиометрической зависимости от содержания гидроксол-, карбонат- и гидрокарбонат-анионов.Для титрования обычно используют титрованные растворы соляной кислоты с точно известным значением концентрации 0,05 г-экв/л либо 0,1 г-экв/л.
Определение гидрокарбонат-анионов основано на реакции:
СО3 2- + Н+ =НСО3.
Присутствие карбонат-аниона в концентрациях, определяемых аналитически, возможно лишь в водах, рН которых более 8,0-8,2. В случае присутствия в анализируемой воде гидроксо-анионов при определении карбонатов протекает также реакция нейтрализации:
ОН-+Н+=Н2О.
Определение гидрокарбонат-анионовосновано на реакции:
НСО3-+Н+=СО2+Н2О.
Таким образом, при титровании по фенолфталеину в реакции с кислотой участвуют анионы ОН- и СО3 2-, а при титровании по метиловому оранжевому – ОН-, СО32- и НСО3-.
Величина карбонатной жесткости рассчитывается с учетом эквивалентных масс участвующих в реакциях карбонат- и гидрокарбонат-анионов.
При анализе карбонатных природных вод правильность получаемых результатов зависит от величины потребления кислоты на титрование по фенолфталеину и метилоранжу. Если титрование в присутствии фенолфталеина обычно не вызывает трудностей, т.к. происходит изменение окраски от розовой до бесцветной, то в присутствии метилового оранжевого, при изменении окраски от желтой до оранжевой, определить момент окончания титрования иногда довольно сложно. Это может привести к значительной ошибке при определении объема кислоты, израсходованной на титрование. В этих случаях, для более четкого выявления момента окончания титрования, определение полезно проводить в присутствии контрольной пробы, для чего рядом с титруемой пробой помещают такую же порцию анализируемой воды (во второй склянке), добавляя такое же количество индикатора.
В результате титрования карбоната и гидрокарбоната, которое может выполняться как параллельно в разных пробах, так и последовательно в одной и той же пробе, для расчета значений концентраций необходимо определить общее количество кислоты (V0) в миллилитрах, израсходованной на титрование карбоната (VK) и гидрокарбоната (VГК). Следует иметь в виду, что при определении потребления кислоты на титрование по метилоранжу (Vмо) происходит последовательное титрование и карбонатов, и гидрокарбонатов. По этой причине получаемый объем кислоты Vмо содержит соответствующую долю, обусловленнуюприсутствием в исходной пробе карбонатов, перешедших после реакции с катионом водорода в гидрокарбонаты, и не характеризует полностью концентрацию гидрокарбонатов в исходной пробе. Следовательно, при расчете концентраций основных ионных форм, обусловливающих потребление кислоты, необходимо учесть относительное потребление кислоты при титровании по фенолфталеину (Vф) и метилоранжу (Vмо). Рассмотрим несколько возможных вариантов, сопоставляя величины Vф и Vмо.
1. Vф = 0. Карбонаты, а также гидроксо-анионы в пробе отсутствуют, и потребление кислоты при титровании по метилоранжу может быть обусловлено только присутствием гидрокарбонатов.
2. Vф ¹ 0, причем 2Vф < Vмо. В исходной пробе отсутствуют гидроксо-анионы, но присутствуют и гидрокарбонаты, и карбонаты, причем доля последних эквивалентно оценивается как VК = 2VФ, а гидрокарбонатов – как VГК = VМО – 2VФ.
3. 2 VФ = Vмо. Гидрокарбонаты в исходной пробе отсутствуют, и потребление кислоты обусловлено содержанием практически только
карбонатов, которые количественно переходят в гидрокарбонаты. Именно этим объясняется удвоенное, по сравнению с Уф, потребление кислоты Vмо.
4. 2 VФ> Vмо. В данном случае в исходной пробе гидрокарбонаты отсутствуют, но присутствуют не только карбонаты, но и другие потребляющие кислоту анионы, а именно – гидроксо-анионы. При этом содержание последних эквивалентно составляет Vон = 2Vф – Vмо. Содержание карбонатов можно рассчитать, составив и решив систему уравнений:
VK + VOH = VMO
ÞVK = 2(VMO – VФ)
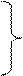 VOH = 2VФ – VMO
VOH = 2VФ – VMO
5. VФ = Vмо. В исходной пробе отсутствуют и карбонаты, и гидрокарбонаты, и потребление кислоты обусловлено присутствиемсильных щелочей, содержащих гидроксо-анионы.
Присутствие свободных гидроксо-анионов в заметных количествах (случаи 4 и 5) возможно только в сточных водах.
Массовые концентрации анионов (не солей!) рассчитываются на основе уравнений реакций потребления кислоты карбонатами (Ск) и гидрокарбонатами (Сгк) в мг/л по формулам:
Ск= Vк • 60 •1000
2 • VA
Сгк = (Vгк-Vк) • Н • 61• 1000,
VA
где Vк и Vгк – объем раствора соляной кислоты, израсходованной на титрование карбоната и гидрокарбонатасоответственно, мл;
Н – точная концентрация титрованного раствора соляной кислоты (нормальность), г-экв/л; VA – объем пробы воды, взятой для анализа, мл; 60 и 61 – эквивалентная масса карбонат- и гидрокарбонат-аниона соответственно, в соответствующих реакциях; 1000 – коэффициент пересчета единиц измерений.
Результаты титрования по фенолфталеину и метилоранжу позволяют рассчитать показатель щелочности воды, который численно равен количеству эквивалентов кислоты, израсходованной на титрование пробы объемом 1 л. При этом потребление кислоты при титровании по фенолфталеину характеризует свободную щелочность, а по метилоранжу – общую щелочность, которая измеряется в мг-экв/л. Показатель щелочности используется в России, как правило, при исследовании сточных вод. В некоторых других странах (США, Канаде, Швеции и др.) щелочность определяется при оценке качества природных вод и выражается массовой концентрацией в эквиваленте СаСО3.
Следует иметь в виду, что при анализе сточных и загрязненных природных вод получаемые результаты не всегда корректно отражают величины свободной и общей щелочности, т.к. в воде, кроме карбонатов и гидрокарбонатов, могут присутствовать соединения некоторых других групп (см. «Щелочность и кислотность»).
|
|
|
|
|
Дата добавления: 2014-12-26; Просмотров: 4183; Нарушение авторских прав?; Мы поможем в написании вашей работы!