
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фенолы
|
|
|
|
Реакции отщепления.
Отщепление молекул воды с образованием олефинов (внутримолекулярная дегидратация).
В общем случае реакция внутримолекулярной дегидратации (элиминирования) заключается в отщеплении воды от двух соседних (a, b) атомов углерода.
Этилены получаются при нагревании спирта с большим количеством кислоты или хлорида цинка, а также при пропускании паров спирта при 350-500 0 С через трубку с оксидом алюминия. Легче всего дегидратируются третичные, потом вторичные и затем уже первичные спирты. В реакциях отщепления воды от спирта наблюдается преимущественное отщепление протона от наименее гидрогенизированного углеродного атома (правило Зайцева) с образованием наиболее разветвленного олефина:
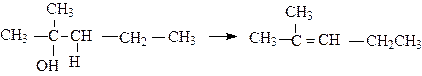
2-метилпентанол-2 2-метил-2-пентен
Реакции окисления.
1Первичные и вторичные спирты окисляются рядом реагентов (хромовой кислотой) с образованием альдегидов и кетонов соответственно:

Третичные спирты в этих условиях не окисляются.
Спирты, в которых гидроксильная группа непосредственно связана с атомом углерода ароматического ядра, называются фенолами.
 |
Фенол о-метилфенол, о-крезол
Фенол является сильным дезинфицирующим средством. Под названием “карболовая кислота” его используют в медицинских учреждениях. Дезинфицирующая жидкость “лизол” содержит 2-фенилфенол и 2-бензил-4-хлорфенол, которые обладают бактерицидным действием. Студенты, изучающие микробиологию, знают, что антимикробную активность соединений сравнивают с активностью фенола при помощи так называемого “фенольного коэффициента”.
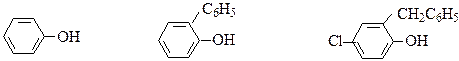 |
Фенол 2-фенилфенол 2-бензил-4-хлорфенол
Как показывает само название «карболовая кислота», фенолы характеризуются кислотными свойствами. Фенолы гораздо более сильные кислоты, чем спирты, хотя много слабее карбоновых и минеральных кислот и, как кислота, фенол на 9 порядков сильнее обычных алифатических спиртов. (рКа фенола 9.7).Следовательно, кислотные свойства у фенолов ярко выражены. В отличие от алифатических спиртов фенол реагирует с водными растворами щелочей, образуя феноксиды:
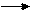 C6H5-OH + NaOH C6H5ONa +H2O,
C6H5-OH + NaOH C6H5ONa +H2O,
в то же время в реакцию со слабыми основаниями не вступают:
 C6H5OH + NaHCO3 /
C6H5OH + NaHCO3 /
Повышенные кислотные свойства фенолов объясняются тем, что свободная электронная пара кислорода в феноле оттянута к ядру (+ М эффект гидроксильной группы):
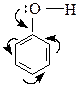 |
Повышение кислотных свойств фенолов имеет своим следствием понижение основных свойств. В отличие от алифатических спиртов фенолы практически не вступают в реакции нуклеофильного замещения. Наличие в феноле ароматического ядра позволяет получать различные производные фенолов реакциями электрофильного замещения (SE).Электронодонорная ОН - группа фенолов активирует бензольное кольцо к атаке электрофилами и, в общем, реакции фенолов протекают в значительно более мягких условиях, чем соответствующие реакции бензола. Hапример:
(3) Салициловая кислота (2) 2,4,6-трибромфенол
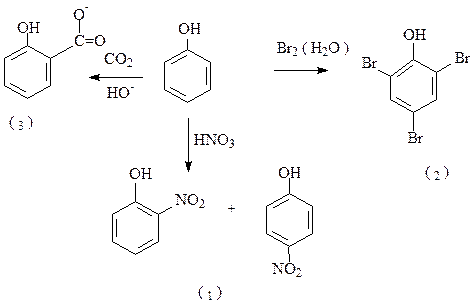 |
(1) 2-нитрофенол 4-нитрофенол
Активность фенолов в реакциях электрофильного замещения настолько велика, что даже альдегиды в присутствии кислоты реагируют с фенолом. На этой реакции основано получение фенолформальдегидных (бакелитовых) смол - дешевых и широко применяемых полимеров.

Фенол широко используется для получения лекарственных препаратов на основе салициловой кислоты.
Реакция получения салициловой кислоты является еще одним примером активации бензольного ядра под действием гидроксильной группы в щелочных условиях.
Окисление. Фенолы очень легко окисляются самыми разнообразными реагентами, включая атмосферный кислород.
В ряде случаев процесс окисления фенолов оказывается весьма сложным, протекающим с образованием радикалов. Последние являются достаточно устойчивыми вследствие сопряжения с бензольным ядром. На этом основано применение фенолов как ингибиторов в свободно-радикальных реакциях.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 935; Нарушение авторских прав?; Мы поможем в написании вашей работы!