КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение молекулы. Теория химической связи. Ионная связь Металлическая связь. Ковалентная связь. Энергия связи. Длина связи. Валентный угол. Свойства химической связи
|
|
|
|
Строение атома. Периодическая система Д.И. Менделеева. Состав ядра. Изотопы. Электронная оболочка. Атомная орбиталь. Квантовые числа. Принцип Паули. Принцип наименьшей энергии. Порядок заполнения энергетических уровней, подуровней. Периодическая система элементов Д.И. Менделеева в свете современной теории строения атома. Электронные семейства элементов. Валентные электроны. Периодическое изменение свойств химических элементов. Энергия ионизации и сродство к электрону. Электроотрицательность элементов. Металлические, неметаллические, амфотерные элементы.
Окружающий нас мир состоит из трёх структурных частиц: атом, молекула, ион. Например, медная пластина состоит из атомов (Сu). В водном растворе сульфата меди (СuSO4) медь присутствует в виде ионов (Сu2+). Атомы (Сu), ионы (Сu2+) являются структурными частицами химического элемента медь. Газ водород состоит из молекул (Н2). Раствор хлороводородной кислоты (НСl) содержит ионы (H+). Молекулы (Н2), ионы (H+) являются структурными частицами химического элемента водород.
Химический элемент – это вид структурных частиц с одинаковым зарядом ядра.
Атом – это наименьшая частица элемента, имеющая его химические свойства.
Согласно современной теории строения атома, атом состоит из ядра /протоны, нейтроны/ и электронной оболочки /электроны/.
Протон (р): относительный заряд равен +1; относительная масса 1,0073.
Нейтрон(n): относительный заряд равен 0; относительная масса 1,0087.
Электрон(е): относительный заряд равен –1; относительная масса 5,48 · 10-4
Периодическая система элементов Д.И.Менделеева позволяет определить число фундаментальных частиц (р,n,е) в атоме любого элемента. Английский физик Мозли установил, что «заряд ядра равен порядковому номеру элемента в Периодической системе». Так как заряд протона равен единице, то порядковый номер определяет число протонов. Атом по заряду - нейтральная частица, следовательно, число электронов в атоме равно числу протонов. Относительная атомная масса элемента определяется сумой масс протонов и нейтронов. Поэтому, число нейтронов в атоме равно атомной массе за вычетом числа протонов.
Пример 1. Определить число протонов, нейтронов, электронов в атоме элемента с порядковым номером 92 в Периодической системе элементов Д.И. Менделеева
Элемент Уран 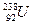
Число протонов (р) равно 92
Число нейтронов (n) равно 238 – 92 = 146
Число электронов (е) равно 92
Изотопы - это структурные частицы, имеющие одинаковое число протонов, но разное число нейтронов (частицы одного и того же элемента с различной массой).
Например 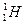 -водород,
-водород, 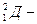 дейтерий,
дейтерий, 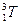 -тритий
-тритий
При рассмотрении строения электронной оболочки атома учитывается, что из-за корпускулярно-волновой природы электрона существует неопределённость в установлении его места пребывания. Шредингер предложил волновое уравнение для атома. Решение этого уравнения даёт плотность вероятности нахождения электрона в данной области пространства. Область пространства вокруг ядра, для которой вероятность пребывания электрона равна 95%, называется атомной орбиталью. Электрон не движется по орбите, а занимает трёхмерную область в пространстве вокруг ядра – орбиталь. Решения волнового уравнения Шредингера позволяют охарактеризовать орбиталь четырьмя квантовыми числами.
n – главное квантовое число. Может принимать значения 1,2,3,4,5,6,7…∞. Определяет энергетический уровень, на котором находится электрон, энергию электрона на уровне, размер орбитали. Чем больше значение главного квантового числа, тем больше энергия электрона и больше размер орбитали.
l-орбитальное квантовое число. Может принимать целочисленные значения от 0 до n-1. Если n = 4, то l = 0,1,2 и 3. Определяет энергетический подуровень, на котором находится электрон, энергию электрона на подуровне, а так же форму орбитали. Каждое значение l обозначают буквой (чтобы не путать с обозначением n): l = 0 (s), 1 (p), 2 (d), 3 (f) и т.д.
Состояние электрона, характеризуемое значениями l и n, записывается в виде электронной формулы.
Например, еслисостояние электрона характеризуется n = 4, l = 3, то говорят, что это - 4f-электрон.
Возможные следующие сочетания этих двух квантовых чисел:
n = 1 l = 0 1s
n = 2 l = 0,1 2s2p
n = 3 l = 0,1,2 3s3p3d
n = 4 l = 0,1,2,3 4s4p4d4f
и т.д.
В пределах одного энергетического уровня наименьшей энергией обладают электроны на s-подуровне (s-электроны), а затем s<p<d<f< и т.д.
Электроны на s-подуровне (s-электроны) имеют сферическую форму орбитали, p-электроны симметричную гантель, у других орбиталь имеет более сложную конфигурацию.

Рис. 1. Форма электронных облаков s и p - орбиталей
m-магнитное квантовое число. Может принимать значение целых чисел от +l до –l. Определяет возможное число орбиталей на подуровне, а так же пространственное расположение орбиталей.
Возможное число орбиталей для подуровней:
l = 0 (s) m = 0 одна s-орбиталь
l = 1 (p) m = 1,0,-1 три p-орбитали
l = 2 (d) m = 2,1,0,-1,-2 пять d-орбиталей и т. д.
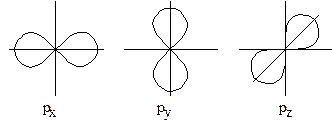
Рис. 2. Пространственное расположение р-орбиталей
S-спиновое квантовое число. Определяет вращение электрона вокруг собственной оси. Может принимать значения +1/2 (предполагает вращение по часовой стрелке) и –1/2 (вращение против часовой стрелки). Во многоэлектронных атомах электроны располагаются по энергетическим уровням (n), подуровням (l) и орбиталям (m). Если орбиталь изобразить в виде ячейки □, то структура электронной оболочки будет иметь вид:
 1
1
s



 2
2
s p








 3
3
s p d
4 














 и т.д.
и т.д.
s p d f
В соответствии с принципом Паули «в атоме не может быть двух электронов, которые имеют одинаковые наборы четырёх квантовых чисел». Таким образом, на одной орбитали могут находиться только два электрона с противоположными спинами.
Отсюда следует, что:
на n=1 уровне находится 2 электрона 1s2
на n=2 уровне находится 8 электронов 2s22р6
на n=3 уровне находится 18 электронов 3s23р63d10
на n=4 уровне находится 32 электрона 4s24р64d104f14 и т.д.
Заполнение электронной оболочки атома электронами происходит по принципу наименьшей энергии (правило Клечковского):
1. В первую очередь заполняется энергетическое состояние с наименьшей суммой главного и орбитального квантовых чисел(n+l). Последующее заполнение происходит в порядке увеличения суммы n+l.
2. При равных значениях суммы n + l заполняется энергетический уровень с меньшим значением главного квантового числа.
Пример 2. Определить порядок заполнения электронами уровней и подуровней 5d, 6p, 6s.
5d = 5 + 2 = 7; 6p = 6 + 1 = 7; 6s = 6 + 0 = 6.
Порядок заполнения 6s,5d,6р.

 Заполнение орбиталей внутри одного подуровня происходит по правилу Хунда «каждая орбиталь заполняется вначале одним электроном, а затем происходит их заполнение вторыми электронами».
Заполнение орбиталей внутри одного подуровня происходит по правилу Хунда «каждая орбиталь заполняется вначале одним электроном, а затем происходит их заполнение вторыми электронами».
 Например, р4:
Например, р4:
Электронные оболочки записываются в виде электронных формул.
Напимер,  1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p2
1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p2
Если сопоставить строение электронной оболочки атома и Периодическую систему элементов Д.И. Менделеева, то видно, что Периодическая система элементов Д.И. Менделеева представляет собой классификацию элементов по структуре заполненных электронных оболочек атомов.
Период – последовательный ряд элементов с одинаковым числом заполняемых энергетических уровней, причём номер периода показывает номер внешнего энергетического уровня.
Группа – последовательный ряд элементов, имеющих однотипную электронную конфигурацию.
Например, элемент 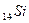 находится в 3 периоде, электронная формула: 1s22s22p63s23p2
находится в 3 периоде, электронная формула: 1s22s22p63s23p2
Элемент 52Sn находится в 5 периоде, электронная формула: 1s22s22p63s23p64s23d104p65s24d105p2
В зависимости от подуровня, который заполняет последний электрон, все элементы можно сгруппировать в четыре электронных семейства.
s – элементы – достраивается s - подуровень
p – элементы – достраивается p - подуровень
d – элементы – достраивается d - подуровень
f – элементы – достраивается f – подуровень
В Периодической системе элементов Д.И. Менделеева s- и р - элементы расположены в главных подгруппах, у этих элементов достраивается внешний энергетический уровень (соответствует номеру периода). d- и f-элементы расположены в побочных подгруппах, у этих элементов достраиваются предвнешние уровни.
Учитывая периодичность заполнения электронами энергетических уровней и взаимосвязь заряда ядра и количества электронов в атоме, Периодический закон Д.И Менделеева может быть сформулирован следующим образом: «свойства простых тел, а также соединений элементов находятся в периодической зависимости от заряда ядра атома».
Начинается период (со II периода) элементом, в атоме которого появился на внешнем уровне s-электрон (активный металл). Заканчивается период элементом в атоме, которого на внешнем уровне s2p6 – электроны (благородный газ). Все элементы в соответствии с электронным строением атома можно подразделить на металлические и неметаллические. Металлические свойства элементов определяются способностью атомов «отдавать» электроны (восстановительные свойства). Неметаллические свойства элементов определяются способностью атомов «принимать» электроны (окислительные свойства). Изменение свойств элементов в Периодической системе можно проследить в горизонтальном направлении (в периоде) и вертикальном направлении (в группе). С увеличением порядкового номера элементов по периоду (слева на право) происходит нарастание неметаллических свойств. Сверху вниз по подгруппам возрастают металлические свойства. Эти свойства связаны с атомными радиусами, а в конечном счете - с электроотрицательностью. Элементы, для которых электроотрицательность меньше двух относят к металлическим элементам (атомы только отдают электроны). Элементы, для которых электроотрицательность больше двух, относят к неметаллическим элементам. Чем ниже электроотрицательность, тем выше металлические свойства элемента и наоборот, чем выше электроотрицательность, тем выше неметаллические свойства.
КОНТРОЛЬНЫЕ ЗАДАНИЯ
55 Напишите электронные формулы атомов элементов с порядковыми номерами 35 и 47. Распределите электроны по квантовым ячейкам. К какому электронному семейству относятся элементы?
56 Напишите электронные формулы атомов элементов с порядковыми номерами 29 и 52. Определите, к какой группе Периодической системы Д.И. Менделеева принадлежит каждый из этих элементов?
57 Напишите электронные формулы ионов элементов Rb+ и Se2-. К какому электронному семейству относятся элементы?
58 Сколько неспаренных электронов содержится в электронной оболочке атомов элементов фосфора и скандия? Ответ обосновать.
59 Напишите электронные формулы атомов элементов алюминий и галлий. Какой элемент проявляет более металлические свойства. Ответ обосновать.
60 Напишите электронные формулы атомов элементов с порядковыми номерами 20 и 50. Распределите электроны по ячейкам. К какому электронному семейству относятся элементы?
61 Напишите электронные формулы атомов элементов с порядковыми номерами 22 и 49. Определите период и группу Периодической системы Д.И. Менделеева, в которых находятся элементы.
62 Напишите электронные формулы ионов элементов Mg2+ и J-. К какому электронному семейству относятся элементы?
63 Сколько свободных d – орбиталей в электронной оболочке атома ванадия и f – орбиталей в электронной оболочке атома урана.
64 Напишите электронные формулы атомов элементов сера и теллур. Какой элемент проявляет более неметаллические свойства? Ответ обосновать.
65 Напишите электронные формулы атомов элементов с порядковыми номерами 38 и 74. Распределите электроны по квантовым ячейкам. К какому электронному семейству относятся элементы?
66 Напишите электронные формулы атомов элементов с порядковыми номерами 48 и 56. Определите период и группу Периодической системы Д.И.Менделеева, в которых находятся элементы.
67 Напишите электронные формулы ионов элементов Al3+ и Те2-. К какому электронному семейству относятся элементы?
68 Сколько неспаренных электронов содержится в электронной оболочке атомов элементов цинка и кремния?
69 Напишите электронные формулы атомов элементов кальция и бария. Какой элемент проявляет более металлические свойства? Ответ обосновать?
70 Напишите электронные формулы атомов элементов с порядковыми номерами 23 и 32. Распределите электроны по квантовым ячейкам. Определите период и группу Периодической системы Д.И. Менделеева, в которых находятся элементы.
71 Напишите электронные формулы атомов элементов с порядковыми номерами 39 и 51. Определите период и группу Периодической системы Д.И.Менделеева, в которых находятся элементы.
72 Напишите электронные формулы атомов элементов с порядковыми номерами 39 и 50. Какой элемент проявляет более металлические свойства? Ответ обосновать.
Молекула – наименьшая частица вещества, обладающая его химическими свойствами.
Согласно теории химической связи, устойчивому состоянию элемента соответствует структура с электронной формулой внешнего уровня s2p6 (аргон, криптон, радон, и другие).
При образовании химической связи атомы стремятся приобрести такую устойчивую структуру. При этом возможны три типа химической связи.
Ионная связь – осуществляется в результате электростатического взаимодействия противоположно заряженных ионов. При взаимодействии атомов металлических и неметаллических элементов (разность электроотрицательности больше 1,9) атомы металлических элементов отдают лишние электроны внешнего уровня, переходя в положительно заряженные ионы, а атомы неметаллических элементов принимают электроны, достраивая внешний уровень до восьми электронов, переходя в отрицательно заряженные ионы.
Например, 12Mg 1s22s22p63s2 -2e = 1s22s22p6
Mg -2e = Mg2+
8F 1s22s22p5 +e = 1s22s22p6
F +e = F-
Так как электрическое поле иона имеет сферическую симметрию, то при образовании связи между двумя противоположно заряженными ионами возможно электростатическое взаимодействие и с другими ионами. У ионных соединений определяющее значение имеют ненасыщенность и ненаправленность связи. Ионные соединения при обычных условиях являются кристаллическими веществами.
Металлическая связь. Осуществляется за счёт делокализованных электронов. При взаимодействии атомов только металлических элементов (в веществах называемых металлами) «лишние» электроны внешнего уровня способны перемещаться по металлу, но находятся в поле действия положительных ионов. Это взаимодействие подвижных ионов определяет, что соединения с металлической связью при обычных условиях являются кристаллами, которые имеют специфические свойства.
Ковалентная связь осуществляется за счёт электронной пары одновременно принадлежащей двум атомам.
Например: На внешнем уровне атома хлора 7 электронов
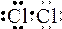
При взаимодействии с другим атомом хлора образуется устойчивая структура молекула Cl2, где у каждого атома на внешнем уровне 8 электронов.
Рассмотрим свойства ковалентной связи с точки зрения метода валентных связей (МВС). Основные положения МВС.
1. В образовании ковалентной связи принимают участие два электрона с противоположными спинами.
2. Образование ковалентной связи происходит за счёт перекрывания атомных орбиталей валентных электронов.
3. Связь образуется по линии максимального перекрывания атомных орбиталей.
Ковалентная связь характеризуется свойствами: насыщаемость, направленность и полярность.
Способность атома к образованию химических связей называют валентностью элемента. Количественной мерой валентности принято считать число электронов способных образовывать химические связи – число валентных электронов.
Для s – элементов валентными электронами является s – электроны внешнего уровня;
Для р – элементов s- и р – электроны внешнего уровня;
Для d – элементов s – электроны внешнего уровня и d – электроны предвнешнего уровня.
Например, 11Na – валентный электрон 3s1
56Ba - 6s2 13Al – 3s23p1 53J – 5s25p5 22Ti – 4s23d2
Большинство соединений с ковалентной связью образовано по обменному механизму, при котором каждый атом поставляет по одному (неспаренному) электрону для образования общей пары.
Насыщаемость – это свойство, которое определяет стехиометрический (определённый) состав устойчивого соединения с ковалентной связью – молекулы. Для соединений образованных по обменному механизму валентность элемента определяется числом неспаренных валентных электронов.
Например, элементы кислород и водород образуют молекулу состава Н2О.
|
|
|
|
s p
У атома элемента кислорода имеется два неспаренных валентных электрона, т.е. валентность равна 2.
Для 1Н валентный электрон 1s1, т.е. валентность равна 1.
Однако большинство элементов могут иметь переменную валентность. Это возможно в том случае, если в пределах одного энергетического уровня имеются свободные орбитали.
Например, элемент углерод и кислород образуют СО и СО2
|
|
|
|
s p
|
|
|
|
s p
Исходя из свойств соединений СО и СО2 можно сделать вывод о том, что элемент в возбуждённом состоянии образует более устойчивое соединение.
 Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы:
Направленность – это свойство определяющее геометрическую форму молекулы с ковалентной связью. При образовании связи принимают участие атомные орбитали различной формы:
 s – электроны имеют форму орбитали
s – электроны имеют форму орбитали
 |
 р – электроны имеют форму орбитали
р – электроны имеют форму орбитали
Однако, когда атом находится в возбуждённом состоянии в образовании равноценных связей участвуют s- и р– гибридные орбитали.
Различают три типа гибридизации:
1. Один s – электрон и один р – электрон: s р – гибридизация
|
|
|
|
2. Один s – электрон и два р – электрона: s р2 – гибридизация
|
|
|
|
3. Один s – электрон и три р – электрона: s р3 – гибридизация
|
|
|
|
В зависимости от направления перекрывания атомных орбиталей различают: s - и π – связи.
s -связь возникает при перекрывании орбиталей вдоль оси, соединяющей ядра взаимодействующих атомов. s - связь наблюдается при перекрывании s – s –, р – р – s - р – орбиталей и т.д.
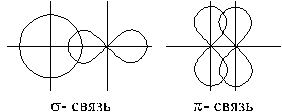
Рис. 3. Перекрывание электронных облаков
при образовании s - и p - связей
π – связь возникает при перекрывании орбиталей по обе стороны от оси соединяющей ядра атомов. Наблюдается при перекрывании р – р орбиталей расположенных перпендикулярно оси, соединяющей ядра атомов.
|
|
|
|
|
Дата добавления: 2015-03-29; Просмотров: 1244; Нарушение авторских прав?; Мы поможем в написании вашей работы!