
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сольволиз и гидролиз. Гидролиз солей. Степень и константа гидролиза
Изолированные неизолированные сис-мы. Функции состояния, уравнения состояния. Работа, теплота, энергия. Температура. Внутренняя энергия.
Соединения, молекулы которых способны при одних и тех же условиях отщеплять и ион Н и ион гидроксила ОН, наз. амфотерными. К ним относятся переходные Ме, а также Be,Al,Pb,Sn и др.
Zn(OH)2+ HCl=ZnCl2+2H2O
Zn(OH)2+2NaOH=Na2ZnO2+2H2O
Водородный показатель (рН ) – это десятичный логарифм концентрации водородный ионов, взятый с обратным знаком.
Индикаторы – специальный реактив, окраска которых меняется в зависимости от концентрации ионов водорода.
Буферные растворы – те рас-ры, рН к-ых остается постоянным при разбавлении р-ра или при добавлении сильной к-ты или щёлочи небольшое кол-во. Кислотные буферы – р-р слабой к-ты и соли этой к-ты. [Н+] (кислотный буфер) = Кдисс [конц. кислоты]/ [конц. соли]
Основные буферы – р-ры слабого основания и соли этого основания.
Буферное действие – сво-во р-ов сохранять неизменным [Н+] при добавлении небольшого кол-ва кис-т или щелочей
Буферная емкость – предельное кол-во сильной к-ты или щелочи, к-ые нужно добавить в 1 л р-ра, стоюы изменить величину рН на 1 единицу.
Гидролиз солей - это обменное взаимодействие ионов соли с молекулами воды, в результате которого смещается равновесие электролитической диссоциации воды и меняется реакция среды. Это обратимая реакция нейтрилизации.
- Если соли образованы катионом сильного основания и анионом сильной кислотой

- Если соли образованы катионом сильного основания и анионом слабой кислотой
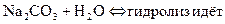
 гидролиз идёт по слабому аниону, который забирает себе ион водорода. Среда щелочная, так как концентрация ионов гидроксила превышена. Теперь дополняем уравнение гидролиза теми ионами, которые в нём не участвовали:
гидролиз идёт по слабому аниону, который забирает себе ион водорода. Среда щелочная, так как концентрация ионов гидроксила превышена. Теперь дополняем уравнение гидролиза теми ионами, которые в нём не участвовали:
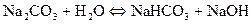
- Если соли образованы катионом слабого основания и анионом сильной кислотой
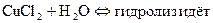
 гидролиз идёт по слабому катиону, который забирает себе ион гидроксила. Среда кислая, так как концентрация ионов водорода превышена. Теперь дополняем уравнение гидролиза теми ионами, которые в нём не участвовали:
гидролиз идёт по слабому катиону, который забирает себе ион гидроксила. Среда кислая, так как концентрация ионов водорода превышена. Теперь дополняем уравнение гидролиза теми ионами, которые в нём не участвовали:

- Если соли образованы катионами слабого основания и анионами слабой кислоты 
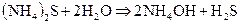 гидролиз идёт ДО КОНЦА, реакция НЕОБРАТИМА
гидролиз идёт ДО КОНЦА, реакция НЕОБРАТИМА
Степень гидролиза - это отношение числа молекул, подвергшихся гидролизу 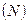 к общему числу молекул в растворе
к общему числу молекул в растворе 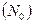 :
:

Другой количественной характеристикой процесса гидролиза является константа гидролиза, характеризующая собой равновесие процесса гидролиза.
- Если соль образована кислотой то 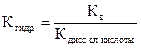
- Если соль образована слабым основанием то 
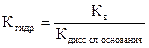
- Если соль образована слабой кислотой и слабым основанием то
|
|
Дата добавления: 2015-04-24; Просмотров: 843; Нарушение авторских прав?; Мы поможем в написании вашей работы!