
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характеристики гидролиза
|
|
|
|
Вопрос 75. Различные случи солей гидролиза..
гидролиз по катиону (в реакцию с водой вступает только катион); гидролиз по аниону (в реакцию с водой вступает только анион); совместный гидролиз (в реакцию с водой вступает и катион, и анион);
Вопрос 76.
Вопрос 77. Степень гидролиза[править | править исходный текст]
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр);
α = (c гидр/ c общ)·100 %
где c гидр — число молей гидролизованной соли, c общ — общее число молей растворённой соли.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Является количественной характеристикой гидролиза.
 Рассмотрим гидролиз соли, образованной одноосновной кислотой и одновалентным металлом. Запишем уравнение гидролиза в общем виде. Пусть НА - кислота, МОН - основание, МА - образования или соль. Тогда уравнение гидролиза будет иметь вид: МА + Н2О НА + МОН.
Рассмотрим гидролиз соли, образованной одноосновной кислотой и одновалентным металлом. Запишем уравнение гидролиза в общем виде. Пусть НА - кислота, МОН - основание, МА - образования или соль. Тогда уравнение гидролиза будет иметь вид: МА + Н2О НА + МОН.
Будем рассматривать достаточно разбавленные растворы. Тогда равновесию реакции (1) при заданной температуре отвечает постоянная величина - константа равновесия
| К = | СНА. СМОН |
| СМА. СН2О |
Где Сi - молярные концентрации веществ. Концентрация воды в разбавленных растворах представляет собой практически постоянную величину. Обозначая К. Сн2о = Кг, получим
| Кг = | СНА. СМОН | (2) |
| СМА |
Величина Кг называется константой гидролиза соли. Ее значение характеризует способность данной соли подвергаться гидролизу; чем больше Кг, тем в большей степени (при одинаковых температуре и концентрации соли) протекает гидролиз.
Отношение числа молей соли, подвергшихся гидролизу (Сг), к общему числу молей соли в растворе (СМА), называется степенью гидролиза.
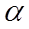 = =
| Сг | (3) |
| СМА |
Для вещества типа МА величина Сг равна концентрации любого из продуктов гидролиза - реакции (1). Поэтому степень гидролиза может быть определена из соотношений вида:
| = | Сг | = | Смон | . |
| СМА | Сма |
Используя такие соотношения и выражение (2) для константы гидролиза, можно легко получить уравнение, связывающее степень и константу гидролиза.
Вопрос 78. Буферные растворы (англ. buffer, от buff — смягчать удар) — растворы с определённой устойчивой концентрацией водородных ионов; смесь слабой кислоты с сопряженным основанием (напр., СН3СООН и CH3COONa — ацетатный буфер) или слабого основания и сопряженной кислоты (напр., NH3 и NH4CI — аммиачный буфер).[1] Величина рН буферного раствора мало изменяется при добавлении небольших количеств свободной сильной кислоты или щёлочи, при разбавлении или концентрировании. Буферные растворы широко используют в различных химических и биохимических процессах.
Принцип действия химических буферных систем заключается в трансформации сильных кислот и сильных оснований в слабые.
Вопрос 79. Буферные растворы играют важную роль во многих технологических процессах. Они используются, например, при электрохимическом нанесении защитных покрытий, в производстве красителей, фотоматериалов и кожи. Кроме того, буферные растворы широко используются в химическом анализе и для калибровки рН-метров (см. гл. 10).
Многие биологические и другие системы зависят от содержащихся в них буферных растворов, которые поддерживают постоянство рН. Нормальные значения рН для некоторых из таких систем указаны в табл. 8.6. Например, рН крови в организме человека поддерживается в пределах от 7,35 до 7,45, несмотря на то, что содержание диоксида углерода и, следовательно, угольной кислоты в крови может варьировать в широких пределах. Содержащийся в крови буфер представляет собой смесь фосфата, гидрокарбоната и белков. Буферы, состоящие из белков, поддерживают рН слез равным 7,4. В бактериологических исследованиях для поддержания постоянства рН культурных сред, используемых с целью выращивания бактерий, тоже приходится использовать буферные растворы.
Разбавление буферного раствора водой или концентрирование его путем выпаривания также почти не изменит рН, так как не изменится соотношение концентраций компонентов, от которого зависит концентрация Н - и ОН - - ионов. Если, например, при разбавлении того же ацетатного буферного раствора водой концентрация Н - ионов уменьшается, то это уменьшение компенсируется увеличением степени диссоциации уксусной кислоты.
Вопрос 80. Разбавление буферного раствора водой или концентрирование его путем выпаривания также почти не изменит рН, так как не изменится соотношение концентраций компонентов, от которого зависит концентрация Н - и ОН - - ионов. Если, например, при разбавлении того же ацетатного буферного раствора водой концентрация Н - ионов уменьшается, то это уменьшение компенсируется увеличением степени диссоциации уксусной кислоты.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 904; Нарушение авторских прав?; Мы поможем в написании вашей работы!