
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Физические свойства. HC≡CNa + CH3-Cl → HC≡C-CH3 + NaCl
|
|
|
|
Применение
Из ацетиленидов
| HC≡CMe + R-Г → HC≡C-R + MeГ |
HC≡CNa + CH3-Cl → HC≡C-CH3 + NaCl
моно
ацетиленид хлорпропан пропин
натрия
| MeC≡CMe + 2R-Г → R-C≡C-R + 2MeГ |
AgC≡CAg + 2CH3-I → CH3-C≡C-CH3 + 2AgI↓
ацетиленид серебра йодметан бутин-2
Ацетилен широко применяют в органическом синтезе. Он является одним из исходных веществ при производстве синтетических каучуков, поливинилхлорида и других полимеров. Из ацетилена получают уксусную кислоту, растворители (1,1,2,2-тетрахлорэтан и 1,1,2-трихлорэтен). При сжигании ацетилена в кислороде температура пламени достигает 3150 °С, поэтому его используют при сварке и резке металлов.
Примеры промышленного использования ацетилена:
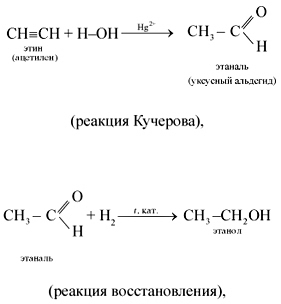
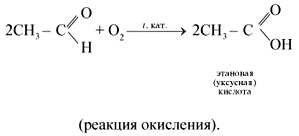
С2Н2 – Ацетилен – бесцветный газ, легче воздуха, мало растворим в воде, в чистом виде почти без запаха.
Свойства гомологов изменяются аналогично алкенам. По физическим свойствам алкины напоминают алкены и алканы. Температуры их плавления и кипения увеличиваются с ростом молекулярной массы. В обычных условиях алкины С2–С3 – газы, С4–С16 – жидкости, высшие алкины – твердые вещества. Наличие тройной связи в цепи приводит к повышению температуры кипения, плотности и растворимости их в воде по сравнению с олефинами и парафинами.
Физические свойства некоторых алкинов сведены в таблице.
Таблица. Физические свойства некоторых алкинов
| Название (Суффикс –ин) | Формула | t°пл., °C | t°кип., °C |
| Этин (Ацетилен) | HC≡CH | -80,8 | -83,6 |
| Пропин (Метилацетилен) | CH3–C≡CH | -102,7 | -23,3 |
| Бутин-1 | C2H5–C≡CH | -122,5 | 8,5 |
| Бутин-2 | CH3–C≡C–CH3 | -32,3 | 27,0 |
| Пентин-1 | CH3–CH2–CH2–C≡CH | -98,0 | 39,7 |
| Пентин-2 | CH3–CH2–C≡C–CH3 | -101,0 | 56,1 |
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 3303; Нарушение авторских прав?; Мы поможем в написании вашей работы!