
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ход работы
|
|
|
|
Билет № 31
ЭТАЛОН ОТВЕТА К БИЛЕТУ №31
Билет № 30
ЭТАЛОН ОТВЕТА К БИЛЕТУ №30
ЗАДАНИЕ №1
Текст задания:
1.
2.
ЗАДАНИЕ №2
Текст задания:
1.Задача
Вычислите, какая масса гидроксида натрия образуется при взаимодействии 2,3 г натрия с водой.
| Дано: | Решение: |
| m(NaOH) = 2.3 г | 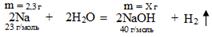
|
| Найти: | 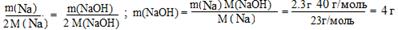
|
| m(NaOH) | Ответ: m(NaOH) = 4 г |
ЗАДАНИЕ №1
Текст задания:
1.
2.
ЗАДАНИЕ №2
Текст задания:
1.Опыт:
Получите углекислый газ и проведите реакции, характеризующие его химические свойства.
Реактивы:
· СаСО3 (мрамор)
· раствор ласмуса
· раствор соляной кислоты
· раствор Са(ОН)2 (известковая вода)
Оборудование:
штатив с пробирками
В лаборатории углекислый газ получают действием соляной кислоты на мрамор (СаСО3).
1. Получение углекислого газа:
СаСО3 + 2НCl = CaCl2 + H2O + CO2↑
2. Углекислый газ СО2 – кислотный оксид и может реагировать с водой, щелочами и основными оксидами.
2.1.Получающийся углекислый газ пропустим в пробирку с раствором лакмуса
 СО2 + Н2О ↔ Н2СО3
СО2 + Н2О ↔ Н2СО3
Цвет раствора становится красным. Окраска неяркая, так как угольная кислота слабая, т.к. неполностью диссоциирует на ионы.
2.2.Заменим пробирку-приемник на новую, содержащую
известковую воду (раствор Са(ОН)2). Наблюдается помутнение известковой воды от образования осадка карбоната СаСО3.
Наблюдаем, что полученный осадок быстро растворяется в избытке СО2, так как образуется растворимый гидрокарбонат кальция:
СаСО3 + Н2О + СО2 = Са(НСО3)2
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 655; Нарушение авторских прав?; Мы поможем в написании вашей работы!