
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Особенности гетерогенных химических реакций. Стадии процесса и области его протекания. Стадии гетерогенных процессов. Первый закон Фика
|
|
|
|
Гетрогенные Р – ХР, протекающие на границе раздела фаз.
Реакции на гр. раздела ТВ. тело – газ и ТВ. тело-жидкость. ГР этого типа широко используются в химической технологии. К ним отн. реакции горения ТВ. и жид. топлива, окисления мет., восстановления мет. из оксидов и сульфидов, р-ции, идущие на пов-ти ТВ. катализаторов. Примеры ГР: окисление мет., разложение карбоната кальция, р-ции обжига и восстановления, р-ции с участием 3-х ТВ. фаз, р-ции 2-го обмена в тв. фазе. В ГР, как правило, можно выделить по кр. мере 3 стадии: 1 – перенос реаг-х в-в к пов-ти раздела фаз, т.е. в реакционную зону. 2 –собственно хим. взаимодействие. 3-перенос продуктов реакции из реакционной зоны. М.б. и др. стадии – напр. адсорбция и десорбция, доп-е хим. превращения…комплексообр-ие. Скорость всего процесса опред-ся лимитирующей стадией. Диффузионный режим р-ции – если скорость собств. хим. взаим. значит. больше скорости подвода реагентов и отвода прод. от реакц. зоны (общ. скор. проц. будет соотв. скорости переноса реагентов и прод.). Перенос в-ва к границе может осуществляться за счет конвекции и диффузии. Конвекция – перемещение всей среды в целом.
Диффузия – направленное перемещение в-ва из области с большей концентрацией в область с меньшей концентрацией. Подвод в-ва диффузией определяется 1-м
законом Фика: кол-во dn в-ва, продиффундировавшего через площадку S, перпендикулярную потоку в направлении от большей концентрации к меньшей, пропорционально времени dt и градиенту концентрации (dC/dx): 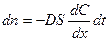 , D – коэф. диффузии.
, D – коэф. диффузии.
В том случае, когда собственно хим. взаим. является наиб. медленной стадией, т.е. диф. протек. сравнительно быстро, говорят, что р-ция протекает в кинетич. режиме или находится в кин. области. В том случае, когда скорости р-ции и диф. приблиз. равны, говорят о переходном режиме или перех. области ГР. При повышении Т лимит. стадия и, соотв. мех-м ГР могут изменяться. Это связано с разным хар-ром зависимости константы скорости ХР и коэф. диффузии от Т. Зависимость D от Т опред-ся аналогично k: 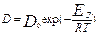 . По величине Еа можно судить о мех-ме процесса: для диф. проц. Еа=5…20 кДж/моль, кин.: Еа=50…200 кДж/моль. В пром. обл. ГР контр-ся как диф-ей, так и ХР на границе раздела фаз.
. По величине Еа можно судить о мех-ме процесса: для диф. проц. Еа=5…20 кДж/моль, кин.: Еа=50…200 кДж/моль. В пром. обл. ГР контр-ся как диф-ей, так и ХР на границе раздела фаз.
Скорость ГХР измеряется изменением поверхностной конц-ии одного из в-в.(газа или жид.), учавствующих в реакции, за ед. времени: 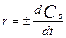 , моль/м*2с.
, моль/м*2с.
Конц-ции в-в в твердом состоянии постоянны, поэтому в кин. Ур-ие они не входят. Т.к. на определить пов. конц. дов. трудно, на практ. исп-ют объемную конц-ю. (r в моль/л*с). При пост. Т число столкн. на пов. разд фаз постоянно.
Скорость ГР с уч. ТВ. в-ва опр. через степень превращения в-ва. 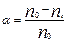 , nt – оставшееся кол-во в-ва к t. Твердофазные реакции: реакции между в-вами в ТВ. фазе и р-ции полиморфных превращений. Взаим-е, из-за малой подв-ти ат. и ионов, возможно лишь в зоне контакта. Образуется слой продукта, а дальнейшее прот. р-ции зависит от скор. диффузии взаим-х в-в через слой продукта. (и продукт тоже учавствует в диффузии). Топохимический хар-р ТВ-фазн. р. – локализация реакционной зоны на пов-ти раздела фаз реаг. и прод-ов.
, nt – оставшееся кол-во в-ва к t. Твердофазные реакции: реакции между в-вами в ТВ. фазе и р-ции полиморфных превращений. Взаим-е, из-за малой подв-ти ат. и ионов, возможно лишь в зоне контакта. Образуется слой продукта, а дальнейшее прот. р-ции зависит от скор. диффузии взаим-х в-в через слой продукта. (и продукт тоже учавствует в диффузии). Топохимический хар-р ТВ-фазн. р. – локализация реакционной зоны на пов-ти раздела фаз реаг. и прод-ов.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 677; Нарушение авторских прав?; Мы поможем в написании вашей работы!