
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Универсальная газовая постоянная численно равна работе, которую совершает один моль идеального газа при изобарическом расширении и изменении температуры на 1 К. 2 страница
| |
|
| |
|
15) .Уравнение Ван-Дер-Ваальса. Изотермы Ван-Дер-Ваальса и их анализ. Внутренняя энергия реального газа.
Ван-дер-Ваальсом в уравнение Клапейрона — Менделеева введены две поправки.
1. Учет собственного объема молекул. Наличие сил отталкивания, которые противодействуют проникновению в занятый молекулой объем других молекул, сводится к тому, что фактический свободный объем, в котором могут двигаться молекулы реального газа, будет не V m, а V m — b, где b — объем,занимаемый самими молекулами.
Объем b равен учетверенному собственному объему молекул. Если, например, в сосуде находятся две молекулы, то центр любой из них не может приблизиться к центру другой молекулы на расстояние, меньшее диаметра d молекулы. Это означает, что для центров обеих молекул оказывается недоступным сферический объем радиуса d, т. е. объем, равный восьми объемам молекулы или учетверенному объему молекулы в расчете на одну молекулу.
2. Учет притяжения молекул. Действие сил притяжения газа приводит к появлению дополнительного давления на газ, называемого внутренним давлением. По вычислениям Ван-дер-Ваальса, внутреннее давление обратно пропорционально квадрату молярного объема, т. е. 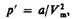 где а — постоянная Ван-дер-Ваальса, характеризующая силы межмолекулярного притяжения, V m — молярный объем.
где а — постоянная Ван-дер-Ваальса, характеризующая силы межмолекулярного притяжения, V m — молярный объем.
Вводя эти поправки, получим уравнение Ван-дер-Ваальса для моля газа (уравнение состояния реальных газов): 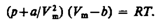
Для произвольного количества вещества v газа (v=m/M) с учетом того, что V=vV m, уравнение Ван-дер-Ваальса примет вид
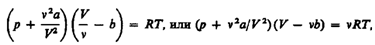
где поправки а и b — постоянные для каждого газа величины, определяемые опытным путем (записываются уравнения Ван-дер-Ваальса для двух известных из опыта состояний газа и решаются относительно а и b).
Изотермы Ван-дер-Ваальса — кривые зависимости р от V m при заданных Т, определяемые уравнением Ван-дер-Ваальса для моля газа. Эти кривые имеют довольно своеобразный характер. При высоких температурах (T > T к) изотерма реального газа отличается от изотермы идеального газа только некоторым искажением ее формы, оставаясь монотонно спадающей кривой. При некоторой температуре T к на изотерме имеется лишь одна точка перегиба К.
Эта изотерма называется критической, соответствующая ей температура T к — критической температурой; точка перегиба К называется критической точкой; в этой точке касательная к ней параллельна оси абсцисс. Соответствующие этой точке объем V к, и давление р к называются также критическими. Состояние с критическими параметрами (p к, V к, T к) называется критическим состоянием. При низких температурах (Т < T к) изотермы имеют волнообразный участок, сначала монотонно опускаясь вниз, затем монотонно поднимаясь вверх и снова монотонно опускаясь.
Для пояснения характера изотерм преобразуем уравнение Ван-дер-Ваальса к виду 
Уравнение при заданных р и Т является уравнением третьей степени относительно V m; следовательно, оно может иметь либо три вещественных корня, либо один вещественный и два мнимых, причем физический смысл имеют лишь вещественные положительные корни. Поэтому первому случаю соответствуют изотермы при низких температурах (три значения объема газа V 1, V 2 и V 3 отвечают (символ «m» для простоты опускаем) одному значению давления р 1), второму случаю — изотермы при высоких температурах. 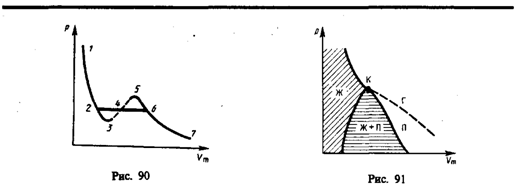
Рассматривая различные участки изотермы при T < Т к (рис. 90), видим, что на участках 1 — 3 и 5 — 7 при уменьшении объема V m давление р возрастает, что естественно. На участке 3—5 сжатие вещества приводит к уменьшению давления; практика же показывает, что такие состояния в природе не осуществляются. Наличие участка 3—5 означает, что при постепенном изменении объема вещество не может оставаться все время в виде однородной среды; в некоторый момент должно наступить скачкообразное изменение состояния и распад вещества на две фазы. Таким образом, истинная изотерма будет иметь вид ломаной линии 7 — 6—2—1. Часть 6–7 отвечает газообразному состоянию, а часть 2 – 1 — жидкому. В состояниях, соответствующих горизонтальному участку изотермы 6—2, наблюдается равновесие жидкой и газообразной фаз вещества. Вещество в газообразном состоянии при температуре ниже критической называется паром, а пар, находящийся в равновесии со своей жидкостью, называется насыщенным.
Для нахождения критических параметров подставим их значения в уравнение

(символ «m» для простоты опускаем). Поскольку в критической точке все три корня совпадают и равны V к уравнение приводится к виду
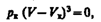 или
или 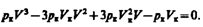
Tax как уравнения тождественны, то в них должны быть равны и коэффициенты при неизвестных соответствующих степеней. Поэтому можно записать 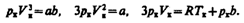
Решая полученные уравнения, найдем 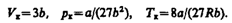
Если через крайние точки горизонтальных участков семейства изотерм провести линию, то получится колоколообразная кривая (рис. 91), ограничивающая область двухфазных состояний вещества. Эта кривая и критическая изотерма делят диаграмму р,V m под изотермой на три области: под колоколообразной кривой располагается область двухфазных состояний (жидкость и насыщенный пар), слева от нее находится область жидкого состояния, а справа — область пара. Пар отличается от остальных газообразных состояний тем, что при изотермическом сжатии претерпевает процесс сжижения. Газ же при температуре выше критической не может быть превращен в жидкость ни при каком давлении.
Сравнивая изотерму Ван-дер-Ваальса с изотермой Эндрюса (верхняя кривая на рис. 92), видим, что последняя имеет прямолинейный участок 2 — 6, соответствующий двухфазным состояниям вещества. Правда, при некоторых условиях могут быть реализованы состояния, изображаемые участками ван-дер-ваальсовой изотермы 5— 6 и 2 — 3. Эти неустойчивые состояния называются метастабильными. Участок 2—3 изображает перегретую жидкость, 5—6 — пересыщенный пар. Обе фазы ограниченно устойчивы.

При достаточно низких температурах изотерма пересекает ось V m, переходя в область отрицательных давлений (нижняя кривая на рис. 92). Вещество под отрицательным давлением находится в состоянии растяжения. При некоторых условиях такие состояния также реализуются. Участок 8—9 на нижней изотерме соответствует перегретой жидкости, участок 9—10 — растянутой жидкости.
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул (определяет внутреннюю энергию идеального газа, равную СVТ) и потенциальной энергии межмолекулярного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к возникновению внутреннего давления на газ (см. (61.1)):

Работа, которая затрачивается для преодоления сил притяжения, действующих между молекулами газа, как известно из механики, идет на увеличение потенциальной энергии системы, т. е. 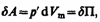 или
или  откуда
откуда
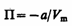
(постоянная интегрирования принята равной нулю). Знак минус означает, что молекулярные силы, создающие внутреннее давление р', являются силами притяжения. Учитывая оба слагаемых, получим, что внутренняя энергия моля реального газа
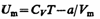 (63.1)
(63.1)
растет с повышением температуры и увеличением объема.

Если газ расширяется без теплообмена с окружающей средой (адиабатический процесс, т. е. dQ =0) и не совершает внешней работы (расширение газа в вакуум, т. е. dА= 0), то на основании первого начала термодинамики (dQ = (U 2 —U 1) + dA) Получим, что
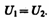 (63.2)
(63.2)
Следовательно, при адиабатическом расширении без совершения внешней работы внутренняя энергия газа не изменяется.
Равенство (63.2) формально справедливо как для идеального, так и для реального газов, но физический смысл его для обоих случаев совершенно различен. Для идеального газа равенство U 1 =U 2 означает равенство температур (T 1= T 2), т. е. при адиабатическом расширении идеального газа в вакуум его температура не изменяется. Для реального газа из равенства (63.2), учитывая, что для моля газа
 (63.3)
(63.3)
получаем
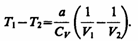
Так как V 2 > V 1, то Т 1 > Т 2, т. е. реальный газ при адиабатическом расширении в вакуум охлаждается. При адиабатическом сжатии в вакуум реальный газ нагревается.
|
|
Дата добавления: 2015-04-24; Просмотров: 626; Нарушение авторских прав?; Мы поможем в написании вашей работы!
 Так как энтропия задается с точностью до аддитивной постоянной, то эту постоянную для простоты возьмем равной нулю. При этом отметим, что это произвольное допущение, т.к. энтропия по своей сущности всегда задается с точностью до аддитивной постоянной. Из теоремы Нернста — Планка следует, что теплоемкости Ср и СV при 0 К равны нулю.
Так как энтропия задается с точностью до аддитивной постоянной, то эту постоянную для простоты возьмем равной нулю. При этом отметим, что это произвольное допущение, т.к. энтропия по своей сущности всегда задается с точностью до аддитивной постоянной. Из теоремы Нернста — Планка следует, что теплоемкости Ср и СV при 0 К равны нулю.
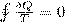 (1) Из равенства нулю интеграла (1), взятого по замкнутому контуру, следует, что подынтегральное выражение δQ/T есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, которым система пришла в это состояние. Таким образом,
(1) Из равенства нулю интеграла (1), взятого по замкнутому контуру, следует, что подынтегральное выражение δQ/T есть полный дифференциал некоторой функции, которая определяется только состоянием системы и не зависит от пути, которым система пришла в это состояние. Таким образом,  (2) Функция состояния, у которой дифференциал равен δQ/T, называется энтропией и обозначается S. Из формулы (1) следует, что для обратимых процессов изменение энтропии
(2) Функция состояния, у которой дифференциал равен δQ/T, называется энтропией и обозначается S. Из формулы (1) следует, что для обратимых процессов изменение энтропии 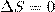 (3) В термодинамике доказывается, что энтропия системы, совершающей необратимый цикл, возрастает:
(3) В термодинамике доказывается, что энтропия системы, совершающей необратимый цикл, возрастает:  (4) Выражения (3) и (4) применяются только к замкнутым системам, если же система обменивается теплотой с внешней средой, то ее энтропия может вести себя произвольным образом. Соотношения (3) и (4) можно представить в виде неравенства Клаузиуса
(4) Выражения (3) и (4) применяются только к замкнутым системам, если же система обменивается теплотой с внешней средой, то ее энтропия может вести себя произвольным образом. Соотношения (3) и (4) можно представить в виде неравенства Клаузиуса 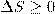 (5) т. е. энтропия замкнутой системы может либо возрастать (в случае необратимых процессов), либо оставаться постоянной (в случае обратимых процессов). Если система совершает равновесный переход из состояния 1 в состояние 2, то, согласно (2), изменение энтропии
(5) т. е. энтропия замкнутой системы может либо возрастать (в случае необратимых процессов), либо оставаться постоянной (в случае обратимых процессов). Если система совершает равновесный переход из состояния 1 в состояние 2, то, согласно (2), изменение энтропии  (6) где подынтегральное выражение и пределы интегрирования определяются через величины, которые характеризуют рассматриваемый процесс. Формула (6) определяет энтропию лишь с точностью до аддитивной постоянной (слагаемого). Физический смысл имеет не сама энтропия, а разность энтропий. Используя выражение (6), найдем изменение энтропии в процессах идеального газа. Taк как dU=(m/M)CVdT, δA=pdV=(m/M)RT(dV/V), то
(6) где подынтегральное выражение и пределы интегрирования определяются через величины, которые характеризуют рассматриваемый процесс. Формула (6) определяет энтропию лишь с точностью до аддитивной постоянной (слагаемого). Физический смысл имеет не сама энтропия, а разность энтропий. Используя выражение (6), найдем изменение энтропии в процессах идеального газа. Taк как dU=(m/M)CVdT, δA=pdV=(m/M)RT(dV/V), то  или
или  (7) т. е. изменение энтропии ΔS1→2 идеального газа при переходе его из cоcтояния 1 в cоcтояние 2 не завиcит от вида процеccа перехода 1→2. Так как для адиабатического процесса δQ = 0, то ΔS = 0 и, следовательно, S=const, т. е. адиабатический обратимый процесс протекает при постоянной энтропии. Поэтому его часто называют изоэнтропийным процессом. Из формулы (7) следует, что при изотермическом процессе (T1= T2)
(7) т. е. изменение энтропии ΔS1→2 идеального газа при переходе его из cоcтояния 1 в cоcтояние 2 не завиcит от вида процеccа перехода 1→2. Так как для адиабатического процесса δQ = 0, то ΔS = 0 и, следовательно, S=const, т. е. адиабатический обратимый процесс протекает при постоянной энтропии. Поэтому его часто называют изоэнтропийным процессом. Из формулы (7) следует, что при изотермическом процессе (T1= T2)  при изохорном процессе (V1 = V2)
при изохорном процессе (V1 = V2) 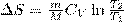 Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, которые входят в систему. Свойством аддитивности обладают также внутренняя энергия, масса, объем (но таким свойством не обладают температура и давление). Более глубокий смысл энтропии показывается в статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Термодинамическая вероятность W состояния системы — это число способов, с помощью которых может быть реализовано данное состояние макроскопической системы, или число микросостояний, которые осуществляют данное макросостояние (по определению, W≥1, т. е. термодинамическая вероятность не есть вероятность в математическом смысле (последняя ≥1!!!)). Cогласно Больцману, энтропия cиcтемы и термодинамическая вероятность связаны между собой следующим образом:
Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, которые входят в систему. Свойством аддитивности обладают также внутренняя энергия, масса, объем (но таким свойством не обладают температура и давление). Более глубокий смысл энтропии показывается в статистической физике: энтропия связывается с термодинамической вероятностью состояния системы. Термодинамическая вероятность W состояния системы — это число способов, с помощью которых может быть реализовано данное состояние макроскопической системы, или число микросостояний, которые осуществляют данное макросостояние (по определению, W≥1, т. е. термодинамическая вероятность не есть вероятность в математическом смысле (последняя ≥1!!!)). Cогласно Больцману, энтропия cиcтемы и термодинамическая вероятность связаны между собой следующим образом: 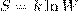 (8) где k — постоянная Больцмана. Таким образом, энтропия определяется логарифмом числа микросостояний, с помощью которых может быть осуществлено данное макросостояние. Значит, энтропия может рассматриваться как мера вероятности состояния термодинамической системы. Формула Больцмана (8) позволяет дать энтропии следующее статистическое толкование: энтропия является мерой неупорядоченности системы. Действительно, чем больше число микросостояний, которые реализуют данное макросостояние, тем больше энтропия. В состоянии равновесия — наиболее вероятного состояния системы — число микросостояний максимально, при этом также максимальна и энтропия. Так как реальные процессы необратимы, то можно говорить, что все процессы в замкнутой системе ведут к увеличению ее энтропии — принцип возрастания энтропии. При статистическом толковании энтропии это означает, что процессы в замкнутой системе идут в направлении увеличения числа микросостояний, другими словами, от менее вероятных состояний к более вероятным, до тех пор пока вероятность состояния не станет максимальной. Соотнося выражения (5) и (8), видим, что энтропия и термодинамическая вероятность состояний замкнутой системы могут либо увеличиваться (в случае необратимых процессов), либо оставаться неизменными (в случае обратимых процессов). Отметим, однако, что эти утверждения имеют место для систем, которые состоят из очень большого числа частиц, но могут нарушаться в системах с малым числом частиц. Для систем с малым числом частиц могут наблюдаться флуктуации, т. е. энтропия и термодинамическая вероятность состояний замкнутой системы на фиксированном отрезке времени могут уменьшаться, а не увеличиваться, или оставаться постоянными.
(8) где k — постоянная Больцмана. Таким образом, энтропия определяется логарифмом числа микросостояний, с помощью которых может быть осуществлено данное макросостояние. Значит, энтропия может рассматриваться как мера вероятности состояния термодинамической системы. Формула Больцмана (8) позволяет дать энтропии следующее статистическое толкование: энтропия является мерой неупорядоченности системы. Действительно, чем больше число микросостояний, которые реализуют данное макросостояние, тем больше энтропия. В состоянии равновесия — наиболее вероятного состояния системы — число микросостояний максимально, при этом также максимальна и энтропия. Так как реальные процессы необратимы, то можно говорить, что все процессы в замкнутой системе ведут к увеличению ее энтропии — принцип возрастания энтропии. При статистическом толковании энтропии это означает, что процессы в замкнутой системе идут в направлении увеличения числа микросостояний, другими словами, от менее вероятных состояний к более вероятным, до тех пор пока вероятность состояния не станет максимальной. Соотнося выражения (5) и (8), видим, что энтропия и термодинамическая вероятность состояний замкнутой системы могут либо увеличиваться (в случае необратимых процессов), либо оставаться неизменными (в случае обратимых процессов). Отметим, однако, что эти утверждения имеют место для систем, которые состоят из очень большого числа частиц, но могут нарушаться в системах с малым числом частиц. Для систем с малым числом частиц могут наблюдаться флуктуации, т. е. энтропия и термодинамическая вероятность состояний замкнутой системы на фиксированном отрезке времени могут уменьшаться, а не увеличиваться, или оставаться постоянными.