
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Зв'язок між положенням хімічного елемента у періодичній системі та електронною будовою його атомів
|
|
|
|
Період об'єднує елементи з однаковим числом електронних шарів в атомах цих елементів. Електронний шар складається з електронів, що знаходяться на одному і тому ж енергетичному рівні. Номер періоду, в якому розміщений елемент, дорівнює числу електронних шарів в атомах елемента. Початок нового періоду збігається з початком формування нового електронного шару в атомах елементів, які знаходяться в цьому періоді.
Підгрупа визначається електронною родиною елемента: головні підгрупи складають елементи s- та р-електронних родин (s- та р-елементи), побічні підгрупи – елементи d-електронної родини (d-елементи). В атомах s-елементів в останню чергу заповнюється електронами s-підрівень, в атомах p-елементів - p-підрівень, в атомах d-елементів – d-підрівень. f-Елементи розміщені в Періодичній системі окремо.
Група об'єднує елементи з однаковим числом валентних електронів в атомах цих елементів. Номер групи, в якій розміщений елемент, дорівнює числу валентних електронів.
В атомах елементів головних підгруп (в атомах s- та р-елементів) валентними є s- та р-електрони зовнішнього електронного шару.
В атомах елементів побічних підгруп (в атомах d-елементів):
– якщо d-підрівень заселений електронами повністю, то номер групи дорівнює числу електронів тільки зовнішнього електронного шару,.
– якщо d-підрівень містить менше, ніж 10 електронів, то валентними є s-електрони зовнішнього та d-електрони передзовнішнього електронних шарів. Винятком є у періоді 4 кобальт та нікол. Хоча в їх атомах містяться відповідно дев`ять та десять валентних електронів, ці елементи, як і ферум, завдяки схожості їх хімічних властивостей, розташували в одній групі, а саме в групі VIII. Те ж саме стосується елементів Rh, Pd, Ir, Pt, які знаходяться відповідно у періодах 5 та 6.
Підрівні, на яких знаходяться валентні електрони, називаються валентними.
Валентність елемента у нормальному стані дорівнює числу неспарених електронів у зовнішньому електронному шарі його атомів. У збудженому стані відбувається роз`єднання спарених електронів, що містяться у зовнішньому електронному шарі, та перехід одного електрона з кожної електронної пари на вільні АО того ж самого енергетичного рівня. Число неспарених електронів в атомах, отже, і валентність елемента збільшується.
При визначенні валентності d-елементів у збудженому стані враховують неспарені електрони зовнішнього і неспарені d-електрони передзовнішнього електрнних шарів.
Вищу валентність, яка збігається з номером групи, більшість елементів виявляють у збудженому стані. Якщо збуджений стан неможливий, то вища валентність деяких елементів менша за номер групи (оксиген, флуор) або збігається з номером групи (лужні метали).
Хімічні властивості елемента визначаються числом електронів, що містять атоми у зовнішньому електронному шарі. Атоми металів містять у зовнішньому електронному шарі 1 або 2, рідше 3, 4 електрони (якщо ці електрони знаходяться на більшій відстані від ядра і зв'язок між цими електронами та ядром слабший). Атоми неметалів містять у зовнішньому електронному шарі 4 або більше (5, 6,7) електронів.
Негативний ступінь окиснення, який чисельно дорівнює числу приєднаних електронів, виявляють лише атоми неметалів: у сполуках з металами та гідрогеном. Найнижчий ступінь окиснення атомів неметалів є негативним і дорівнює «8 – номер групи». Атоми металів у вільному стані приєднувати електрони не здатні, тому їх атоми не набувають негативного ступеня окиснення. Отже, найнижчий ступінь окиснення атомів металів дорівнює “0”.
Позитивний ступінь окиснення, який чисельно дорівнює числу відданих валентних електронів, виявляють і атоми металів, і атоми неметалів: в оксидах, гідроксидах, солях. Найвищий ступінь окиснення атомів і металів, і неметалів є позитивним, чисельно збігається з вищою валентністю елемента і у більшості дорівнює номеру групи в якій знаходиться елемент.
Формулювання періодичного закону Д.І Меделєєва: ”Властивості елементів а також властивості утворених ними простих речовин та хімічних сполук перебувають в періодичній залежності від величини заряду ядер атомів елементів”.
Періодична зміна властивостей елементів та їх сполук обумовлена тим, що через певні періоди відбувається повторення подібної електронної будови атомів цих елементів.
Характерною хімічною властивістю металів є здатність їх атомів віддавати зовнішні електрони і перетворюватись на позитивно заряджені йони, тобто катіони.
Енергія йонізації І – це енергія, яка необхідна для відриву електрона від атома.
Енергія йонізації є мірою металічних властивостей елементів: чим менша величина енергії йонізації, тим легше відірвати електрон від атома, тим активнішим є метал.
Неметали характеризуються здатністю їх атомів до приєднання електронів з утворенням негативно заряджених йонів, тобто аніонів.
Енергія спорідненості до електрона Е – це енергія, яка у більшості виділяється під час приєднання електрона до атома. Спорідненість до електрона у більшості металів є близькою до нуля, що свідчить про те, що приєднання електронів для атомів металів енергетичного невигідно.
Отже, спорідненість до електрона є мірою неметалічних властивостей елементів: чим більша спорідненість до електрона, тим активнішим є неметал.
У межах періоду зі збільшенням порядкового номера елементів, тобто по мірі зростання заряду ядер, збільшуються сили притягання зовнішніх електронів до ядра і зменшується радіус атомів. Тому енергія йонізації поступово теж збільшується і металічні властивості елементів послаблюються. За таких причин збільшується спорідненість елементів до електрона, тобто їх неметалічні властивості посилюються.
У межах головних підгруп по мірі зростання порядкового номера елементів, збільшується число електронних шарів в атомах, отже, збільшуються і розміри атомів. Крім того, збільшення числа проміжних електронних шарів між зовнішніми електронами та ядром атома сприяє більш сильному екрануванню ядра, тобто послабленню сил притягання зовнішніх електронів до ядра.
Збільшення заряду ядер в головних підгрупах менше впливає на зв'язок зовнішніх електронів з ядром, ніж збільшення розмірів атомів і числа екрануючих електронних шарів. Тому в межах головних підгруп зв'язок зовнішніх електронів з ядром зменшується, що призводить до зменшення енергії йонізації і до посилення металічних властивостей елементів. Зменшується також і спорідненість елементів до електрона, тобто їх неметалічні властивості послаблюються.
Побічні підгрупи складають метали, які належать до d-електронної родини елементів. В атомах цих елементів останніми заповнюються електронами внутрішні енергетичні оболонки, які утримуються ядром сильніше, ніж зовнішні. Тому розміри атомів металів побічних підгруп менші, ніж розміри атомів металів головних підгруп. Внаслідок цього значення енергії йонізації металів побічних підгруп більш високі і їх металічні властивості зі збільшенням порядкового номера послаблюються.
Приклад 1. Вкажіть період, групу та підгрупу у періодичній системі для елемента, атоми якого мають наведену конфігурацію двох останніх електронних шарів:... 4s24p64d105s25p4.
Назвіть цей елемент. Які властивості: металічні чи неметалічні – він виявляє? Чому дорівнює валентність елемента у нормальному та збудженому стані? Вкажіть найнижчий та найвищий ступені окиснення елемента у сполуках. Запишіть формулу вищого оксиду та відповідного гідроксиду елемента. За якою ознакою об`єднано елементи в одній підгрупі?
Розв'язання. Елемент розташований:
– В періоді 5: електронна оболонка атомів елемента складається з п`яти електронних шарів (в умові наведена конфігурація четвертого та п`ятого електронних шарів).
– В головній підгрупі: елемент належить до р-електронної родини (в останню чергу заповнюється електронами р-підрівень).
– В групі VI: в атомах елемента містяться шість валентних електронів (...5s25p4).
Цей елемент – телур. Він виявляє неметалічні властивості, бо у зовнішньому електронному шарі його атомів знаходяться шість електронів. Тому атоми телуру здатні приєднувати два електрони з утворенням стійкої восьмиелектронної оболонки зовнішнього шару (...5s25p6), набуваючи найнижчого ступеня окиснення який дорівнює “–2” у сполуках з атомами гідрогену (H2Te) та з атомами металів, наприклад, Na2Te.
Валентість елемента у нормальному стані становить II, тому що зовнішній електронний шар містить два неспарені електрони:...5s25px2py1pz1.
У збудженому стані відбувається роз`єднання спарених електронів на 5s- та 5p-підрівнях та перехід одного електрона з кожної електронної пари на вільні АО того ж самого енергетичного рівня, тобто на АО 5d-підрівня:
Te* … 5s25px1py1pz15d11d2d3d4d5 ,
Te** … 5s15px1py1pz15d11d21d3d4d5.
Число неспарених електронів в атомах збільшується. Отже, і валентність елемента у збудженому стані збільшується і становить IV (Te*) та VI (Te**).
Атоми телуру здатні віддавати електрони, набуваючи позитивного ступеня окиснення. Найвиший ступінь окиснення телуру дорівнює максимальному числу відданих електронів зовнішнього електронного шару (...5s05p0), чисельно збігається з вищою валентністю елемента та з номером групи, в якій розташований телур, і дорівнює “+6”.
Вищий оксид телуру ТеО3 (оксид неметалу) виявляє кислотний характер. Відповідним гідроксидом є кислота: TeO3·H2O=H2TeO4.
| В одній підгрупі періодичної системи об`єднано елементи-аналоги, тобто елементи з подібною електронною будовою їх атомів. Отже, атоми елементів, що складають головну підгрупу групи VI, мають наведену електронну конфігурацію валентних підрівнів: | O...2s22p4 S...3s23p4 Se...4s24p4 Te...5s25p4 Po...6s26p4. |
Приклад 2. Складіть електронну конфігурацію атомів скандію. Дайте обгрунтування розташування елемента у періодичній системі. Які властивості: металічні чи неметалічні – виявляє цей елемент? Запишіть формулу вищого оксиду скандію та рівняння реакцій, що доводять його хімічний характер. За якою ознакою об`єднано елементи головної та побічної підгруп в одну групу?
Розв'язання. Протонне число скандію становить 21, отже в його атомах міститься 21 електрон. Електронна конфігурація атомів скандію:
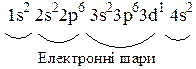
Елемент розташований:
– В періоді 4: електронна оболонка атомів елемента складається з чотирьох електронних шарів.
– В побічній підгрупі: елемент належить до d-електронної родини (згідно з правилом Клечковського в останню чергу електронами заповнюється 3d-підрівень, тобто після заповнення 4s-підрівня).
– В групі III: в атомах скандію знаходяться три валентних електрони (…3d14s2).
Скандій виявляє металічні властивості, тому що його атоми містять у зовнішньому шарі два лектрони (...4s2).
Валентність скандію у нормальному стані становить 0, оскільки у зовнішньому електронному шарі його атомів відсутні неспарені електрони. У збудженому стані відбувається роз`єднання спарених електронів на 4s-підрівні та перехід одного з них на вільну АО того ж самого четвертого енергетичного рівня, а саме, на АО 4p-підрівня:
Sc* …3d14s14p1.
Число неспарених електронів в атомах елемента у збудженому стані дорівнює трьом, що відповідає вищій валентності скандію і збігається з номером групи.
Атоми скандію здатні віддавати три валентних електрони (…3d04s0) і набувати найвищоого ступеня окиснення, що дорівнює “+3” в оксиді, відповідному гідроксиді та в солях скандію.
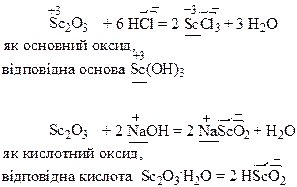
Вищий оксид елемента Sc2O3 (оксид металу з валентністю III) виявляє амфотерний характер, отже вза`ємодіє як з кислотами, так і з основами.
Атоми металів, отже, і атоми Sc не приєднують електрони, тому не набувають у сполуках негативного ступеня окиснення.
Нижче наведена електронна конфігурація валентних підрівнів атомів елементів головної та побічної підгруп групи III:
Головна підгрупа Побічна підгрупа
B … 2s22p1
Al … 3s23p1 Sc … 3d14s2
Ga … 4s24p1 Y … 4d15s2
In … 5s25p1 La … 5d16s2
Tl … 6s26p1 Ac … 6d17s2
Елементи обох підгруп, хоча належать до різних електронних родин, об`єднано в одну групу, тому що їх атоми містять однакове число валентних електронів:
– в атомах елементів головної підгрупи групи III, які є р-елементами, валентними є електрони зовнішнього електронного шару (... ns2np1).
– в атомах елементів побічної підгрупи групи III, які є d-елементами, валентними є не тільки s-електрони зовнішнього, а і d-електрони передзовнішнього електронних шарів (... (n-1)d1ns2).
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 2371; Нарушение авторских прав?; Мы поможем в написании вашей работы!