
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Виконання роботи. Завдання 2. Визначити вміст натрій гідрогенкабонату в технічному динатрій карбонаті
|
|
|
|
Завдання 2. Визначити вміст натрій гідрогенкабонату в технічному динатрій карбонаті.
Обладнання та реактиви
1. Iономiр типу рН-340, ЛПУ-001 або iнший з скляним Н+ -селективним iндикаторним електродом та аргентум хлоридним електродом порiвняння;
2. Терези аналітичні;
3. Магнiтна мiшалка;
4. Бюретка для титрування місткістю 25 см3;
5. Титрований розчин HCl - 0,1 моль/дм3;
6. Зразки технічного динатрiй карбонату Na2CO3 для аналізу.
1. На аналiтичних терезах взяти наважку (близько 0,1 г) Na2CO3.
2. Кількісно перенести наважку Na2CO3 з бюкса в стакан для титрування.
3. Поставити стакан на столик магнiтної мiшалки i додати такий об’єм дистильованої води, щоб електроди були зануренi в розчин. Увiмкнути мішалку.
4. Заповнити бюретку титрованим розчином HCl.
5. Титрування проводити додаванням невеликих порцiй по 0,5-1 см3 титрованого
розчину та вимiрюючи значення рН пiсля додавання кожної порції.
6. Отриманi данi i результати обчислень занести до таблицi за формою:
| V,см3 | pH | 
| 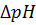
| 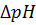 / / 
| V* |
7. Побудувати графiчні залежності в координатах: V –  (pH) та V*–
(pH) та V*–  (
( pH/
pH/  V),
V),
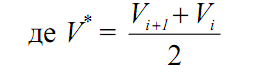
8. За побудованими графіками визначити точки еквівалентності, що відповідають титруванню Na2CO3 до NaHCO3 i далi NaHCO3 до H2CO3.
9. Обчислити вміст NaHCO3 в Na2CO3 за формулою:
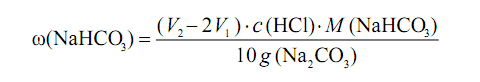
де V1 – об’єм розчину HCl, витраченого до першої точки еквiвалентностi, cм3; V2 –
об’єм розчину HCl, витраченого до другої точки еквiвалентностi, cм3; М(NaHCO3) –
молярна маса NaHCO3, г/моль; g(Na2CO3) – наважка (Na2CO3), г; c(HCl) – молярна
концентрація робочого розчину HCl, моль/дм3.
Na2CO3 + HCl=NaHCO3 + NaCl
NaHCO3 + HCl=H2CO3 + NaCl
Висновок:
.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 272; Нарушение авторских прав?; Мы поможем в написании вашей работы!