
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фізичні і хімічні властивості
|
|
|
|
Чиста сірка — крихка кристалічна речовина жовтого кольору, добре розчинна в бензолі та сірковуглеці, погано розчинна у воді. Сірка утворює кілька алотропних модифікацій: ромбічна моноклінна та пластична. На рисунку 55 показана геометрична форма кристалів ромбічної та моноклінної сірки.
За нормальних умов сірка утворює восьмиатомну молекулу, атоми зв’язані між собою зигзагоподібно ковалентними зв’язками:

При кімнатній температурі стійка ромбічна сірка. Поступове нагрівання до 94,5 °С перетворює її на моноклінну. Кристали ромбічної та моноклінної сірки відрізняються взаємною орієнтацією ц просторі кільцевих молекул S8. Отже у випадку з сіркою було б вірніше говорити не про алотропію, а про поліморфізм. В інтервалі температур від +94,5 °С до плавлення +119,3 оС стійка моноклінна сірка. Подальше нагрівання перетворює сірку на жовту легкорухливу рідину. При t> 160 °С кільцеві молекули S8 починають розмикатись і виникають відкриті ланцюги з вільними зв'язками на кінцях — так звані довголанцюгові радикали. При подальшому нагріванні ці радикали взаємодіють між собою, утворюючи подовжені ланцюги. При цьому рідина стає більш темнішою та більш в'язкою. При нагріванні до +250 оС в'язкість знову зменшується, оскільки гомогенна структура молекул руйнується. Нагріту до +250 °С можна повільно охолодити, при цьому знову утворюється моноклінна модифікація, яка повільно перетворюється на ромбічну. Якщо розплавлену сірку вилити в холодну воду, утворюється чорна липка та тягуча маса — пластична сірка. Приблизно за годину шматки гомоланцюгів знову перетворюються на восьмиатомні молекули. Пластична сірка світлішає і перетворюється на ромбічну.
При нагріванні пара сірки набуває змін, які можна описати рівновагою:
S8 «S6 «S4 «S2 «S
Близько +900 °С молекули S2 мають хімічні будову, аналогічну будові О2 і характеризуються парамагнітними властивостями на відміну від усіх інших станів сірки, які є діамагнітними. Вживаються різні торгові назви сірки. Так, черешкова сірка — це ромбічна сірка, відлита у вигляді паличок — черешків. Для очищення від домішок технічну сірку переганяють у спеціальних печах. При цьому сірка осідає на стінках у вигляді дрібних пилинок — «сірчаного квіту». Це порошок все тієї ж ромбічної сірки.
Конфігурація зовнішнього електронного рівня атома сірки в незбудженому стані 3s23р4, що відповідає електронно-графічній формулі:
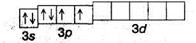
Приєднуючи два електрони, сірка утворює сполуки зі ступенем окиснення -2 (H2S, Na2S, CS2). Завдяки наявності d-орбіталей, електрони в атомі сірки можуть переходити у збуджений стан. При цьому утворюються сполуки з позитивними ступенями окиснення: +4 (SO2, H2SO3, NaHSO3, SF4, SOC12); +6 (SO3, H2SO4, HSO3C1, SF6, SO2CI2).
Знаходячись у проміжному ступені окиснення, сірка виявляє окиснювально-відновну двоїстість. Вона інтенсивно окиснює метали та водень, утворюючи сульфіди:
2Na + S* = Na2S.
З сильними окисниками сірка виступає відновником, наприклад:
S + O2 = SO2,
S + 2F2 = SF4.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 533; Нарушение авторских прав?; Мы поможем в написании вашей работы!