
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Нахождение истинных и средних теплоемкостей
|
|
|
|
Теплоемкость
Задачи
23.Горючая смесь газового двигателя состоит по объему из 8 частей воздуха и 1 части светильного газа. Найти удельную газовую постоянную и плотность смеси при давлении 0,1 МПа и температуре 15°С, если светильный газ состоит из следующих объемных частей: 48,5% водорода; 39,5% метана; 7% угарного газа и 5% азота. Ответ: R0 = 308,2 Дж/(кг×К); r = 1,126 кг/м3.
24.Объемные доли сухих продуктов сгорания (т.е. не содержащих водяного пара) следующие: хCO2 =0,123; хO2 = 0,072;хN2 =0,805. Найти удельную газовую постоянную, плотность и удельный объем продуктов сгорания, если их давление 0,1 МПа, а температура 800°С. Ответ: R0 = 274,7 Дж/(кг× К); v =2,947 м3/кг; r =0,339 кг/м3.
25.Газовая смесь задана следующими молярными долями: хCO2 =0,04; хСО = 0,1;хN2 =0,03; хН2 = 0,45; хСН4 = 0,35; хС2Н4 = 0,03. Давление смеси 90 кПа. Найти удельную газовую постоянную смеси и парциальное давление метана, а также плотность смеси при нормальных условиях. Ответ: R0 = 652,3 Дж/(кг×К); рСН4 = 31,5 кПа; r =0,569 кг/м3.
26.Найти массу продуктов сгорания топлива состава: nCO2 = 789 моль; nН2О = 67,4 моль; nО2 = 96,2 моль; nN2 = 787,3 моль. Ответ: 61,052 кг.
27.Продукты сгорания нефти имеют следующий состав в молях: nН2О = 66; nО2 = 70; nN2 = 660; nCO2 = 70. Найти удельную газовую постоянную и удельный объем смеси при нормальных условиях. Ответ: R0 = 288 Дж/(кг× К); v = 0,776 м3/кг.
Пример 12. Найти среднюю удельную теплоемкость кислорода при постоянном давлении при повышении его температуры от 600 до 2000°С.
Решение. Искомую теплоемкость принимаем равной истинной удельной изобарной теплоемкости при средней температуре
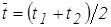 ;
;  = (600+2000)/2=1300°С.
= (600+2000)/2=1300°С.
Находим в приложении 4 истинную удельную изобарную теплоемкость кислорода при температуре 1300°С: ср=1,1476 кДж/(кг×К). Это значение теплоемкости равно средней удельной изобарной теплоемкости кислорода в интервале температур 600-2000°С.
Пример 13. Найти среднюю молярную изобарную теплоемкость углекислого газа при повышении его температуры от 200 до 1000°С.
Решение. Найти эту теплоемкость можно по уравнению
 .
.
Молярная масса углекислого газа равна 0,044 кг/моль. Среднюю удельную изобарную теплоемкость находим в табл. 2 прил. как истинную удельную изобарную теплоемкость при средней температуре 600°С. ср = 1,1962 кДж/(кг×К).
Следовательно, срm = 11962×0,044 = 526,33 кДж/(кг×К).
Пример 14. Воздух, содержащийся в баллоне вместимостью 12,5 м3 при температуре 20°С и давлении 1 МПа, подогревается до температуры 180°С. Найти подведенную теплоту Q12.
Решение. Воспользуемся уравнением:
Q12 = 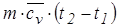 .
.
Массу воздуха найдем из уравнения состояния, среднюю изохорную теплоемкость - по таблицам прил.4 для средней температуры, равной 100°С.
В результате получим уравнение:
Q12 = 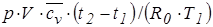 = 106×12,5×722,6×160/(287,1×(20+273)) = 17,18 МДж.
= 106×12,5×722,6×160/(287,1×(20+273)) = 17,18 МДж.
|
|
|
|
|
Дата добавления: 2015-05-08; Просмотров: 2575; Нарушение авторских прав?; Мы поможем в написании вашей работы!