
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Следствия второго начала термостатики
Следствия второго начала термостатики широко применяются в термодинамических расчетах и формулируются на основе анализа его математического выражения (162), (163).
Следствие I. Совместное выражение первого начала термодинамики и второго начала термостатики позволяет получить дифференциальное уравнение термодинамики, которое связывает между собой все термодинамические свойства веществ
T ds= cv dT + 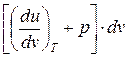 = cp dT +
= cp dT + 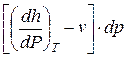 . (164)
. (164)
Следствие II. Координаты Т - S являются универсальными координатами термодинамического теплообмена.
Рассмотрим процесс 1-2 в координатах Т-S и выделим на нем элементарный участок с температурой Т и изменением энтропии dS (рис. 14).
|
 |
Исходя из математического выражения второго начала термостатики площадь под кривой элементарного участка процесса равна подводимому (отводимому) количеству теплоты
d Q = T×dS. (165)
При этом полное количество теплоты, подведенной или отведенной от системы в процессе 1-2, определяется следующим образом:
Q1,2 = 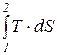 . (166)
. (166)
Если из-под знака интеграла в соотношении (166) вынести среднюю температуру конечного процесса Tm, то количество теплоты в процессе может быть определено по соотношению
Q1,2 = Tm × (S2 - S1). (167)
Как видно из выражения (166) и рис. 15, знак теплообмена определяется знаком изменения энтропии. Процессы, протекающие с увеличением энтропии, сопровождаются подводом теплоты. Процессы, протекающие с уменьшением энтропии - отводом теплоты. Независимо от природы рабочего тела площадь под кривой процесса в координатах Т-S равна количеству подведенной или отведенной теплоты.
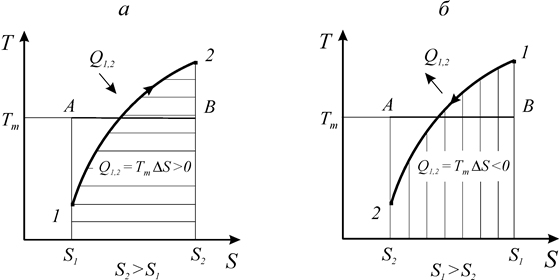
Рис. 15. Теплообмен в термодинамических процессах
Следствие III. Адиабатный процесс является процессом изоэнтропийным.
Так как в адиабатном процессе теплообмен отсутствует (d Q = 0), то, согласно второму началу термостатики (162), в таком процессе изменение энтропии dS = 0 (S = idem). Согласно этому следствию, показатель адиабатного процесса (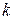 ) равен показателю изоэнтропийного процесса (
) равен показателю изоэнтропийного процесса (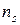 )
)
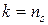 . (168)
. (168)
Следствие IV. Коэффициент полезного действия и холодильный коэффициент термодинамических циклов тепловых машин не зависят от вида цикла и природы рабочего тела, а определяются лишь средними абсолютными температурами рабочего тела в процессах подвода и отвода теплоты.
Рассмотрим термодинамические циклы в координатах Т-S: прямой цикл (цикл теплового двигателя) 1-А-2-В-1 (а) и обратный цикл (цикл холодильной машины) 1-А-2-B-1 (б) (рис. 16).
В процессе 1-А- 2 теплота подводится к рабочему телу. Количество подводимой теплоты соответствует на диаграмме горизонтально заштрихованной площади. Вертикально заштрихованная площадь соответствует количеству отведенной теплоты от рабочего тела в процессе 2-В-1.
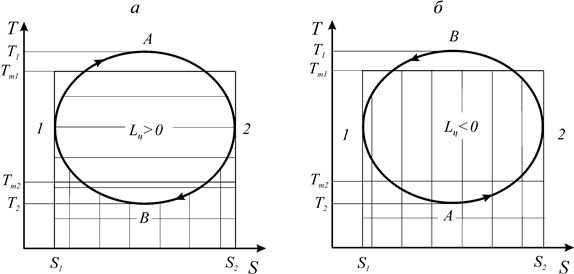
Рис. 16. Прямой и обратный циклы в координатах Т-S
Средние температуры рабочего тела в процессах подвода и отвода
теплоты в цикле теплового двигателя обозначим Тm1 и Тm2
соответственно (рис. 16а). Согласно выражения (167), количества подведенной и отведенной теплоты определяется по следующим соотношениям:
ú Q1 ç = 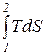 = Tm1 × (S2 - S1 ) = Tm1 ×úD S1,2 ç; (169)
= Tm1 × (S2 - S1 ) = Tm1 ×úD S1,2 ç; (169)
ú Q2 ç = 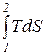 = Tm2 ×× (S2 - S1 ) = Tm2 ×úD S1,2 ç, (170)
= Tm2 ×× (S2 - S1 ) = Tm2 ×úD S1,2 ç, (170)
а коэффициент полезного действия любого термодинамического цикла теплового двигателя может быть найден из выражения
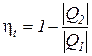 =
= 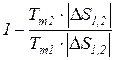 =1 -
=1 - 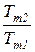 . (171)
. (171)
В результате аналогичных рассуждений получаем выражение для определения холодильного коэффициента термодинамического цикла холодильной машины (рис. 16б)
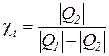 =
= 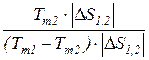 =
= 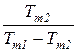 . (172)
. (172)
Полученные выражения (171), (172) свидетельствуют о том, что КПД и холодильный коэффициент термодинамических циклов тепловых машин определяются только средними абсолютными температурами рабочего тела в процессах подвода и отвода теплоты.
Из уравнений (171), (172) следует также, что для любого термо-динамического цикла тепловых машин выполняется следующее соотношение:
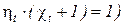 . (173)
. (173)
Следствие V. Коэффициент полезного действия и холодильный коэффициент цикла Карно всегда выше этих коэффициентов эффективности для любых других термодинамических циклов тепловых машин, осуществляемых в одинаковом диапазоне предельных температур рабочего тела (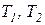 ).
).
Это следствие вытекает из анализа соотношений по определению КПД цикла Карно (153) и любого термодинамического цикла (171) теплового двигателя. Вследствие того, что Т1 >Тm1 и Т2 < Тm2 (рис. 16а),
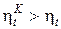 . (174)
. (174)
Аналогичный вывод можно сделать и при сравнении холодильных коэффициентов обратных циклов
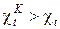 . (175)
. (175)
Рассматриваемое следствие утверждает, что цикл Карно является эталонным циклом, по сравнению с которым можно определить термодинамическое совершенство любого цикла, осуществляемого в заданном интервале предельных значений температур рабочего тела.
Следствие VI. Изменение энтропии системы равно сумме изменений энтропии всех тел, входящих в систему (теорема аддитивности энтропии).
Количество теплоты, полученное в элементарном процессе системой, состоящей из 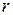 тел, можно определить из соотношения
тел, можно определить из соотношения
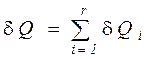 , (176)
, (176)
что и подтверждает справедливость сформулированного следствия
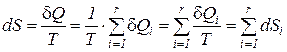 . (177)
. (177)
|
|
Дата добавления: 2015-05-09; Просмотров: 591; Нарушение авторских прав?; Мы поможем в написании вашей работы!