
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные теоретические положения. Цель проведения лабораторной работы
|
|
|
|
Цель проведения лабораторной работы
КОРРОЗИИ СТАЛИ ПО ЦВЕТАМ ПОБЕЖАЛОСТИ
ОПРЕДЕЛЕНИЕ СКОРОСТИ ВЫСОКОТЕМПЕРАТУРНОЙ
ЛАБОРАТОРНАЯ РАБОТА № 1
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к выполнению лабораторного практикума по дисциплине «Коррозия и защита металлов» для студентов всех специальностей
Днепропетровск НМетАУ 2005
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
НАЦИОНАЛЬНАЯ МЕТАЛЛУРГИЧЕСКАЯ АКАДЕМИЯ УКРАИНЫ
к выполнению лабораторного практикума по дисциплине «Коррозия и защита металлов» для студентов всех специальностей
УТВЕРЖДЕНО
на заседании кафедры ПМ и ЗМ,
протокол № от
Днепропетровск НМетАУ 2005
УДК
Методические указания к выполнению лабораторного практикума по дисциплине «Коррозия и защита металлов» для студентов всех специальностей. Сост.: C. И. Пинчук, А. П. Стовпченко, И. Г. Рослик, О. О. Внуков. - Днепропетровск: НМетАУ, 2006.- 33 с.
Приведены положения теории химической и электрохимической коррозии металлов и методические указания по определению скорости газовой коррозии и жаростойкости сталей, исследованию особенностей коррозии металлов в кислых и нейтральных средах, получению гальванических защитных покрытий.
Предназначены для студентов всех специальностей.
Разработали: С. И. Пинчук, д-р техн. наук, проф.
А. П. Стовпченко, д-р техн. наук, с.н.с..
И.Г. Рослик, канд. техн. наук. доц.
О.О. Внуков, ст. преп.
Ответственный за выпуск: С. И. Пинчук, д-р техн. наук, проф.
Рецензент
Редактор
Установить влияние температуры на скорость окисления углеродистой стали и рассчитать эффективную энергию активации процесса.
Задачи проведения лабораторной работы состоят в том, чтобы
знать: метод определения скорости коррозии металла по цветам побежалости;
уметь: самостоятельно проводить исследование влияния температуры на скорость окисления, рассчитывать энергию активации процесса.
Большинство металлов при высоких температурах в атмосфере термодинамически неустойчивы по отношению к кислороду. На их поверхности образуются оксидные пленки, защитные свойства которых в значительной мере определяют жаростойкость металлов и сплавов. Толщина оксидных пленок может изменяться в очень широких пределах.
Принято различать тонкие, средние и толстые пленки. Толщина тонких пленок - от мономолекулярной до 0,04 мкм. Такие пленки на металле невидимы и их наличие может быть установлено оптическими методами с применением поляризованного света или с помощью радиоактивных индикаторов. Толщина средних пленок (0,04 - 0,5 мкм) сопоставима с длиной волны видимых световых лучей (0,04 < l < 0,75 мкм). Эти пленки являются видимыми благодаря интерференционному окрашиванию, то есть возникновению так называемых цветов побежалости. Толстые пленки имеют толщину более 0,5 мкм и видны невооруженным глазом.
Интерференционные цвета побежалости позволяют определить толщину получаемых на металле пленок. Механизм появления цветов побежалости можно объяснить следующим образом. Погашение света вследствие интерференции двух лучей света, которые налагаются друг на друга, с длиной волны l происходит, если эти два луча смещены один относительно другого на половину фазы, то есть на непарное число полуволн: 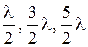 и т.д.
и т.д.
Пусть два луча проходят сквозь прозрачную пленку на поверхности металла, отражаясь один от внешней поверхности пленки (рисунок 1.1, линии 1, 2), другой - непосредственно от поверхности металла, пройдя через нее (рисунок 1.1, линии 3, 4).
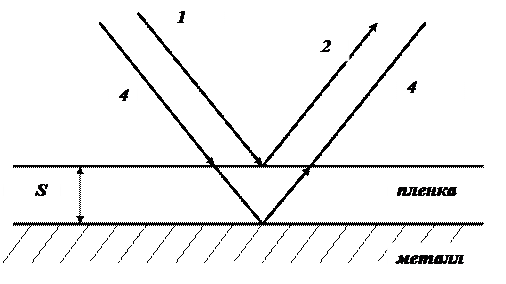
Рисунок 1.1 – Схема интерференции лучей света
Как это видно из рисунка, различие в ходе этих двух лучей определяется двойной толщиной пленки S (при падении луча под углом близким к прямому). Если учесть, что длина световой волны в прозрачной среде сокращается в обусловленное коэффициентом преломления число раз, то условия погашения данного луча с длиной волны l для пленки с показателем преломления n будут удовлетворяться, если толщина пленки S будет отвечать следующим значениям:
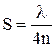 ;
; 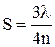 и т.д. (1.1)
и т.д. (1.1)
По этим формулам можно определить S, если установить интерференционное погашение луча при освещении образца монохроматическим светом. Такие измерения были проведены (таблица 1.1). Данные, приведенные в таблице 1.1, представляют собой толщины окисных пленок на железе, на котором получены цвета побежалости при нагревании образца на воздухе.
Таблица 1.1 - Толщина оксидных пленок на железе
| Цвет пленки | S, мкм |
| желтый | 0,046 |
| оранжевый | 0,052 |
| красный | 0,058 |
| фиолетовый | 0,068 |
| синий | 0,072 |
Зная толщину пленки и продолжительность процесса окисления, можно рассчитать скорость газовой коррозии.
В соответствии с уравнением Аррениуса скорость газовой коррозии V является функцией температуры:
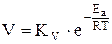 , (1.2)
, (1.2)
где - KV - константа скорости, Ea- эффективная энергия активации процесса.
Оксидные пленки могут быть сплошные или несплошные. Пиллинг и Бедвортс сформулировали условия, при которых образуются сплошные пленки, способные препятствовать дальнейшему окислению металла.
Если молекулярный объем оксида обозначить Vок, а объем металла Vме, то можно записать условие сплошности:

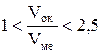 (1.3)
(1.3)
Соотношение 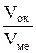 можно рассчитать по формуле:
можно рассчитать по формуле:
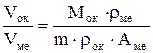 , (1.4)
, (1.4)
где Мок – молекулярная масса оксида, rме – плотность металла, rок – плотность оксида, Аме – атомная масса металла, m – количество атомов металла в оксиде.
Если 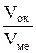 <1 - то пленка не может быть сплошной.
<1 - то пленка не может быть сплошной.
Рост пористой (незащитной) пленки (соотношение 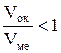 ) контролируется скоростью химической реакции окисления металла (кинетический контроль процесса) и протекает во времени по линейному закону:
) контролируется скоростью химической реакции окисления металла (кинетический контроль процесса) и протекает во времени по линейному закону:
h=k×t. (1.5)
Если пленка сплошная (соотношение 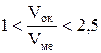 ) и оказывает сопротивление проникновению кислорода к металлу, то рост оксидной пленки описывается параболическим законом:
) и оказывает сопротивление проникновению кислорода к металлу, то рост оксидной пленки описывается параболическим законом:
h2 = k²×t. (1.6)
Часто рост тонких оксидных пленок (соотношение 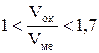 ) на металлах при низких температурах и на первых стадиях окисления металлов при высоких температурах сопровождается большим самоторможением во времени, тогда выполняется логарифмический закон:
) на металлах при низких температурах и на первых стадиях окисления металлов при высоких температурах сопровождается большим самоторможением во времени, тогда выполняется логарифмический закон:
h = k×ln t. (1.7)
Окисление металлов в различных температурных интервалах происходит по-разному. Линейный закон окисления характерен для натрия, кальция, магния; параболический – для меди, железа, никеля; логарифмический – для алюминия, цинка, хрома. Например, рост пленки на железе при температурах до 400°С происходит по логарифмическому закону, а в интервале 500-1100°С – по параболическому.
|
|
|
|
|
Дата добавления: 2015-05-07; Просмотров: 464; Нарушение авторских прав?; Мы поможем в написании вашей работы!