
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ізохорний
|
|
|
|
Рівняння стану ідеального газу
Об’єм даної маси газу є функцією від p і T:
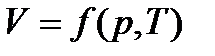 ,
,
тоді повний диференціал 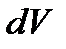 визначається як похідна:
визначається як похідна:
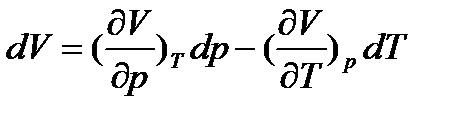 . (7)
. (7)
Рівняння (4) запишемо у вигляді:
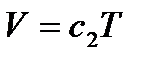 ,
,
тоді з рівнянь (1) і (.4):
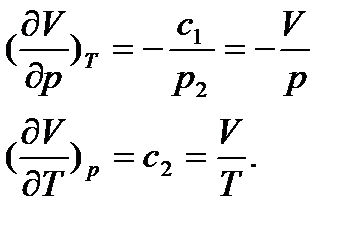 (8)
(8)
Якщо підставити рівняння (8) у рівняння (7), то отримаємо:
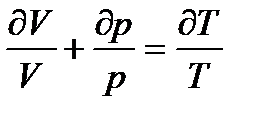 . (9)
. (9)
Якщо проінтегрувати, то:
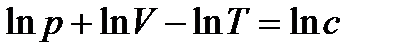 . (10)
. (10)
Потенціюючи дане рівняння, отримаємо:
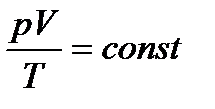 . (11)
. (11)
Дане рівняння було отримане французьким фізиком Клайпероном у1834році. У 1884 році Менделєєв придав рівнянню (11) універсального вигляду, записавши його для 1 моль газу з об’ємом V:
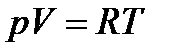 , (12)
, (12)
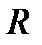 - постійна величина, універсальна газова стала:
- постійна величина, універсальна газова стала:
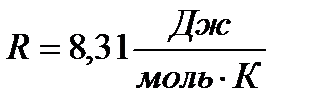 .
.
Якщо помножити (12) на кількість молів 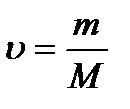 , отримаємо рівняння стану ідеального газу для довільної маси:
, отримаємо рівняння стану ідеального газу для довільної маси:
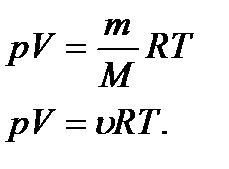 (13)
(13)
Останнє рівняння – рівняння Менделєєва-Клайперона
Ізохорний процес відбувається при сталому об’ємі газу (V=const):
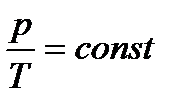 . (27)
. (27)
Це рівняння ізохорного процесу.
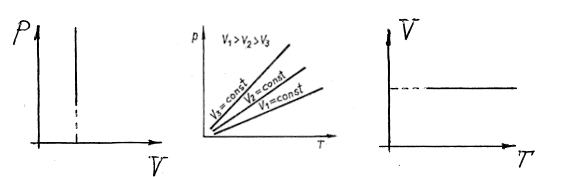
Рис. 5
За законом Шарля, рівняння ізохорного процесу також можна записувати у вигляді:
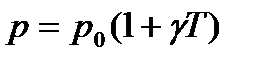 ,
,
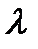 - термічний коефіцієнт тиску (
- термічний коефіцієнт тиску ( ).
).
Аналогічно до коефіцієнту 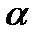 :
:
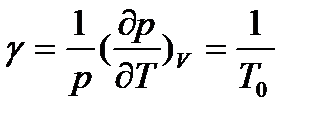 .
.
Зв’язок між коефіцієнтами 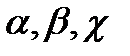 :
:
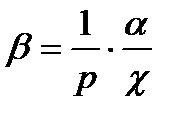 .
.
Робота в ізохорному процесі дорівнює нулю:
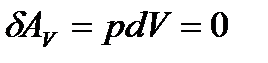 (28)
(28)
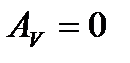 .
.
Тоді рівняння першого закону термодинаміки:
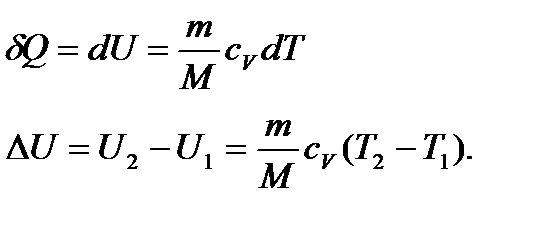 (29)
(29)
3.Обернений цикл Карно
Прямий обернений цикл Карно
Цикл Карно дозволяє підійти до поняття коефіцієнта дії теплової машини.
Схема роботи ідеальної теплової машини, що працює по циклу Карно:
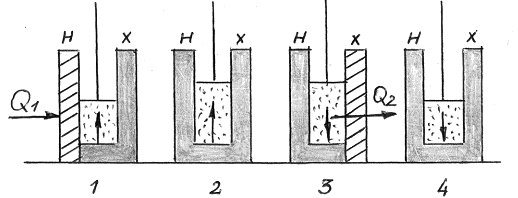
Рис. 2
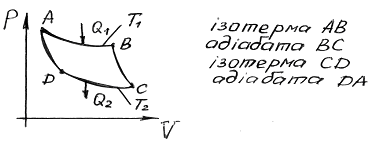
1. Нагрівач отримує теплоту  , і газ під поршнем починає розширюватися так як
, і газ під поршнем починає розширюватися так як 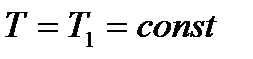 (ізотерма АВ). Так як процес рівновісний, то температура газу дорівнює температурі нагрівача.
(ізотерма АВ). Так як процес рівновісний, то температура газу дорівнює температурі нагрівача.
2. Газ теплоізольований і починає адіабатично розширюватись до 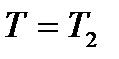 яка дорівнює температурі холодильника (адіабата ВС).
яка дорівнює температурі холодильника (адіабата ВС).
3. Газ ізотермічно 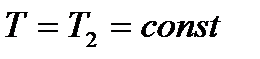 стискається, віддаючи холодильнику теплоту
стискається, віддаючи холодильнику теплоту 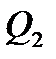 .
.
4. Газ адіабатно стискається, нагріваючись до температури нагрівача (адіабата DA).
Знайдемо роботу, яку здійснює ідеальний газ в даному циклі. Так як тепловий цикл – круговий, то повна зміна внутрішньої енергії газу дорівнює нулю (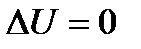 ). Тоді перший закон термодинаміки для робочого тіла (газу) в циклі Карно має вигляд:
). Тоді перший закон термодинаміки для робочого тіла (газу) в циклі Карно має вигляд:
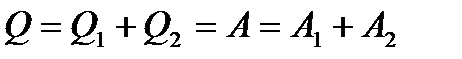 , (1)
, (1)
при цьому слід пам’ятати, що: 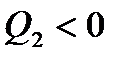
Роботу циклу можна виразити як суму робіт окремих процесів:
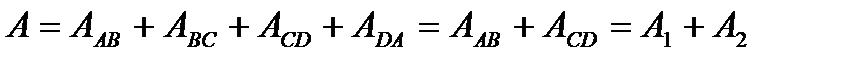 .
.
Так як сумарна робота адіабатичного розширення і стискання газу в даному циклі чисельно дорівнює нулю, тому:
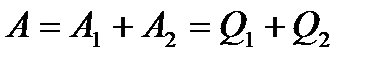 , (2)
, (2)
А – корисна робота циклу.
Так як 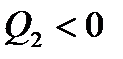 , то з рівняння (2) слідує, що ця робота
, то з рівняння (2) слідує, що ця робота 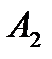 і менша від тієї кількості теплоти, що підводиться до нагрівача. Частина енергії віддається холодильнику у вигляді теплоти
і менша від тієї кількості теплоти, що підводиться до нагрівача. Частина енергії віддається холодильнику у вигляді теплоти 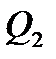 . Даний висновок справедливий для будь-якого кругового процесу. Величину відношення роботи до кількості теплоти позначають
. Даний висновок справедливий для будь-якого кругового процесу. Величину відношення роботи до кількості теплоти позначають 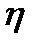 - термічний коефіцієнт теплового двигуна:
- термічний коефіцієнт теплового двигуна:
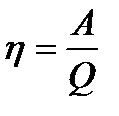 .
. 
Для нашого оберненого циклу Карно:
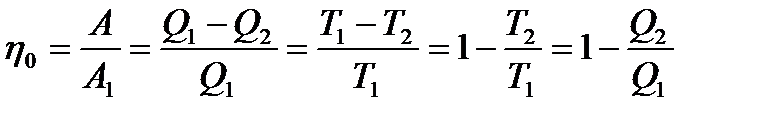 . (3)
. (3)
Формула (3) не має жодних даних про властивості робочого тіла і про будову теплової машини, тобто звідси випливає, що ККД усіх обернених машин, що працюють в ідеальних умовах, тобто при одній і тій самій температурі нагрівача 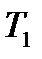 і температурі холодильника
і температурі холодильника 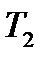 буде однаковим і визначатиметься тільки температурами нагрівача і холодильника. Дане твердження носить назву теореми Карно, яка є основою встановлення термодинамічної шкали температур.
буде однаковим і визначатиметься тільки температурами нагрівача і холодильника. Дане твердження носить назву теореми Карно, яка є основою встановлення термодинамічної шкали температур.
З рівняння (3) випливає:
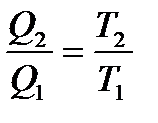 .
.
Таким чином, щоб порівняти температури двох тіл 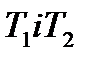 , потрібно здійснити обернений цикл Карно, в якому ці тіла використовуються у вигляді нагрівача і холодильника і порівняти теплоту
, потрібно здійснити обернений цикл Карно, в якому ці тіла використовуються у вигляді нагрівача і холодильника і порівняти теплоту 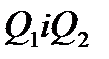 .
.
Термодинамічна шкала не зв’язана з властивостями термодинамічного тіла і в цьому є її досягнення. Але внаслідок необерненості реальних термодинамічних процесів, такий спосіб порівняння температур практично не виконується і має лише принципіальне значення.
1.3.2.б. Обернений рівновісний цикл Карно
В оберненому циклі Карно теплота  відводиться від газу в процесі ізотермічного стискання при температурі
відводиться від газу в процесі ізотермічного стискання при температурі  , а кількість теплоти
, а кількість теплоти 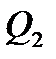 навпаки підводиться до газу в процесі ізотермічного розширення при
навпаки підводиться до газу в процесі ізотермічного розширення при 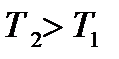 . Тоді результуюча робота
. Тоді результуюча робота 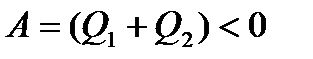 , тобто результуюча робота виконується зовнішнім середовищем над газом.
, тобто результуюча робота виконується зовнішнім середовищем над газом.
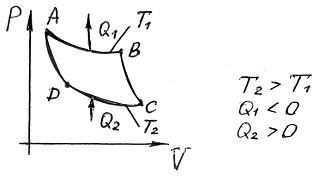
Даний результат справедливий для будь-якого оберненого циклу, таким чином за рахунок здійсненої роботи зовнішніми силами над робочим тілом, можна переносити енергію у вигляді теплоти від менш нагрітого тіла до більш нагрітого тіла. Даний метод використовується в холодильній техніці. Холодильна техніка буде тим більш економічною, чим менша буде робота 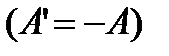 , яка витрачається зовні на відведення від холодильного тіла теплоти
, яка витрачається зовні на відведення від холодильного тіла теплоти  .
.
З рівняння, що  і з умови, що
і з умови, що 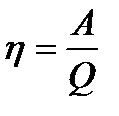 , знаходимо, що:
, знаходимо, що:
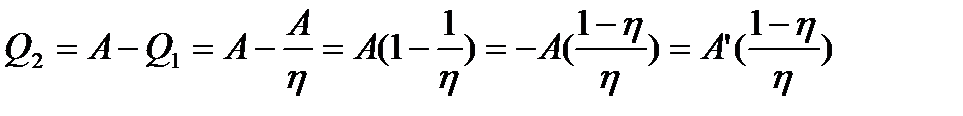 . (4)
. (4)
4.Потенціал Гіббса
Енергією Гіббса називається функція стану, що визначається рівнянням:
G=H-TS=U+pV-TS. (19)
Повний диференціал енергії Гіббса визначається як:
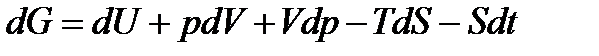 .
.
Така як dU=TdS-pdV, то потенціал енергії Гіббса:
dG=Vdp-SdT.
Тобто природними змінними для функції енергії Гіббса є тиск і температура (p i T), а частинні похідні цієї функції:
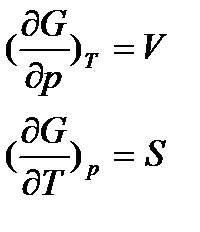 . (20)
. (20)
Якщо температура T і тиск p залишаються сталими, то відповідно до рівняння (13) можна записати:
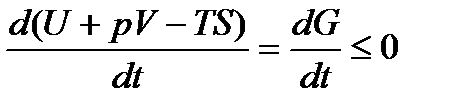 . (21)
. (21)
З рівняння слідує: якщо необхідний процес буде проходити при постійному тискові p=const і постійній температурі T=const, то це буде супроводжуватися зменшенням енергії Гіббса.
В стані рівноваги енергія Гіббса буде мінімальною.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 987; Нарушение авторских прав?; Мы поможем в написании вашей работы!