
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Решение. Бром Br является р-элементом VII группы 4-го периода, следовательно, конфигурация внешнего электронного уровня атома атома брома такова: 4s24p5
|
|
|
|
Решение.
Бром Br является р -элементом VII группы 4-го периода, следовательно, конфигурация внешнего электронного уровня атома атома брома такова: …4 s2 4 p5. Поскольку номер периода определяет значение главного квантового числа n, а для р -подуровня орбитальное орбитальное квантовое число l =1, то для последнего электрона внешнего уровня сумма n + l = 4 + 1 = 5.
Пример 5. Изотоп 101-го элемента – менделевия (256) был получен бомбардировкой α-частицами ядер атомов эйнштейния (253). Составьте уравнение этой ядерной реакции и напишите его в сокращенной форме.
Превращение атомных ядер обусловливается их взаимодействием с элементарными частицами или друг с другом. Ядерные реакции связаны с изменением состава ядер атомов химических элементов. С помощью ядерных реакций можно из атомов одних элементов получить атомы других.
Превращения атомных ядер как при естественной, так и при искусственной радиоактивности записывают в виде уравнений ядерных реакций. При этом следует помнить, что суммы массовых чисел (цифры, стоящие у символа элемента вверху слева) и алгебраические суммы зарядов (цифры, стоящие у символа элемента внизу слева) частиц в левой и правой частях равенства должны быть равны. Данную ядерную реакцию выражают уравнением
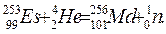
Часто применяют сокращенную форму записи. Для приведенной реакции она имеет вид:253Es(α, n)256Md. В скобках на первом месте пишут бомбардирующую частицу, а на втором, через запятую, - частицу, образующуюся при данном процессе. В сокращенных уравнениях частицы 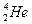 ,
,  ,
, 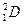 ,
, 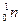 обозначают соответственно α, p, d, n.
обозначают соответственно α, p, d, n.
Контрольные задания
31. Определите, в каком периоде, группе, подгруппе находится элемент, электронная формула которого имеет следующее окончание: 1) …4 d 55 s 1; 2) …6 s 26 p 2; 3)…3 р 64 s 2. К какому семейству элементов он относится, какую максимальную степень окисления он может проявлять?
32. Напишите электронные формулы атомов элементов с порядковыми номерами 9 и 28. К какому электронному семейству относится каждый из этих элементов?
33. Напишите электронные формулы атомов фосфора и ванадия. К какому электронному семейству относится каждый из этих элементов?
34. Какое максимальное число электронов могут занимать s-, р-, d- и f- орбитали данного энергетического уровня? Почему?
35. Составьте электронные формулы атомов азота, имеющих степень окисления +5 и -3, и укажите число электронов на внешнем уровне.
36. Напишите электронные формулы атомов марганца и селена. К какому электронному семейству относится каждый из этих элементов?
37. Определите максимальное число неспаренных электронов, которые могут иметь атомы бериллия, кремния и серы при их переходе в возбужденное состояние.
38. Какие орбитали атома заполняются электронами раньше: 4 s или 3 d; 5 s или 4 p? Почему? Составьте электронную формулу атома элемента с порядковым номером 21.
39. Назовите элементы 1-, 2- и 3-го периодов, у атомов которых s -орбитали полностью заполнены электронами. Напишите электронные формулы атомов этих элементов и укажите, к какому периоду, группе и подгруппе периодической системы они относятся.
40. Определите, в каком периоде, группе, подгруппе находится элемент, электронная формула которого имеет следующее окончание: 1) …4 d 15 s 2; 2) …3 s 23 p 2; 3)…4 р 65 s 1. К какому семейству элементов он относится, какую максимальную степень окисления он может проявлять?
41. Составьте электронные формулы атомов элементов с порядковыми номерами 17 и 29. У последнего происходит провал одного 4 s -электрона на 3 d -подуровень. К какому электронному семейству относится каждый их этих элементов?
42. Какие орбитали атома заполняются раньше: 4 d или 5 s; 6 s или 5 p? Почему? Составьте электронную формулу атома элемента с порядковым номером 43.
43. Что такое изотопы? Чем можно объяснить дробность атомных масс большинства элементов периодической системы? Могут ли атомы разных элементов иметь одинаковую массу? Как называются подобные атомы?
44. Составьтеэлектронную формулу атома никеля и определите сумму значений главного и орбитального квантовых чисел последнего электрона предвнешнего уровня.
45. В чем сущность α-, β- - и β+ - радиоактивного распада? Изотоп какого элемента получается в результате последовательного излучения 4α- и 2 β- - частиц атомным ядром 238U?
46. Составьте электронные формулы атомов элементов с порядковыми номерами 14 и 40. Какие электроны этих атомов являются валентными?
47. Какую радиоактивность называют искусственной? Изотоп какого элемента образуется в результате ядерной реакции, происходящей при бомбардировке ядер атомов 27Al протонами, если при этом поглощается один протон и выделяется одна α-частица? Составьте уравнение этой ядерной реакции.
48. Составьте электронные формулы атомов элементов с порядковыми номерами 16, 43 и 54. К какому электронному семейству относится каждый из этих элементов?
49. Составьте электронные формулы атомов элементов с порядковыми номерами 28, 48 и 52. К какому электронному семейству относится каждый из этих элементов?
50. Назовите элементы 4, 5 и 6-го периодов, у которых заканчивается заполнение d -орбиталей (3 d 10, 4 d 10 и 5 d 10). Напишите электронные формулы атомов этих элементов и укажите, к какому периоду, группе и подгруппе они относятся.
51. Изотоп какого элемента образуется в результате ядерной реакции, происходящей при бомбардировке ядер атомов 54Fe α -части-цами, если при этом поглощается одна α -частица и выделяется один нейтрон. Составьте уравнение этой ядерной реакции.
52. Сколько и какие значения может принимать магнитное квантовое число при орбитальном квантовом числе l = 0; 1; 2 и 3? Какие элементы в периодической системе носят название s-, p-, d-, f- элементов? Приведите примеры.
53. Какие значения могут принимать квантовые числа n, l, ml и ms, характеризующие состояние электронов в атоме? Какие значения они принимают для внешних электронов атома магния?
54. Чем отличается последовательность в заполнении атомных орбиталей у атомов d -элементов от последовательности заполнения их у атомов s - и p -элементов? Составьте электронную формула атома элемента с порядковым номером 46, учитывая, что, находясь в пятом периоде, атомы этого элемента на пятом энергетическом уровне не содержат ни одного электрона.
55. Составьте электронные формулы атомов элементов с порядковыми номерами 24 и 33, учитывая, что у первого происходит провал одного 4 s - электрона на 3 d -подуровень. К какому электронному семейству относится каждый из этих элементов?
56. Значения какого квантового числа определяют число s-, p-, d-, f- орбиталей на энергетическом уровне? Сколько всего s-, p- и d -электронов в атоме кобальта?
57. В чем заключается принцип несовместимости Паули? Может ли быть на каком-нибудь подуровне атома p7- или d12- электронов? Почему? Составьте электронную формулу атома элемента с порядковым номером 22 и укажите его валентные электроны.
58. Составьте электронные формулы атомов элементов с порядковыми номерами 32 и 42, учитывая, что у последнего происходит провал одного 5 s -электрона на 4 d -подуровень. К какому электронному семейству относится каждый из этих элементов?
59. Составьте электронные формулы атома Ni0 и ионов Ni2+, Ni3+.
60. Какие из электронных формул, отражающих строение невозбужденного атома некоторого элемента неверны: а)1 s 22 s 22 p 53 s 1; б)1 s 22 s 22 p 6; в)1 s 22 s 22 p 63 s 23 p 63 d 4; г)1 s 22 s 22 p 63 s 23 p 64 s 2; д)1 s 22 s 22 p 63 s 23 d 2? Почему? Атомам каких элементов отвечают правильно составленные электронные формулы?
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 3204; Нарушение авторских прав?; Мы поможем в написании вашей работы!