
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Решение. Метод валентных связей (ВС) не может объяснить целый ряд свойств и строение некоторых молекул (парамагнетизм молекулы О2; большую прочность связей в
|
|
|
|
Метод валентных связей (ВС) не может объяснить целый ряд свойств и строение некоторых молекул (парамагнетизм молекулы О2; большую прочность связей в молекулярных ионах F 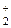 и O
и O 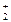 , чем соответственно в молекулах F2 и O2; наоборот, меньшую прочность связи в ионе N
, чем соответственно в молекулах F2 и O2; наоборот, меньшую прочность связи в ионе N 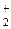 , чем в молекуле N2; существование молекулярного иона He
, чем в молекуле N2; существование молекулярного иона He 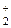 и неустойчивость молекулы He2 и т.п.). Более плодотворным оказался другой подход к объяснению ковалентной связи – метод молекулярных орбиталей (МО). В методе МО состояние молекулы описывается как совокупность электронных молекулярных орбиталей. При этом число молекулярных орбиталей равно сумме атомных орбиталей. Молекулярной орбитали, возникающей от сложения атомных орбиталей (АО), соответствует более низкая энергия, чем исходным орбиталям. Такая МО имеет повышенную электронную плотность в пространстве между ядрами, способствует образованию химической связи и называется связывающей. Молекулярной орбитали, образовавшейся от вычитания атомных, соответствует более высокая энергия, чем атомным орбиталям. Электронная плотность в этом случае сконцентрирована за ядрами атомов, а между ними равна нулю. Подобные МО энергетически менее выгодны, чем исходные АО, они приводят к ослаблению химической связи и называются разрыхляющими. Электроны, занимающие связывающие и разрыхляющие орбитали, называют соответственно связывающими (св) и разрыхляющими (разр) электронами. Заполнение молекулярных орбиталей происходит при соблюдении принципа Паули и правила Хунда по мере увеличения их энергии в такой последовательности:
и неустойчивость молекулы He2 и т.п.). Более плодотворным оказался другой подход к объяснению ковалентной связи – метод молекулярных орбиталей (МО). В методе МО состояние молекулы описывается как совокупность электронных молекулярных орбиталей. При этом число молекулярных орбиталей равно сумме атомных орбиталей. Молекулярной орбитали, возникающей от сложения атомных орбиталей (АО), соответствует более низкая энергия, чем исходным орбиталям. Такая МО имеет повышенную электронную плотность в пространстве между ядрами, способствует образованию химической связи и называется связывающей. Молекулярной орбитали, образовавшейся от вычитания атомных, соответствует более высокая энергия, чем атомным орбиталям. Электронная плотность в этом случае сконцентрирована за ядрами атомов, а между ними равна нулю. Подобные МО энергетически менее выгодны, чем исходные АО, они приводят к ослаблению химической связи и называются разрыхляющими. Электроны, занимающие связывающие и разрыхляющие орбитали, называют соответственно связывающими (св) и разрыхляющими (разр) электронами. Заполнение молекулярных орбиталей происходит при соблюдении принципа Паули и правила Хунда по мере увеличения их энергии в такой последовательности:
σсв1 s < σразр1 s < σсв2 s < σразр2 s < σсв2 p x< πсв2 p y=πсв2 p z<πразр2 p y=πразр2 p z < σразр2 p x.
На рис. 1 изображена энергетическая схема образования молекулярных орбиталей из атомных для двухатомных гомоядерных (одного и того же элемента) молекул элементов второго периода. Число связывающих и разрыхляющих электронов зависит от их числа в атомах исходных элементов.
Следует отметить, что при образовании молекул B2, C2, и N2 энергия связывающей σ2 p x-орбитали больше энергии связывающих π2 p y- и π2 p z-орбиталей, тогда как в молекулах O2 и F2, наоборот, энергия связывающих π2 p y- и π2 p z-орбиталей больше энергии связывающей σ2px-орбитали. Это нужно учитывать при изображении энергетических схем (рис. 1) соответствующих молекул.
Порядок связи в молекуле определяется разностью между числом связывающих и разрыхляющих орбиталей, деленной на два. Порядок связи может быть равен нулю (молекула не существует), целому или дробному положительному числу.
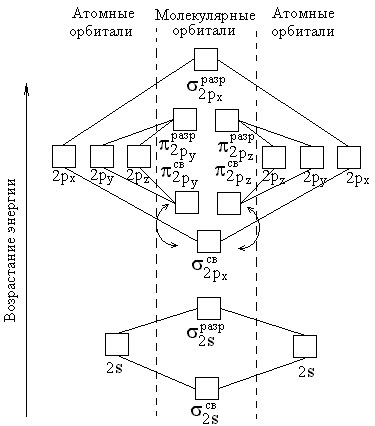
Рис.1. Энергетическая схема образования молекулярных орбиталей из
атомных для гомоядерных молекул второго периода
Подобно электронным формулам, показывающим распределение электронов в атоме по атомным орбиталям, в методе МО составляют формулы молекул, отражающие их электронную конфигурацию. По аналогии с атомными s-, p-, d-, f -орбиталями молекулярные орбитали обозначаются греческими буквами σ, π, δ, φ.
Так, электронная конфигурация молекул О2 описывается следующим образом:
O2[KK (σ2sсв)2 (σ2sразр)2 (σ2 p xсв)2 (π2 p yсв)2(π2 p zсв)2 (π2 p yраз)1(π2 p zразр )1].
Буквами КК показано, что четыре 1 s -электрона (два связывающих и два разрыхляющих) практически не оказывают влияния на химическую связь.
Пример 4. Сера образует химические связи с калием, водородом, бромом и углеродом. Какие из связей наиболее и наименее полярны? Укажите, в сторону какого атома смещается общая электронная пара?
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 855; Нарушение авторских прав?; Мы поможем в написании вашей работы!